Lääkinnällisten laitteiden valvonta tiukkenee
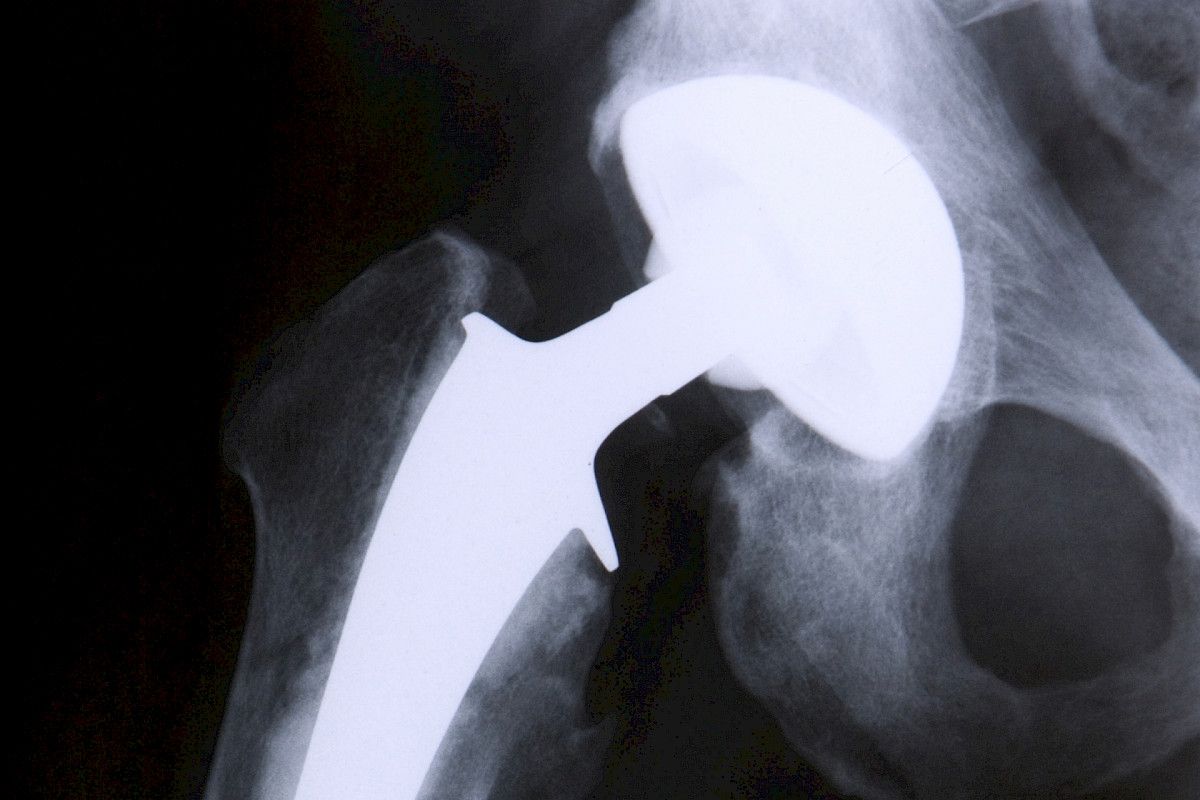
EU:n uudet säännöt koskevat muun muassa rintaimplantteja ja lonkkaproteeseja.
EU:n parlamentti on hyväksynyt uudet säännöt, joilla halutaan taata lääkinnällisten laitteiden jäljitettävyys ja varmistaa, että laitteet noudattavat EU:n potilasturvallisuusvaatimuksia.
Tällaisia lääkinnällisiä laitteita ovat muun muassa rintaimplantit ja lonkkaproteesit.
Yksilöllistä laitetunnistetta varten perustetaan sähköinen järjestelmä eli UDI-tietokanta, jotta voidaan varmistaa muun muassa potilaisiin implantoitujen laitteiden jäljittäminen. Potilaille annetaan implanttikortti, jolla myös he voivat saada tietoa UDI-tietokannasta.
Uudet säännöt tiukentavat esimerkiksi raskaus- ja DNA-testeissä käytettyjen diagnostisten lääkinnällisten laitteiden eettisiä vaatimuksia.
Uudet säännökset koskevat myös in vitro -diagnostiikkaan tarkoitettuja lääkinnällisiä laitteita. Lainsäädäntö edellyttää myös, että potilaille kerrotaan DNA-testien seurauksista.
Säännöksiä kehitettäessä on otettu oppia rintaimplantti- ja lonkkaproteesiskandaaleista.
Uusien sääntöjen mukaan:
– Valmistajien toimintaa valvotaan satunnaistarkastuksin sen jälkeen, kun laitteet on saatettu markkinoille.
– Ns. ilmoitettuja tarkastuslaitoksia valvotaan tiukemmin, ja laitosten edellytetään käyttävän myös kliinisiä asiantuntijoita.
– Korkean riskin laitteita, kuten rintaimplanttien ja HIV-testien turvallisuutta valvotaan erityisillä lisätarkastuksilla. Tästä valvonnasta vastaa ilmoitettujen laitosten lisäksi erityinen asiantuntijakomitea.
– Potilaille annetaan "implanttikortti", jonka avulla potilaat ja lääkärit pystyvät jäljittämään, mikä lääkinnällinen laite potilaalla on.
– Valmistajien tulee osoittaa kliininen näyttö erityisesti korkean riskin lääkinnällisten laitteiden turvallisuudesta.
Lue lisää Valviran sivuilta.
Kuva: Panthermedia