Ratkaiseeko ensimmäisen vuoden hoitotulos astmapotilaan pitkäaikaisennusteen?
Lähtökohdat
Inhaloitava kortikosterioidi on ollut astman perushoito jo 30 vuotta, mutta pitkäaikaisseurantoja sen käytöstä on vähän. Tässä tutkimuksessa selvitettiin aikuisena astmaan sairastuneiden vointia ja lääkkeiden käyttömäärää.
Menetelmät
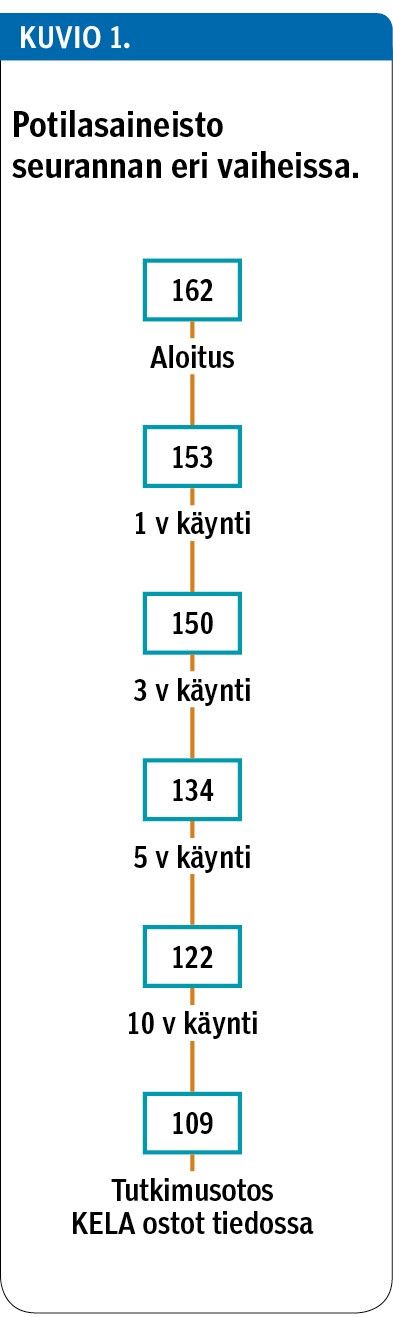
Aineistona oli 162 vuosina 1991–1993 peräkkäin diagnosoitua astmapotilasta (keski-ikä alussa 42,1 v). Kymmenvuotistarkastukseen tuli 122 potilasta. Heiltä tutkittiin keuhkofunktiot (histamiinialtistus, spirometria ja PEF) ja elämänlaatu (St. Georges Respiratory Questionnaire ja 15D) sekä arvioitiin astman hallinta (Global Initiative for Asthma, GINA 2008). Tiedot lääkeostoista saatiin Kelasta 109 potilaasta.
Tulokset
Pitkän ajan hoitotulosta ennustivat ensimmäisen hoitovuoden lopussa ja ennen hoitoa mitattu FEV1 sekä tupakointi. Hoitotulos ei korreloinut ostettujen inhaloitavien kortikosteroidien määrään. Ostettujen lääkkeiden määrät olivat kohtuulliset ja ne vähenivät seurannan aikana. Potilaiden ilmoittama lääkkeiden käyttö oli suurempi kuin Kelan kirjaamat ostot; ero oli tilastollisesti erittäin merkitsevä (p < 0,001). Seurannan lopussa astma oli täysin hallinnassa 23 %:lla potilaista ja osittain 52 %:lla, mutta 25 %:lla se ei ollut hallinnassa.
Päätelmät
Aikuisiässä astmaan sairastuneen potilaan ensimmäinen hoitovuosi on tärkeä, sillä sen hoitotulos näyttää olevan yhteydessä pitkäaikaistulokseen. Lääkkeiden todellinen käyttö on tärkeää tarkistaa, samoin taito käyttää niitä.
Astman hoidossa on Suomessa noudatettu parin vuosikymmenen ajan astmaohjelman mukaisia hoitoperiaatteita (1). Seurantatutkimuksen mukaan astman ennuste on parantunut viime vuosien aikana (2,3,4). Ennuste on hyvä erityisesti keuhkojen toimintakokeilla mitattuna, mutta hoitotasapainon saavuttamisessa on parannettavaa (5). Aikuisiässä alkaneen astman pitkäaikaisennusteesta, lääkityksestä ja lääkityksen suhteesta hoitotuloksiin on niukasti julkaisuja (6). Alkuvaiheen tehokkaan hoidon viivästyminen voi olla yhteydessä huonontuviin hoitotuloksiin (7).
Olemme aiemmin julkaisseet astman omahoidon ohjaukseen osallistuneiden potilaiden kymmenen vuoden seurantatutkimuksen (8). Nyt selvitimme saman aineiston perusteella Kansaneläkelaitoksen rekisteristä (Kela) saaduista seitsemän vuoden lääkeostotiedoista astmalääkkeiden käyttöä ja lääkkeiden käytön yhteyttä saavutettuun hoitotulokseen. Ostotiedot ovat saatavissa vain niistä henkilöistä, jotka olivat käyttäneet erityiskorvausoikeuttaan.
Aineisto ja menetelmät
Potilasaineisto muodostui valikoimattomista, vuosina 1991–1993 peräkkäin diagnosoiduista, enintään kymmenen askivuotta tupakoineista 162 uudesta aikuisiässä sairastuneesta astmapotilaasta (miehiä 60, naisia 102). Potilaiden ikä oli tutkimuksen alussa keskimäärin 42,1 vuotta, (95 %:n LV 39,2–45,1 v). Tutkimukseen osallistuneet henkilöt kävivät erikoispoliklinikalla tutkimussuunnitelman mukaisilla tarkastuskäyneillä 1, 3, 5 ja 10 vuoden kohdalla. Väliaikana he olivat terveyskeskuksen, työterveyshuollon tai yksityislääkärin seurannassa ja ostivat itse lääkkeensä, joten tutkimusasetelma vastasi normaalia hoitotilannetta.
Etelä-Karjalan keskussairaalan eettinen toimikunta on hyväksynyt tutkimussuunnitelman ja potilaat ovat antaneet suostumuksensa kymmenvuotistarkastaukseen.
Kymmenvuotistarkastukseen tuli 122 henkilöä. Seurannan aikana 7 oli kuollut (ei astmaan), 14 muuttanut pois ja 19 ei halunnut tulla kontrollikäynnille, koska kokivat sen turhaksi (kuvio 1). Nämä 19 kieltäytynyttä eivät eronneet tarkastukseen tulleista iän, sukupuolijakauman tai atopian esiintyvyyden suhteen eikä tilastollisesti merkitsevää eroa ollut sekuntikapasiteetissa (FEV1) ja PEF-arvoissa tutkimuksen alussa, yhden ja viiden vuoden hoidon jälkeen. Kontrolliin tulleista henkilöistä 109 potilaan astmalääkkeiden ostoista löytyi tieto Kelan rekisteristä, ja he muodostivat tämän tutkimuksen aineiston. Potilaskohtaiset ostot kerättiin henkilötunnusta ja astman erityiskorvausnumeroa käyttäen.
Kelan tiedot potilaiden lääkeostoista olivat saatavissa seurannan neljännestä vuodesta lähtien. Jokaisella kontrollikäynnillä potilailta kysyttiin ja kirjattiin lääkkeiden käyttö. Ostetuista inhaloitavista steroideista ja lyhytvaikutteisista sympatomimeeteistä laskettiin keskimääräinen päiväannos. Inhaloitavat steroidit muutettiin beklometasoniekvivalenteiksi annoksiksi (0,2 mg budesonidia = 0,1 mg flutikasonia = 0,2 mg beklometasonia). Potilaat luokiteltiin inhaloitavien steroidien satunnaiskäyttäjiksi, kun ostettu lääkemäärä oli alle 0,2 mg/vrk, vähän eli enintään 0,5 mg/ vrk käyttäneiksi, kohtalaisesti eli 0,51–1,0 mg/vrk käyttäneiksi ja runsaasti eli yli 1,0 mg/vrk käyttäneiksi. Sympatomimeetit laskettiin annoksina niin, että yksi annos salbutamolia oli 0,2 mg ja terbutaliinia 0,5 mg. Pitkävaikutteiset sympatomimeetit tulivat käyttöön vasta tutkimuksen neljäntenä vuonna.
Kontrollikäynneillä tehdyt seurantatutkimukset on kuvattu aiemmin (9). Spirometria tehtiin peruslääkityksellä ilman edeltävää keuhkoputkia laajentavaa lääkitystä. Keuhkofunktion ryhmittelyssä normaalin uloshengityksen sekuntikapasiteetin (FEV1) rajana oli 80 % viitetasosta.
Elämänlaatua tutkittiin käyttäen sekä astmalle spesifistä St. Georges Respiratory Questionnairea (SGRQ) (10) että yleismittaria 15D (11,12). Viimeisellä kontrollikäynnillä kirjattujen tietojen perusteella (yö- ja päiväoireet, avaavan lääkkeen käyttö, FEV1) määritettiin astman hallintaa kuvaava Global Initiative for Asthma (GINA 2008) -luokituksen mukainen luokka, jonka mukaan astma on hallinnassa, osittain hallinnassa tai ei hallinnassa (13).
Atooppisiksi määriteltiin potilaat, joilla oli vähintään kaksi positiivista ihopistokoetulosta. Tutkimuksen alussa astman fenotypiat olivat allerginen tai sisäsyntyinen astma.
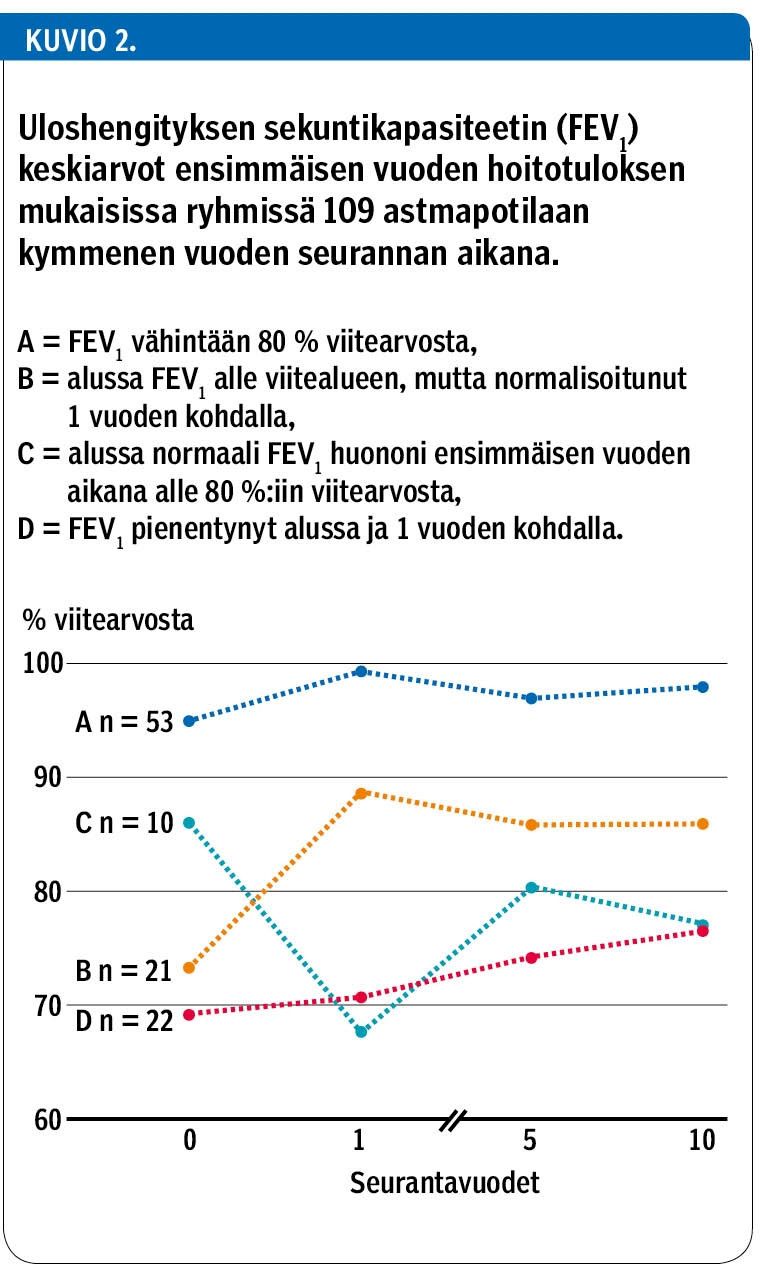
Potilaat jaettiin ensimmäisen hoitovuoden FEV1-muutoksen mukaan 4 ryhmään. Ryhmässä A (53 potilasta) oli hoidon alussa ja vuoden kuluttua normaali FEV1. Ryhmässä B (21 potilasta) alussa pienentynyt FEV1 parani ensimmäisen hoitovuoden aikana normaaliksi. Ryhmässä C (10 potilasta) FEV1 oli alussa normaali, mutta huononi ensimmäisen vuoden aikana alle viitearvon. Ryhmässä D (22 potilasta) FEV1 oli alussa ja yhden vuoden kohdalla alle viitearvon.
Tilastomenetelmät
Mittasuureet ilmoitetaan keskiarvoina (ka) ja 95 %:n luottamusvälein (LV). Erot ryhmien kesken on testattu riippumattomien suureiden t-testillä. Eri tutkimuskertojen välistä eroa on testattu toistettujen mittausten t-testillä. Erot jakaumien välillä on testattu χ2-testillä. Monimuuttujamenetelmänä käytettiin valikoivaa (askeltavaa) regressioanalyysiä. Regressiomallissa selittävinä tekijöinä olivat sukupuoli, ikä, atopia, inhaloitavan steroidin aloitusannos, ostettujen inhaloitavien steroidien sekä lyhyt- ja pitkävaikutteisten sympatomimeettien määrät, tupakointi (ei koskaan tai lopettaneet vs. edelleen polttava) sekä FEV1 ennen hoitoa ja ensimmäisen vuoden lopussa.
Analyysit on tehty suomalaisella PATO-tilastomatematiikkaohjelmalla, versio 4.5 (Mikrovuo Oy, Forssa). Testeissä merkitsevänä erona pidettiin p-arvoa < 0,05.
Tulokset
Mittaustulokset
Tutkimukseen osallistuneiden 109 potilaan ikä oli seurannan lopussa 26–84 vuotta (keskiarvo 52,1 v). Heistä miehiä oli 36 (33 %) ja atoopikkoja 57 henkilöä (53 %). Spirometrian tulokset kaikilta kontrollikerroilta oli tiedossa 106 potilaalta (kolmelta puuttui ensimmäisen vuoden mittaus).
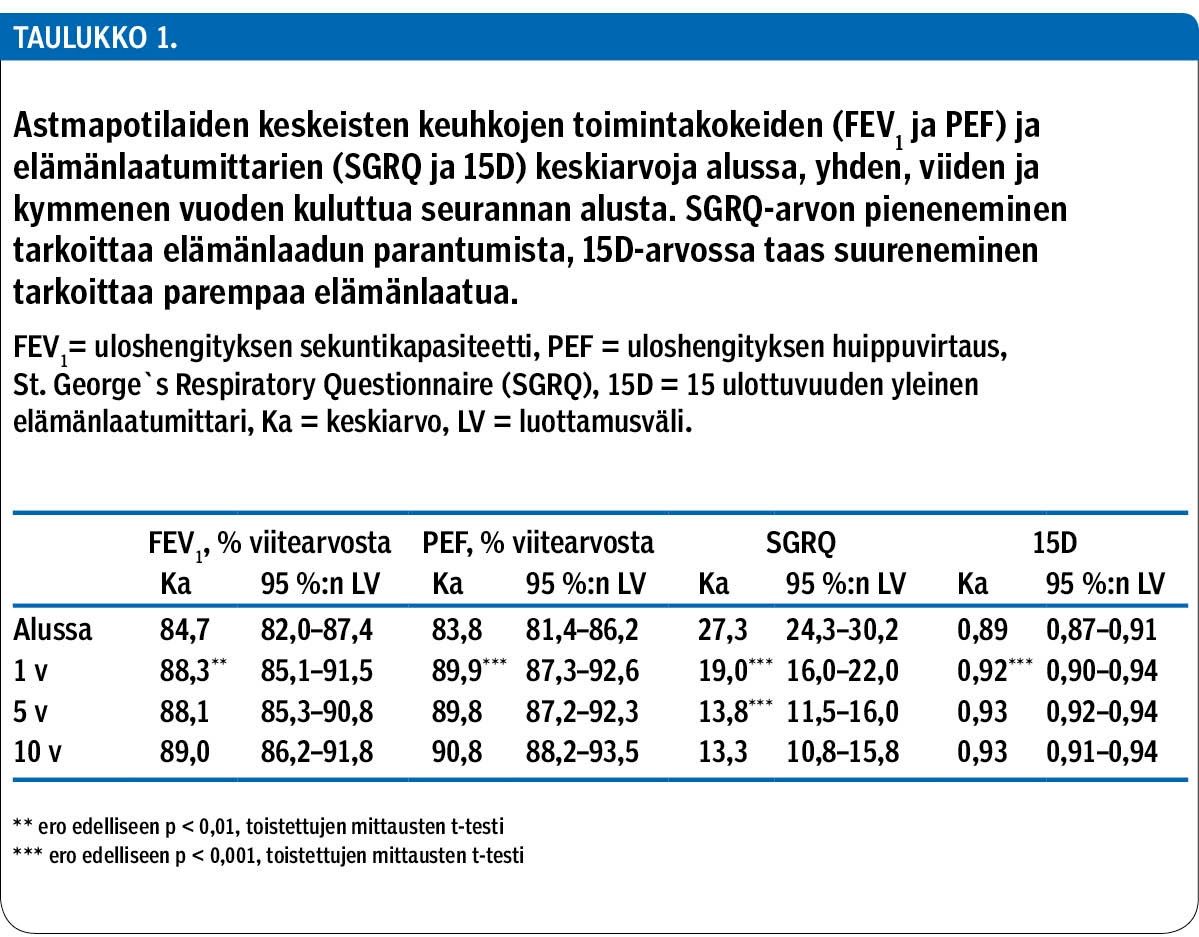
Koko aineiston PEF- ja FEV1-arvot paranivat tilastollisesti merkitsevästi ensimmäisen vuoden aikana ja pysyivät sillä tasolla seurannan loppuun asti. Samoin parani yleistä elämänlaatua mittaavan (15D) mittaustulos. Astmaspesifisellä mittarilla (SGRQ) mitaten elämänlaatu parani viiteen vuoteen asti ja säilyi saavutetulla tasolla (taulukko 1). GINA-luokituksen mukainen hallinta-asteen arviointi tehtiin kymmenennen hoitovuoden tietojen perusteella. Astma oli täysin hallinnassa 23 %:lla (25 henkilöä), osittain hallinnassa 52 %:lla (57 henkilöä) ja ei hallinnassa 25 %:lla (27 henkilöä).
Potilasryhmät A–D muodostettiin ensimmäisen hoitovuoden aikana tapahtuneen FEV1-muutoksen mukaan, ja ryhmissä todettiin tämän ensimmäisen hoitovuoden muutoksen yhteys pitkäaikaisennusteeseen (kuvio 2). Valikoivan regressioanalyysin mukaan kymmenennen vuoden FEV1-arvoa selittävät vain ensimmäisen hoitovuoden jälkeinen FEV1-arvo (korrelaatiokerroin 0,642, p < 0,001), ennen hoitoa mitattu FEV1-arvo (korrelaatiokerroin 0,335, p < 0,01) sekä tupakointi (korrelaatiokerroin 0,243, p < 0,05).
Ensimmäisen hoitovuoden aikana tapahtuneen FEV1-muutoksen mukaiset ryhmät A–D eivät eronneet tilastollisesti toisistaan sukupuolen tai aloitusvaiheen tupakoinnin suhteen. A-ryhmässä oli eniten tupakoinnin lopettaneita (kahdeksan potilasta kymmenestä) ja atoopikkoja (χ2-testi, p < 0,01). Toisaalta D-ryhmän potilaat olivat merkitsevästi vanhempia kuin A-ryhmän (D-ryhmä ka 62,2 vuotta, 95 %:n LV 56,3–68,2 ja A-ryhmä ka 48,2 vuotta, 95 %:n LV 44,2–52,1) (t-testi, p < 0,001).
Tupakoinnin vaikutus
Kaikkiaan 23 tupakoineesta astmapotilaasta tupakoinnin lopetti seurannan aikana 15. Tupakointia jatkaneilla FEV1 huononi seurannan aikana keskimäärin 6,4 prosenttiyksikköä (95 %:n LV –14,8–2,1). Sen sijaan tupakoinnin lopettaneilla se korjaantui keskimäärin 1,7 prosenttiyksikköä (95 %:n LV –1,8–5,2). Muutoksen ero oli tilastollisesti merkitsevä (t-testi, p < 0,05). Potilailla, jotka eivät koskaan olleet tupakoineet, FEV1 korjaantui keskimäärin 6,7 prosenttiyksikköä (95 %:n LV 3,6–9,8). Ero tupakoivien vastaavaan muutokseen oli merkitsevä (p < 0,01).
Inhaloitavan kortikosteroidin käyttö
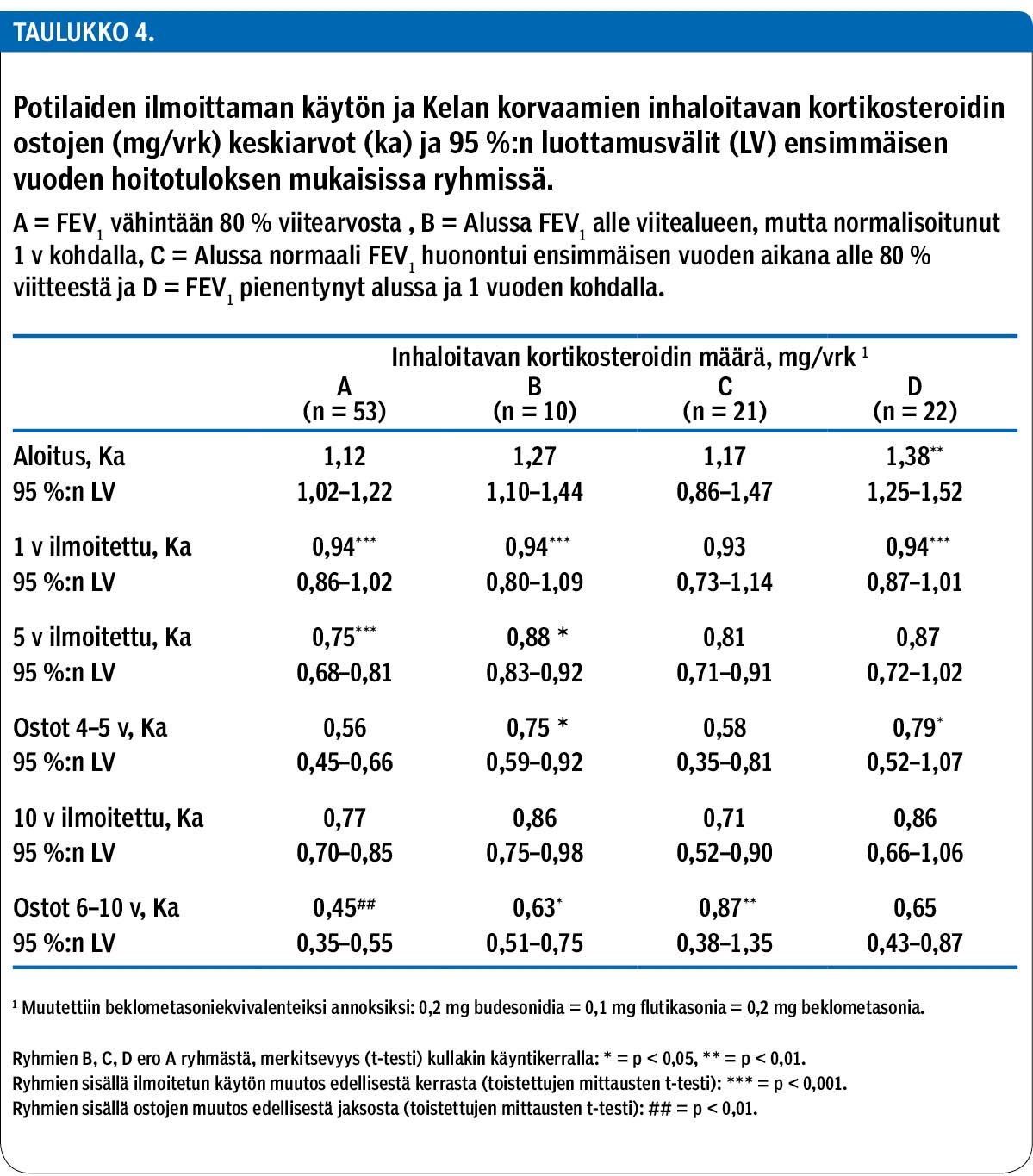
Inhaloitavan kortikosteroidin aloitusannos oli keskimäärin 1,21 mg/vrk (95 %:n LV 1,15–1,28). Sen käyttö väheni potilaiden ilmoituksen mukaan ensimmäisten viiden vuoden aikana ja pysyi sillä tasolla jatkoseurannan ajan. Ostotietojen mukaan inhaloitavien kortikosteroidien käyttö oli seurannan neljännen ja viidennen vuoden aikana 0,65 mg/vrk (95 %:n LV 0,57–0,73) ja se väheni seurannan aikana (taulukko 2). Tutkimuksen viimeisten 12 kuukauden ostot vastasivat annostasoa 0,44 mg/vrk (95 %:n LV 0,37–0,51) . Potilaiden ilmoittamat ja ostotietojen mukaiset käytöt erosivat tilastollisesti merkitsevästi sekä neljännen ja viidennen vuoden (t-testi p < 0,05) että viimeisen vuoden aikana (p < 0,001).
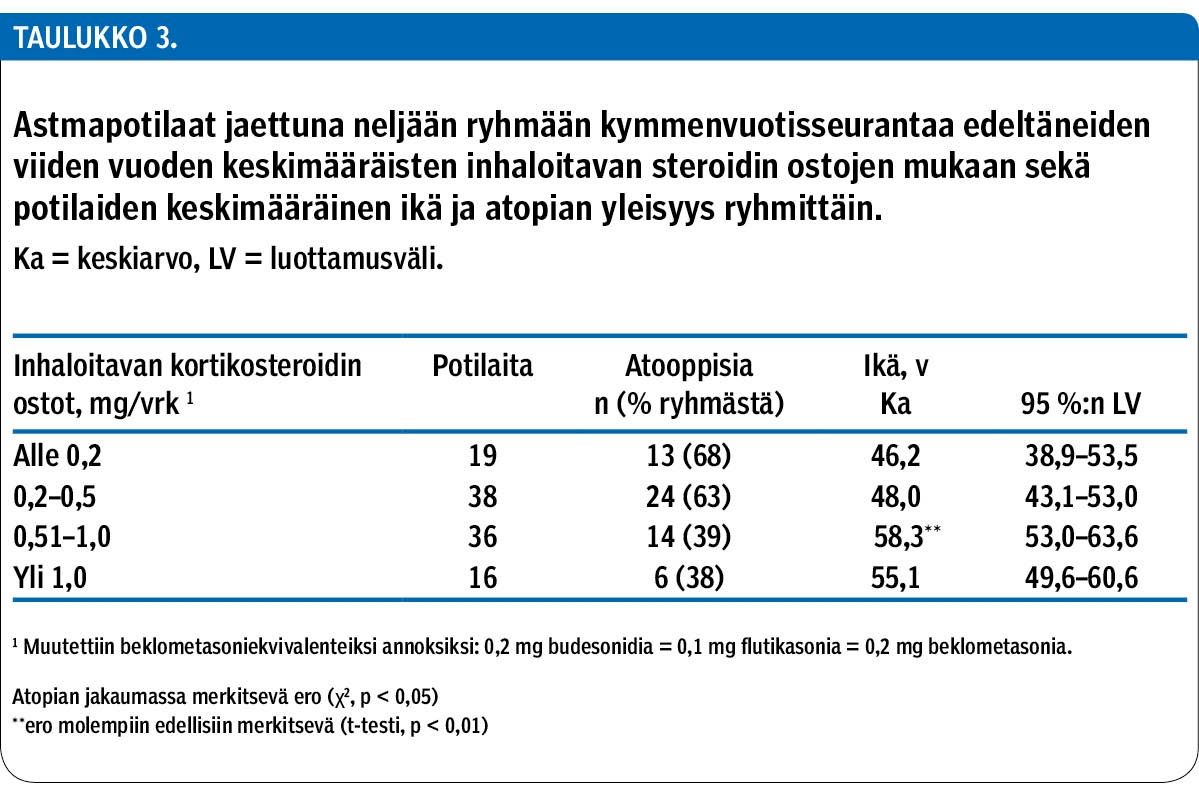
Vähemmän inhaloitavia kortikosteroideja ostaneet olivat nuorempia (t-testi, p < 0,01) ja useimmin atoopikkoja kuin runsaammin näitä lääkkeitä ostaneet (χ2-testi, p < 0,05) (taulukko 3). Muuten ostomäärän mukaiset ryhmät eivät eronneet tilastollisesti toisistaan sukupuolen, tupakoinnin, lääkkeestä koetun tai epäillyn haitan suhteen. Eroja ei ollut myöskään kymmenvuotistarkastuksen elämänlaatukyselyjen, PEF-mittausten ja sekuntikapasiteetin tuloksissa eikä astman hallinnan mukaisissa ryhmissä.
Uloshengityksen sekuntikapasiteetin muutoksen mukaisissa ryhmissä (A–D) hoidon aloitusannokset olivat suunnilleen samat ryhmissä A–C, mutta merkitsevästi suuremmat D-ryhmässä (FEV1 oli viitearvoa matalampi) (taulukko 4). Käyttöannokset pienenivät ensimmäisen hoitovuoden aikana erittäin merkitsevästi muissa paitsi C-ryhmässä (alussa ollut normaali FEV1 pieneni). Ilmoitettu käyttö pieneni edelleen viidenteen hoitovuoteen asti merkitsevästi ryhmissä A ja B. Kelan tilastojen mukaiset inhaloitavien kortikosteroidien ostot olivat pienimmät A-ryhmän potilailla (taulukko 4).
Muut astmalääkkeet
Viiden edeltäneen hoitovuoden aikana lyhytvaikutteisten sympatomimeettien keskimääräinen osto vastasi 1,26 annosta/vrk (95 %:n LV 0,91–1,61). Ostoissa ei ollut merkitseviä eroja ryhmissä A–D.
Pitkävaikutteiset sympatomimeetit tulivat käyttöön vasta seurannan neljäntenä vuonna. Niitä oli ostanut 37 henkilöä ja osto vastasi keskimäärin 0,84 annosta (95 %:n LV 0,61–1,06). Heillä oli kymmenvuotistarkastauksessa huonompi FEV1 (keskiarvo 83,8 % viitearvosta, 95 %:n LV 78,7–89,0 %) kuin potilailla, jotka eivät käyttäneet näitä lääkkeitä (91,6 %, 95 %:n LV 88,4–94,8 %) (t-testi p < 0,01), ja he olivat harvemmin atooppisia (36 % vs. 64 %, χ2-testi p < 0,05).
Nedokromiilia käytti kuusi potilasta ensimmäisten kolmen kuukauden ajan, mutta sen jälkeen he siirtyivät inhaloitaviin kortikosteroideihin. Montelukastia oli inhaloitavan kortikosteroidin lisänä ajoittain ostanut 18 potilasta.
Kortisonikuureja oli koko kymmenen vuoden aikana käyttänyt 18 henkilöä keskimäärin 2,9 kertaa (95 %:n LV 2,2–3,7).
Pohdinta
Tutkimuksessamme astman hoitotasapainoa kuvaavat mittarit korjaantuivat pääasiassa ensimmäisen hoitovuoden aikana. Kymmenennen hoitovuoden tulos saattaa olla ennustettavissa ensimmäisen hoitovuoden aikana tapahtuneen uloshengityksen sekuntikapasiteetin muutoksen ja tupakointitiedon perusteella. Tällaista havaintoa ei tietääksemme ole aikaisemmin julkaistu. Tulos tulisi varmistaa etenevässä hoitotutkimuksessa, ja siinä voitaisiin myös selvittää astman hoitotulokseen vaikuttavat muut riskitekijät (4) ja voiko ennustetta parantaa muuttamalla hoitoa ensimmäisen vuoden tulosten perusteella.
Tuloksen perusteella käytännön työssä tulisi kiinnittää huomio niiden potilaiden hoitoon, joiden astma ei FEV1-arvon perusteella ole hallinnassa ensimmäisen hoitovuoden lopulla. Tätä tukee de Marcon ym. havainto 9 vuoden seurantatutkimuksesta, jossa ensimmäisen hoitovuoden aikana tapahtunut keuhkotoiminnan huononeminen ennusti vaikeampaa astmaa (14). Toisaalta Haahtelan ym. 13 vuoden seurannassa spirometriatulokset paranivat samalla tavalla vuoden viiveellä kuin alusta alkaen hoitoa saaneiden ryhmissä, vaikka viivästyneesti inhaloitavan kortikosteroidihoidon saaneiden astmatasapaino oli muuten hiukan huonompi. Haahtelan ym. tutkimuksessa ei ollut alaryhmäanalyysiä FEV1:n paranemisen mukaan (7). Aiemmin on havaittu, että lääkehoidossa olevien astmapotilaiden suorituskyvyssä tai keuhkofunktioissa ei tapahtunut pidemmänkään seurannan aikana enää merkitsevää heikkenemistä (15,16,17). On ilmeistä, että astman biologisen luonteen vaihtelu vaikuttaa hoitovasteeseen, kuten nykyinen fenotyyppien luokitus antaa aihetta odottaa (18,19,20,21,22,23). Tätä ajatusta tukee myös se, että potilaat, joiden FEV1-arvo oli matala ensimmäisen hoitovuoden jälkeen, olivat vanhempia ja harvemmin atoopikkoja. Toisin sanoen atoppisen astman ennuste oli parempi kuin ei-atooppisen.
Tässä tutkimuksessa noudatettiin hoitoperiaatetta, joka vastasi myöhemmin julkaistua astmaohjelmaa (1). Hoito aloitettiin suuremmalla inhaloitavan kortikosteroidin annoksella, ja annos puolitettiin 2–3 kuukauden hoidon jälkeen. Ensimmäisen vuoden lopulla hoitoannos vastasi 4–5 annosta/vrk 200 µg:n vahvuista beklometasonia. Hoitotulos kymmenennen vuoden kohdalla FEV1-arvolla mitattuna ei korreloinut käytettyyn inhaloitavan kortikosteroidin määrään, joskin potilaat, joiden FEV1-arvo oli matala, käyttivät inhaloitavaa kortikosteroidia enemmän kuin potilaat, joiden FEV1 oli normaali. Hoitavan lääkkeen käyttömäärä väheni merkitsevästi hoitovuosien aikana. Ostojen perusteella viimeisen hoitovuoden keskimääräinen päivittäinen inhaloitavan kortikosteroidin käyttö vastasi 2–3 annosta 200 µg:n vahvuista beklometasonia, ja tämä oli 64 % potilaiden ilmoittamasta käyttömäärästä.
Tupakoitsijoita oli tässä seurantaryhmässä vähän. Tupakoinnin jatkaminen hoidon aikana huononsi hoitovastetta FEV1:n perusteella, mikä sopii aikaisempiin havaintoihin (24,25). Uloshengityksen sekuntikapasiteetin pieneneminen voi liittyä keuhkoahtaumataudin kehittymiseen, tai kyse voi olla tupakointiin liittyvästä steroideille resistentistä astmasta (27). Tupakoinnin lopettaminen hoidon aikana vaikutti suotuisasti hoitotulokseen. Tuloksemme vastaa osin aiempia tutkimuksia, joiden mukaan inhaloitavan steroidin käyttö näyttää hidastavan keuhkotoiminnan heikkenemistä (28,29) ja tupakointi huonontaa ennustetta (28,30).
Tutkimuksessa esiin tullut lyhytvaikutteisten sympatomimeettien käyttö oli kohtuullista, 1,26 annosta/vrk, mutta kuitenkin runsaampaa kuin nykyisen ohjeistuksen mukainen käyttö hallinnassa olevassa astmassa (alle 3 annosta viikossa) (13). Potilaita oli seuranta-aikana vallinneen käytännön mukaan neuvottu lisäämään lyhytvaikutteisen sympatomimeetin annoksia oirevaiheessa ja toisaalta suurentamaan inhaloitavan kortikosteroidin annosta vasta, jos tilanne ei korjaannu. Se ilmeisesti osittain vaikutti siihen, että GINA-luokituksen mukainen astman hallinta-aste oli hyvä vain 23 %:lla potilaista. Nykykäytännön mukainen yhdistelmähoito, jossa inhaloitavaan kortikosteroidiin yhdistetään pitkävaikutteinen sympatomimeetti, voi saada astman paremmin hallintaan. Toisaalta tulos tukee Hedmanin ym. aikaisempaa löydöstä, että astman hallinta ei ole niin hyvä kuin keuhkofunktiotutkimusten perusteella voisi odottaa (5). Käytännön työssä on tärkeä paneutua potilaiden kokemaan astman tasapainoon, oireiluun ja lääkkeiden oikeaan käyttöön.
GINA-luokituksen mukainen astman hallinta ei tilastollisesti korreloinut inhaloitavan kortikosteroidin käyttöön. Tämä viittaa siihen, että hoitotulos ei ole riippuvainen vain inhaloitavan steroidin käyttömäärästä, vaan taudin fenotyypin mukaisesta luonteesta. Potilaat myös tasapainoilevat oireiden ja hoitolääkkeiden lisäämiseen liittyvien (todellisten tai epäiltyjen) haittojen välillä. Huomionarvoista on se, että potilaiden ostamien inhaloitavien kortikosteroidien määrä oli 64 % heidän ilmoittamastaan käytöstä.
Pitkävaikutteinen sympatomimeetti tuli käyttöön vasta seurannan neljännen vuoden aikana, joten sillä ei ollut vaikutusta ensimmäisten vuosien tulokseen. Pitkävaikutteista sympatomimeettiä käytti tutkimuksen lopussa vain noin kolmannes tutkimukseen osallistuneista. Heillä oli sen lisäämisestä huolimatta seurannan lopussa huonompi FEV1 kuin muilla ja he käyttivät enemmän inhaloitavaa kortikosteroidia. Heillä saattoi olla vaikeampi taudinkuva ja erilainen taudin biologinen luonne, sillä he olivat vanhempia kuin muut potilaat ja atoopikkoja harvemmin.
Tämän tutkimuksen aloittamisen aikaan astma jaoteltiin atopian mukaan. Tarkempaa fenotypiamäärittelyä ei silloin tehty (19). Seurannassa ei kiinnitetty huomiota veren ja yskösten eosinofiliaan tai painoindeksiin, joten ylipainon vaikutusta hoitotuloksiin ei tässä tutkimuksessa voitu ottaa huomioon. Astman tasapaino arvioitiin seurantamittausten mukaan, mutta sitä, kuinka monella tauti oli remissiossa, ei erikseen määritelty.
Havaintomme ensimmäisen hoitovuoden uloshengityksen sekuntikapasiteetin yhteydestä myöhempään pitkäaikaishoitotulokseen vaatii varmistamista lisätutkimuksin, sillä tässä työssä alaryhmät jäivät pieneksi. Lisäksi olisi tarkemmin selvitettävä muiden tiedossa olevien riskitekijöiden vaikutus pitkäaikaistuloksiin (4).
Lääkkeiden käyttöä koskevan tuloksen luotettavuutta rajoittaa se, että ensimmäisten hoitovuosien tiedot käytön määristä perustuvat vain potilaiden ilmoittamaan. Lääkeostotiedot puuttuivat 13 potilaalta, vaikka he seurantatietojen mukaan sanoivat käyttävänsä lääkettä.
Vasta diagnosoidun, aikuisena alkaneen astman ensimmäisen vuoden hoitotulos näyttää olevan yhteydessä pitkäaikaishoidon tuloksiin. Potilaan seuranta ensimmäisen hoitovuoden aikana on tärkeää. Käytännön työssä on myös tärkeä paneutua potilaiden oikeaan lääkkeiden käyttöön. Erityisenä riskiryhmänä on otettava huomioon tupakoivat astmaatikot, joilla voi olla astman ja keuhkoahtaumataudin sekamuoto. Hoitotuloksen kannalta tärkeintä olisi, että tupakointi saataisiin loppumaan. Hoitoa on syytä tehostaa erityisesti silloin, jos astma ei ole hoitosuosituksen mukaisesti hallinnassa eli potilaalla on oireita, avaavan lääkkeen käyttöä tai FEV1- tai PEF-seuranta-arvo poikkeaa normaalista (31). Tällöin potilas ohjataan tarvittaessa erikoissairaanhoitoon.
Kiitämme Viipurin tuberkuloosisäätiötä apurahasta, professori Harri Sintosta elämänlaatuindeksien laskemisesta, Kelaa ja edesmennyttä tutkimusprofessori Timo Klaukkaa tutkimustyöhön innostamisesta ja lääkkeiden ostotiedoista, dosentti Jussi Karjalaista aineistoon tutustumisesta ja arvokkaista kommenteista.
Ritva Kauppinen, Vesa Vilkka: Apuraha (Viipurin tuberkuloosisäätiö).
Jouni Hedman: Konsultointipalkkiot (Astra Zeneca, GSK), luentopalkkiot (Astra Zeneca, GSK, Orion), osallistumis- ja matkakulut kansainvälisiin kongresseihin (Allmirall, GSK, Novartis).
Tästä asiasta tiedettiin
Keuhkojen toiminta kokeilla mitattuna astman ennuste on viime vuosikymmeninä parantunut, mutta oireiden perusteella astma ei ole aina täysin hallinnassa.
Astmapotilaat käyttävät usein vähemmän lääkettä kuin lääkäri on määrännyt.
Tupakointi huonontaa astmapotilaiden ennustetta.
Tämä tutkimus opetti
Astmapotilaan ensimmäisen hoitovuoden aikana tapahtunut toimintakokeiden muutos voi ennustaa pitkäaikaistulosta.
Potilaiden ostamat inhaloitavan steroidin määrät ovat kohtuulliset, ja ne ovat noin kaksi kolmasosaa siitä, mitä he ilmoittivat käyttävänsä.
Keuhkojen toimintakokeet pysyvät hyvinä, vaikka astmalääkkeiden käyttö vähenee ajan mittaan, mutta astma on täysin hallinnassa vain joka neljännellä potilaalla.
- 1
- Astmaohjelma 1994–2004. Sosiaali- ja terveysministeriön työryhmämuistioita 1994:16.
- 2
- Jantunen J ym. Astma- ja allergialääkkeiden kulutus kasvaa mutta kustannukset pienenevät. Suom Lääkäril 2015;70:3117–24.
- 3
- Haahtela T ym. A 10-year asthma programme in Finland: major change for the better. Thorax 2006;61:663–70.
- 4
- Kauppi P ym. Follow-up the Finnish Asthma Programme 2000-2010: reduction of hospital burden needs risk group rethinking. Thorax 2013;68: 292–3.
- 5
- Hedman J ym. Onko luulo suomalaisten astman hyvästä hoitotasapainosta tiedon väärtti? Suom Lääkäril 2008;63:2691–6.
- 6
- Tuomisto L ym. Prognosis of new-onset asthma diagnosed at adult age. Resp Med 2015;109:944–54.
- 7
- Haahtela T ym. Thirteen-year follow-up of early intervention with an inhaled corticosteroid in patients with asthma. J Allergy Clin Immunol 2009;124:1180–5.
- 8
- Kauppinen R ym. Ten-year follow-up of early intensive self-management guidance in newly diagnosed patients with asthma. J Asthma 2011;48:945–51.
- 9
- Kauppinen R ym. One-year economic evaluation of intensive vs conventional patient education and supervision for selfmanagement of new asthmatic patients. Respir Med 1998; 92:300–7.
- 10
- Jones PW ym. The St George’s Respiratory Questionnaire. Respir Med 1991;85 suppl B):25–31.
- 11
- Sintonen H, Pekurinen M. A fifteen-dimensional measure of life (15D) and its applications. Kirjassa: Walker SP, Rosser RM, toim. Quality of Life Assessment: Key Issues in the 1990s. Dordrecht, the Netherlands: Kluwer 1993:185–95.
- 12
- Aromaa A, Koskinen, toim. Health and Functional Capacity in Finland. Baseline Results of the Health 2000 Health Examination Survey. Publications of the National Public Health Institute, 2004, B12/2004.
- 13
- Global Strategy for Asthma Management and Prevention. Global Initiative for Asthma (GINA) 2008. Report updated 2008. hppt://www.ginasthma.org/
- 14
- de Marco R ym. Prognostic factors of asthma severity: a 9-year international prospective cohort study. J Allergy Clin Immunol 2006;117:1249–56.
- 15
- Shimoda T ym. Impact of inhaled corticosteroid treatment on 15-year longitudinal respiratory function changes in adult patients with bronchial asthma. Int Arch Allergy Immunol 2013;162:323–9.
- 16
- Ulrik CS ym. A 10 year follow up of 180 adults with bronchial asthma: factors important for the decline in lung function. Thorax 1992;47:14–8.
- 17
- Porpodis K ym. Long-term prognosis of asthma is good--a 12-year follow-up study. Influence of treatment. J Asthma 2009;46:625–31.
- 18
- Kauppi P. Onko aikuisten astman taudinkuva muuttunut? Suom Lääkäril 2015;70:1811–7.
- 19
- Cowan DC ym. Biomarker-based asthma phenotypes of corticosteroid response. J Allergy Clin Immunol 2015;4:877–83.
- 20
- Wenzel SE. Complex phenotypes in asthma: Current definitions. Pulm Pharmacol Ther 2013;26:710–5.
- 21
- Chung KF. Defining phenotypes in asthmatic: a step towards personalized medicine. Drugs 2014;74:719–28.
- 22
- Sutherland ER ym.National Heart, Lung and Blood Institute’s Asthma Clinical Research Network. Body mass index and phenotype in subjects with mild-to-moderate persistent asthma. J Allergy Clin Immunol 2009;123:1328–34.
- 23
- Westerhof GA ym. Predictors for the development of progressive severity in new-onset adult asthma. J Allergy Clin Immunol 2014;134:1051–6.
- 24
- Zheng X ym. Smoling influences response to inhaled corticosteroids in patients with asthma: a meta-analysis. Int Arch Allergy Immunol 2012;158:175–83.
- 25
- Telenga ED ym. Inflammation and corticosteroid responsiveness in ex-, current- and never-smoking asthmatics. Curr Med Res Opin 2012;28:1791–8.
- 26
- Barnes PJ. Corticosteroid resistance in patients with asthma and chronic obstructive pulmonary disease. J Allergy Clin Immunol 2013;131:636–45.
- 27
- Stapleton M ym. Smoking and asthma. J Am Board Fam Med 2011;24:313–22.
- 28
- van Schayck OC ym. Do asthmatic smokers benefit as much as non-smokers on budesonide/formoterol maintenance and reliever therapy? Results of an open label study. Respir Med 2012;106:189–96.
- 29
- Cerveri I ym. The impact of cigarette smoking on asthma: a polulation-based international cohort study. Int Arch Allergy Immunol 2012;158:175–83.
- 30
- Brusselle G ym. Real-life effectiveness of extrafine beclometasone dipropionate/formoterol in adults with persistent asthma according to smoking status. Respir Med 2012;106:811–9.
- 31
- Suomalaisen Lääkäriseuran Duodecimin ja Suomen Kardiologisen Seuran asettama työryhmä. Astma. Käypä hoito -suositus 24.9.2012. www.kaypahoito.fi
Is the first treatment year crucial for the prognosis of newly diagnosed adult onset asthma patients? Ten-year follow-up study.
Background
Inhaled corticosteroids (ICS) have been the basic asthma treatment for more than thirty years. During that time, the prognosis of asthma has improved. However, few long-term studies have been published about asthma patients’ real use of ICS. In this study we correlated the clinical 10-year follow-up results to the asthma drugs used according to the information given by the patients and to the data received from the Social Insurance Institution of Finland (Kela) concerning the drugs bought during the last seven follow-up years.
Methods
The material included those consecutive, newly diagnosed asthma patients participating in the ten-year study whose asthma drug purchase data had been submitted to Kela (n = 109). The clinical parameters included spirometry, peak flow measurements, disease specific quality of life (St George’s respiratory questionnaire) and general quality of life 15D (15 dimensions). Using the data collected at the final visit the control of asthma was estimated according to the Global Initiative for Asthma (GINA).
Results
The lung function parameters were good (mean > 80% of normal values). The long-term asthma lung function prognosis could be estimated from the FEV1 values at the beginning of treatment and after one year of treatment, as well as from the patient’s smoking habit.
The treatment results did not correlate with the ICS used. The amount of ICS used decreased during the follow-up, and during the last 12 months was on average 0.44 mg beclomethasone/day (95% CI 0.37–0.51). The patients communicated a greater use of ICS than that verified according to the data from Kela. The difference was significant during the last 12 months (p < 0.001). The patients used short-acting sympathomimetics, with a mean of 1.26 doses/day (95% CI 0.91–1.61). Long-acting sympathomimetics were not available before the fourth treatment year, and 37 patients used them with an average of 0.84 doses/day (95% CI 0.61–1.06). At the end of the follow-up, asthma was controlled (GINA 2008) in 23% (25 patients), partly controlled in 52% (57 patients), and not in control in 25% (27 patients) of the patients.
Conclusions
The long-term treatment outcome of a new adult asthma patient could be estimated from the change of FEV1 during the first treatment year and the patient’s smoking habit. As such, control at the end of the first treatment year is important, and the treatment schedule should be re-evaluated if the FEV1 has not improved. It is also important to determine the real doses of asthma drugs used. If the prognosis of the later treatment results seems to predict difficult asthma, there is reason to revise the treatment programme and to consult a specialist clinic if needed.