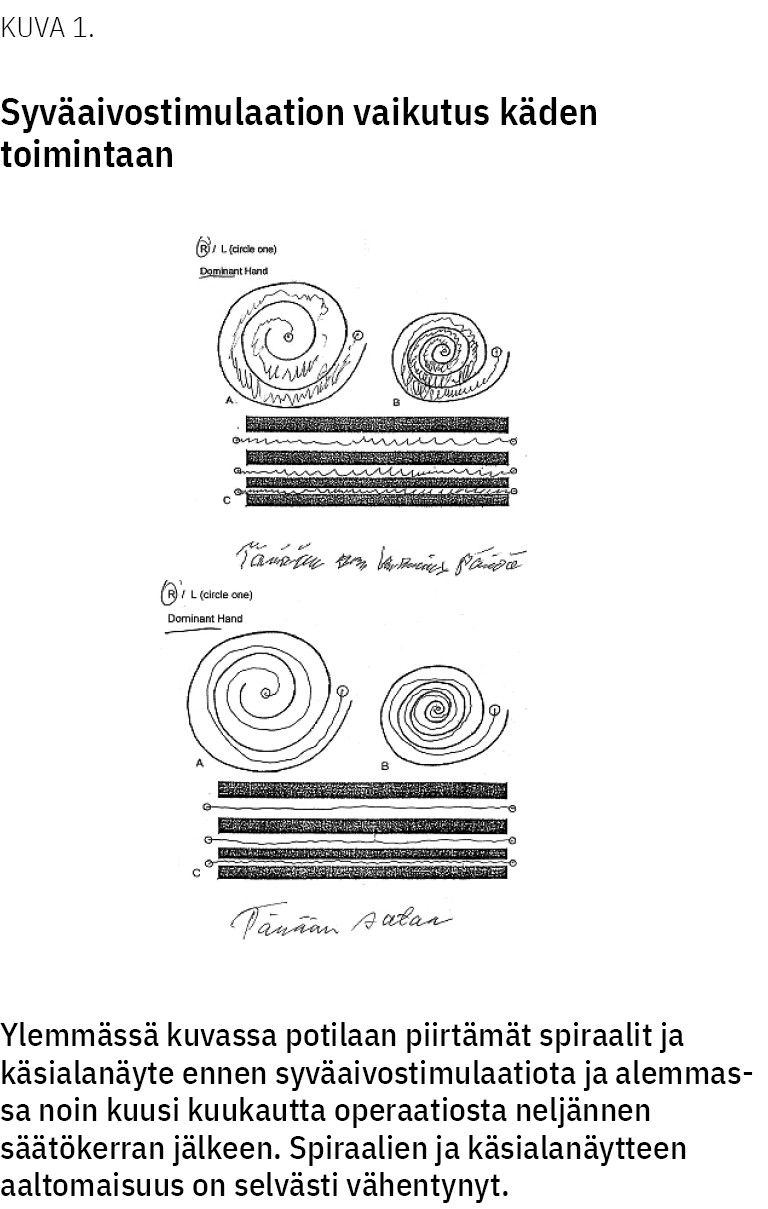
Essentiaalisen vapinan oireet, diagnostiikka ja hoito
• Keskeinen oire essentiaalisessa vapinassa on yläraajojen molemminpuolinen aktiovapina. Myös muiden alueiden vapinaa voi esiintyä.
• Oirekuvaan saattaa liittyä lieväasteisina myös muita neurologisia oireita, kuten lepovapinaa, kognitiivisia ongelmia, ataksiaa, ja tasapainon vaikeuksia.
• Muut kuin motoriset oireet, kuten mieliala- ja muistioireet, ovat myös tavallisia ja ne vaikuttavat merkittävästi elämänlaatuun.
• Lääkehoidosta hyötyy noin puolet potilaista. Vaikeassa sairaudessa on harkittava syväaivostimulaatiota.
Essentiaalinen vapina on tavallisin liikehäiriösairaus. Sairaus on monimuotoisempi kuin aiemmin uskottiin, ja joka kymmenennellä oirekuva etenee vaikea-asteiseksi (1). Vapinan lisäksi sairauteen saattaa liittyä myös merkittäviä ei-motorisia oireita kuten masennusta, ahdistusta ja muistioireita.
Esiintyvyydeksi on arvioitu 1 % väestöstä. Esiintyvyys kasvaa iän myötä: yli 65-vuotiaiden ikäryhmässä se on noin 5 % ja vanhimmassa ikäryhmässä jopa 20 % (2).
Oireet
Johto-oire on molemminpuolinen yläraajojen aktiovapina. Oirekuva saattaa alkaa toispuolisena, mutta sairauden edetessä oire leviää molempiin yläraajoihin. Lisäksi saattaa esiintyä muiden alueiden, kuten pään tai puheen vapinaa (3). Muita erillisiä vapinoita tai toispuolista yläraajan vapinaa ei pidä diagnosoida essentiaaliseksi vapinaksi.
Essentiaalisen vapinan diagnoosi suositellaan määritettäväksi vasta vapinan kestettyä vähintään kolme vuotta, jotta mahdollisten muiden neurologisten oireiden kehittyminen voidaan havaita (3). Vapina on luonteeltaan nopeataajuista käsien aktiovapinaa ja erityisesti kannatteluvapinaa. Se voi korostua kohdetta lähestyessä, jolloin puhutaan intentiovapinasta. Vapina haittaa usein päivittäistoimintoja, kuten kirjoittamista, syömistä ja juomista. Psyykkinen kuormitus voi korostaa oireita. Alkoholi tyypillisesti lievittää tilapäisesti vapinaa.
Muita neurologisia oireita ei saa puhtaassa essentiaalisessa vapinassa esiintyä (3). Viidesosalla potilaista oirekuva on monimuotoisempi, jolloin voi esiintyä lieväasteisena muita neurologisia oireita, kuten lepovapinaa, kognitiivisia ongelmia, ataksiaa, rigiditeettiä tai kävelyn ja tasapainon vaikeuksia (4). Tällöin on ehdotettu käytettävän essentiaalinen vapina plus -määritelmää. Termi on toistaiseksi kiistanalainen, eikä sitä pidä sekoittaa Parkinson plus -sairauksiin. Merkittävämmän neurologisen oireen esiintyminen on essentiaalisen vapinan poissulkukriteeri.
Muut kuin motoriset oireet
Ei-motorisia oireita saattaa esiintyä essentiaalisessa vapinassa, etenkin sairauden edenneessä vaiheessa. Erityisesti mielialan, muistin ja kognition ongelmia on todettu. Myös väsymystä, uniongelmia, kuulon heikkenemistä ja seksuaalitoimintojen ongelmia on havaittu enemmän kuin verrokeilla (5,6,7).
Masennusta ja ahdistusta on esiintynyt tutkimuksissa 50–80 %:lla essentiaalista vapinaa sairastavista; luku on samaa luokkaa kuin Parkinsonin taudissa ja dystoniassa (7,8,9). Kroonisen sairauden leima ja häpeä aiheuttavat osin mielialan muutoksia, mutta masennusta on todettu esiintyvän jo ennen diagnoosia. Sosiaalisten tilanteiden pelkoa esiintyi lähes puolella potilailla. Nämä oireet eivät korreloineet vapinan vaikeusasteeseen (10).
Muistin ja kognition ongelmat ovat yliedustettuina etenkin vanhemmalla iällä alkavassa tautimuodossa (5,7,11). Kognition ongelmat ovat usein lieviä, mutta yleensä ne etenevät (4,12). Häiriöt painottuvat keskittymisen ja toiminnanohjauksen häiriöihin sekä kielellisiin ongelmiin, mutta myös amnestisia ongelmia on todettu (12,13). Potilaat eivät aina tiedosta kognitiivisia ongelmia, joten niitä täytyy aktiivisesti seuloa (14).
Muut kuin motoriset oireet, etenkin masennus ja kognitiiviset oireet, ennustavat toimintakyvyn ja elämänlaadun heikkenemistä paremmin kuin vapinan vaikeusaste (5,15).
Etiologia
Yli puolella potilaista essentiaalisen vapinan on osoitettu periytyvän autosomaalisesti ja dominantisti. Jopa 96 % potilaista on samaa tautia sairastavia sukulaisia (16). Sairauden geneettinen tausta on monimuotoinen. Yksittäisen potilaan kohdalla ei suositella geneettisiä selvityksiä, eikä todettu mutaatio vaikuta hoitoon.
Neuropatologisesti on todettu pikkuaivojen degeneraatiota ja Purkinjen solujen vaurioita, jotka johtavat pikkuaivokuorelta lähtevän inhibitorisen hermotuksen vähenemiseen (17). Syväaivostimulaation (deep brain stimulation, DBS) hyvän teho essentiaalisessa vapinassa sopii hypoteesiin, jonka mukaan se estää pikkuaivoista talamukseen menevää patologista eksitaatiota. Osassa tutkimuksista on myös havaittu locus coeruleuksen solutuhoa, Lewyn kappaleita ja GABA-pitoisuuksien vähentymistä (18).
Erotusdiagnostiikka
Erotusdiagnostisesti on tärkeää arvioida fysiologisen vapinan mahdollisuus sekä sitä mahdollisesti korostavat metaboliset syyt ja lääkkeet (taulukko 1) (19).
Usein potilaat ovat huolissaan, että vapina viittaa Parkinsonin tautiin, jossa vapinaoireisto on tyypillisesti toispuolista lepovapinaa. Jos potilaalla on muita Parkinson-oireita, diagnostisia ongelmia ei yleensä esiinny (20).
Dystoninen vapina on usein pään alueen vapinaa, ja oirekuvaan liittyy dystonisia virheasentoja. Tosin dystoniapotilailla saattaa olla pitkään käsien liikevapinaa ilman poikkeavia asentoja (19).
Diagnostiset tutkimukset
Essentiaalisen vapinan diagnoosi perustuu kliiniseen tutkimukseen eikä kuvantamistutkimuksia yleensä tarvita. Tapauskohtaisesti voidaan harkita kuvantamista poissulkututkimuksena.
Kliiniseen tutkimukseen kuuluvat perusteellinen neurologinen tutkimus sekä verenpaineen ja pulssin mittaus ja kilpirauhasen palpointi. Metabolisten syiden poissulkemiseksi voi laboratoriokokeista tarkistaa tarpeen mukaan elektrolyytit, sokeri- ja kilpirauhasaineenvaihduntakokeet .
Vapinan esiintyminen ja vaikeusaste arvioidaan erikseen ylä- ja alaraajoista, pään alueelta, äänestä sekä vartalolta. Vapinaa arvioidaan levossa, raajaa kannatellessa sekä liikkeessä. Hyviä testejä ovat käsialanäyte, Arkhimedeen spiraalin jäljentäminen, veden kaataminen vesilasista toiseen ja juominen. Vapinaa on hyvä arvioida myös potilaan pukiessa sekä anamnestisesti muissa päivittäistoiminnoissa. Päivittäistoimintojen jäljitteleminen tutkimuksen aikana tarkentaa usein vapinan luonnetta.
Mahdolliset virheasennot ja poikkeavat liikkeet arvioidaan potilaan istuessa silmät auki ja kiinni, kirjoittaessa ja kävellessä. Kognitiivista oirekuvaa epäillessä voi suppeana tutkimuksena tehdä MoCA-testin (Montreal Cognitive Assessment), joka mittaa kielellisiä taitoja, toiminnanohjausta, visuospatiaalisia taitoja, viivepalautusta, tarkkaavuutta sekä orientaatiota (23). MMSE:tä (Mini-Mental State Examination) voi käyttää, joskin se on suunnattu Alzheimerin taudin diagnostiikkaan eikä ole yhtä herkkä havaitsemaan muita kognitiivisia ongelmia.
Jos todetaan paikallisiin muutoksiin sopivia löydöksiä, suositellaan kuvantamistutkimukseksi nuoremmille potilailla pään magneettikuvantamista ja vanhemmissa ikäryhmissä aivojen tietokonetomografiaa.
Jos essentiaaliseen vapimaan liittyy epätyypillisiä oireita kuten parkinsonismia, voidaan erotusdiagnostiikassa tarvittaessa tehdä aivojen dopamiinitransportterikuvantamistutkimus (Datscan), joka on essentiaalisessa vapinassa pääsääntöisesti normaali, toisin kuin Parkinsonin taudissa (24).
Hoito
Sairauteen ei ole parantavaa hoitoa. Oireenmukainen hoito perustuu lääkkeettömiin hoitomuotoihin, suun kautta otettaviin lääkkeisiin, botuliinitoksiinihoitoon, invasiivisiin hoitoihin sekä kuntoutukseen (25). Hoito on keskitetty perusterveydenhuoltoon, mutta vaikeissa tilanteissa on syytä pyytää neurologin kannanotto.
Stressitilanteen rauhoittaminen vähentää vapinaa. Vapinaa aiheuttavia lääkkeitä ja kofeiinia on hyvä välttää. Lääkkeettömänä hoitomuotona voi kokeilla raajan viilennys upottamalla se viileään veteen 10–15 minuutin ajaksi saattaa tilapäisesti helpottaa vapinaa.
Lääkehoito
Lääkehoitoa harkitaan, jos vapina aiheuttaa merkittävää toiminnallista haittaa. Noin puolet potilaista hyötyy suun kautta otettavista lääkkeistä (taulukko 2), ja vapina lievittyy yleensä 30–70 %.
Propranololista, primidonista ja topiramaatista on katsottu olevan hyötyä essentiaalisen vapinan hoidossa (25). Myös gabapentiiniä on käytetty hyvän siedettävyyden vuoksi, vaikka näyttö sen tehosta on vaihtelevaa. Näitä lääkkeitä käytetään pääasiassa säännöllisesti, mutta propranololia voi käyttää myös tarvittaessa.
Haittavaikutukset vaikeuttavat usein lääkityksen tehokasta käyttöä tai lääkkeitä käytetään liian pienellä annoksella. Etenkin primidonin ja topiramaatin annoksia suositellaan nostettavaksi hitaasti. Lääkityksiä voi tarvittaessa yhdistää riittävän vasteen saamiseksi (25).
Toistuvasti pistoshoitona annettavan botuliinitoksiinin on todettu auttavan vapinaan, mutta toiminnallisesti merkittävää lisähyötyä ei saatu (25). Pistoksia voi kokeilla erityisesti pään alueen ja äänen vapinaan, johon suun kautta otettavalla lääkityksellä ei usein ole vaikutusta.
Kirurginen hoito
Kirurgista hoitoa voidaan harkita vaikeaa essentiaalista vapinaa sairastaville potilaille, joille ei lääkehoidolla ole saavutettu tyydyttävää vastetta vapinaan ja joiden työkyky on uhattuna tai elämänlaatu on merkittävästi huonontunut (29). Käytettävissä on kolme hoitomuotoa: syväaivostimulaatio (deep brain stimulation, DBS), talamotomia ja uusimpana aivoihin kohdistettu ultraäänihoito (high intensity focused ultrasound, HIFU). Syväaivostimulaatio on lähes kokonaan syrjäyttänyt talamotomian.
Ennen toimenpidettä potilaan on hyväksyttävä hoitoon liittyvät riskit eli aivoverenvuoto, infektio ja puheen kankeus.
Yleisimmin kohdetumake essentiaalisen vapinan hoidossa on talamuksen ventraalinen tumake nucleus ventralis intermedius (VIM). Myös zona incerta (ZI) -tumaketta voidaan stimuloida. Syväaivostimulaatiossa elektrodit voidaan laittaa bilateraalisesti kohdetumakkeeseen. Uusi suunnattava elektrodi vähentää hoitoon liittyviä sivuvaikutuksia, kuten puhevaikeutta.
Ensimmäisen kuuden kuukauden aikana vaaditaan useita säätökertoja optimaalisen vasteen saamiseksi. Parhaimmillaan syväaivostimulaatio lievittää vapinaa niin, että potilas voi jatkaa työuraansa. Hän voi esimerkiksi juoda jälleen vesilasista yhdellä kädellä, käyttää turvallisesti veistä ja haarukkaa sekä kirjoittaa (kuva 1). Kirjallisuuden mukaan bilateraalinen VIM-tumakkeen stimulaatio voi lievittää vapinaa jopa 78 % verrattuna lähtötasoon (30).
Vaste syväaivostimulaatioon voi kestää jopa yli kymmenen vuotta (31), mutta osalla potilaista se voi hiipua jo viiden vuoden kuluessa. Syynä voi olla taudin eteneminen, mutta myös habituaation kehittyminen.
Talamotomia voidaan tehdä sellaisille potilaille, joille syväaivostimulaatiota ei voida tehdä esimerkiksi korkean iän tai pään magneettikuvauslöydösten takia (30). Toimenpide tehdään unilateraalisesti, jolloin tavoitteena on dominantin käden vapinan lievittäminen ja samalla pyritään välttämään dysartriaa. Husissa talamotomioita tehdään 1–2 vuosittain, ja lisäksi niitä tehdään Oysissa ja Tyks aloittanee toimenpiteet lähiaikoina.
Pään magneettikuvien avulla fokusoidulla ultraäänellä voidaan aiheuttaa talamotomia kajoamattomasti. Toimenpide aiheuttaa pysyvän vaurion kohdetumakkeeseen, joten se tehdään yleensä toispuolisena. FDA on hyväksynyt HIFU-hoidon essentiaaliseen vapinaan, Suomessa hoitoa ei ole toistaiseksi saatavilla.
Kuntoutus ja apuvälineet
Potilaan fyysisen aktiivisuuden väheneminen korreloi vanhempaan ikään, tasapainovaikeuksiin ja vapinan vaikeusasteeseen sekä huonompaan kognitioon. Fysioterapiasta on apua tasapainon ja fyysisen toimintakyvyn ylläpitämisessä (32). Toimintaterapeutin arviosta on hyötyä apuvälineiden valinnassa, käden toimintojen harjoittamisessa sekä arjen toimintakyvyn tukemisessa.
Puheterapiaa voidaan tarvita, jos äänen vapina on merkittävää tai esiintyy kielellisiä ongelmia. Keskusteluavulla voidaan käsitellä sairaudesta aiheuttavia häpeän ja hallinnan puutteen tuntemuksen tuomia psyykkisiä ongelmia. Neuropsykologin arvio voi olla tarpeen, jos todetaan merkittäviä kognitiivisia oireita.
Lopuksi
Tutkimuksen mukaan essentiaalista vapinaa sairastavat potilaat kokivat hoidossa puutteita erityisesti tarjotussa psyykkisessä tuessa ja sairauteen liittyvien tuntemuksien käsittelyssä (33). Lisäksi hoidon keskittymistä lääkehoitoihin ilman muiden hoitomuotojen laaja-alaisempia kartoittamista pidettiin ongelmana. Erityisesti fysio- ja toimintaterapeutin kartoitusta ja ohjantaa toivottiin.
Vapinan lisäksi on tärkeää arvioida myös muita kuin motorisia oireita, erityisesti mieliala- ja kognitiivisia oireita. Sairaus aiheuttaa sosiaalista ahdistusta, ja asia on hyvä ottaa puheeksi vastaanoton aikana. Erityistyöntekijöiden arvio ja ohjaus saattavat lisätä merkittävästi potilaan elämänlaatua ja sairauden hallinnan tunnetta.
Rebekka Ortiz: Korvaus käsikirjoituksen kirjoittamisesta ja luentopalkkiot (Suomen Parkinsonliitto).
Jari Honkaniemi: Asiantuntijalausunnot (A-vakuutus, Fennia, FINE vakuutuslautakunta, If, Kaleva, Liikennevakuutuskeskus LähiTapiola, Länsi- ja Sisä-Suomen aluehallintovirasto, OP-Pohjola, Pohjantähti Potilasvakuutuskeskus Tapaturma-asioiden muutoslautakunta, Valtiokonttori, Valvira, Ålands Ömsesidiga Försäkringsbolag), luentopalkkiot (Abbvie, Finva, Orion Pharma), matka-, majoitus- ja kokouskulut (Abbvie, Bayer, Biogen, Boehringer Mannheim, GSK, Orion Pharma, Pfizer, Teva).
Eero Pekkonen: Konsultointipalkkiot ja asiantuntijalausunnot (Abbvie, NordicInfu Care), työsuhde (Potilasvakuutuskeskus), apurahat (TYH-rahoitus), luentopalkkiot (Abbott, Abbvie, NordicInfue Care, Orion), matka-, majoitus- ja kokouskulut (Abbvie, Abbott), Suomen tutkimusvastaava DYSCOVER study (Abbvie), Adroit study (Abbott) (rahoitus laitokselle). Parkinsonin tauti Käypä hoito -työryhmän puheenjohtaja, Kansainvälisen liikehäiriösairauksien yhdistyksen non-motor study -ryhmän jäsen.
- 1
- Louis ED, Gerbin M, Galecki M. Essential tremor 10, 20, 30, 40: clinical snapshots of the disease by decade of duration. Eur J Neurol 2013;20:949–54.
- 2
- Louis ED, Ferreira JJ. How common is the most common adult movement disorder? Update on the worldwide prevalence of essential tremor. Mov Disord 2010;25:534–41.
- 3
- Bhatia KP, Bain P, Bajaj N ym. Consensus statement on the classification of tremors. from the task force on tremor of the International Parkinson and Movement Disorder Society. Mov Disord 2018;33:75–87.
- 4
- Louis ED, Joyce JL, Cosentino S. Mind the gaps: What we don't know about cognitive impairment in essential tremor. Parkinsonism Relat Disord 2019;63:10–9.
- 5
- Shalash AS, Hamid E, Elrassas H ym. Non-motor symptoms in essential tremor, akinetic rigid and tremor-dominant subtypes of Parkinson's disease. PLoS One 2021;1:e0245918.
- 6
- Ondo WG, Sutton L, Dat Vuong K ym. Hearing impairment in essential tremor. Neurology 2003;61:1093–7.
- 7
- Lee SM, Kim M, Lee HM ym. Nonmotor symptoms in essential tremor: Comparison with Parkinson's disease and normal control. J Neurol Sci 2015;349:168–73.
- 8
- Huang H, Yang X, Zhao Q ym. Prevalence and risk factors of depression and anxiety in essential tremor patients: a cross-sectional study in Southwest China. Front Neurol 2019;10:1194.
- 9
- Miller KM, Okun MS, Fernandez HF ym. Depression symptoms in movement disorders: comparing Parkinson's disease, dystonia, and essential tremor. Mov Disord 2007;22:666–72.
- 10
- Smeltere L, Kuznecovs V, Erts R. Depression and social phobia in essential tremor and Parkinson's disease. Brain Behav 2017;9:e00781.
- 11
- Benito-Leon J, Louis ED, Mitchell AJ ym. Elderly-onset essential tremor and mild cognitive impairment: a population-based study (NEDICES). J Alzheimers Dis 2011;23:727–35.
- 12
- Park IS, Oh YS, Lee KS ym. Subtype of mild cognitive impairment in elderly patients with essential tremor. Alzheimer Dis Assoc Disord 2015;29:141–5.
- 13
- Kim JS, Song IU, Shim YS ym. Cognitive impairment in essential tremor without dementia. J Clin Neurol 2009;5:81–4.
- 14
- Azar M, Bertrand E, Louis ED ym. Awareness of cognitive impairment in individuals with essential tremor. J Neurol Sci 2017;377:155–60.
- 15
- Lee S, Chung SJ, Shin HW. Neuropsychiatric symptoms and quality of life in patients with adult-onset idiopathic focal dystonia and essential tremor. Front Neurol 2020;11:1030.
- 16
- Busenbark K, Barnes P, Lyons K ym. Accuracy of reported family histories of essential tremor. Neurology 1996;47:264–5.
- 17
- Louis ED. Essential tremor and the cerebellum. Handb Clin Neurol 2018;155:245–58.
- 18
- Deuschl G. Locus coeruleus dysfunction: a feature of essential or senile tremor? Mov Disord 2012;27:1–2.
- 19
- Kärppä M. Vapinan erotusdiagnostiikka ja hoito. Duodecim 2007;123:161–8.
- 20
- Tan EK, Lee SS, S FC ym. Evidence of increased odds of essential tremor in Parkinson's disease. Mov Disord 2008;23:993–7.
- 21
- Jokela M, Hietala M, Karhu J ym. Särö-X-esimutaatio-oireyhtymä (FXTAS) - magneettikuvauksesta apua diagnosointiin. Duodecim 2019;135:683–6.
- 22
- Suomalaisen Lääkäriseuran Duodecimin ja Suomen Neurologisen yhdistyksen asettama työryhmä. Parkinsonin tauti. Käypä hoito -suositus 10.5.2019. www.kaypahoito.fi
- 23
- Kang JM, Cho YS, Park S ym. Montreal cognitive assessment reflects cognitive reserve. BMC Geriatr 2018;18:261–8.
- 24
- Isaias IU, Marotta G, Hirano S ym. Imaging essential tremor. Mov Disord 2010;25:679–86.
- 25
- Ferreira JJ, Mestre TA, Lyons KE ym. MDS evidence-based review of treatments for essential tremor. Mov Disord 2019;34:950–8.
- 26
- Hedera P, Cibulcik F, Davis TL. Pharmacotherapy of essential tremor. J Cent Nerv Syst Dis 2013;5:43–55.
- 27
- Cleeves L, Findley LJ. Propranolol and propranolol-LA in essential tremor: a double blind comparative study. J Neurol Neurosurg Psychiatry 1988;51:379–84.
- 28
- Linnebank M, Moskau S, Semmler A ym. Antiepileptic drugs interact with folate and vitamin B12 serum levels. Ann Neurol 2011;69:352–9.
- 29
- Pekkonen E. Vapinan hoito – syväaivostimulaatiosta apua vaikeisiin tapauksiin. Duodecim 2016;132:1850–6.
- 30
- Iorio-Morin C, Fomenko A, Kalia SK. Deep-brain stimulation for essential tremor and other tremor syndromes: a narrative review of current targets and clinical outcomes. Brain Sci 2020;12:10.3390/brainsci10120925.
- 31
- Baizabal-Carvallo JF, Alonso-Juarez M. Low-frequency deep brain stimulation for movement disorders. Parkinsonism Relat Disord 2016;31:14–22.
- 32
- Louis ED, Collins K, Rohl B ym. Self-reported physical activity in essential tremor: Relationship with tremor, balance, and cognitive function. J Neurol Sci 2016;366:240–5.
- 33
- Louis ED, Rohl B, Rice C. Defining the treatment gap: what essential tremor patients want that they are not getting. Tremor Other Hyperkinet Mov (N Y) 2015;5:331.
Essential tremor – symptoms, diagnosis and treatment
Essential tremor is a common movement disorder with bilateral upper limb action tremor as leading symptom. Other mild neurological signs, such as slight ataxia or rest tremor, can be seen. The existence of non-motor symptoms, such as depression, anxiety and cognitive problems is common, especially in the advanced stage, affecting quality of life even more than the tremor.
The clinical examination is the basis for diagnosis. Besides neurological examination, the examiner should also evaluate cognition and mood. Imaging studies are not necessary if no atypical signs are present.
Half of the patients benefit from oral medicines. Commonly used medicines are propranolol, primidone, topiramate and gabapentin. Tremor is alleviated by 30–70% on average but side effects often prevent the effective use of medicines. The patient can use two or more medicines to increase efficacy. In addition, physical and occupational therapy and supportive discussions can increase understanding of the disease and quality of life.
Deep brain stimulation (DBS) effectively alleviates severe drug resistant essential tremor. Directional DBS (dDBS) using novel directional electrode technology appears to reduce stimulation related side effects such as dysarthria. Several programming sessions are needed to identify the optimal settings. Thalamotomy and high intensity focused ultrasound (HIFU) can be used when DBS is contraindicated.
Rebekka Ortiz, Jari Honkaniemi, Eero Pekkonen
Rebekka Ortiz
M.D., Ph.D., Specialist in Neurology and General Practice
Neurology Department, Tampere University Hospital