Paikallisestrogeenit ja rintasyöpä
Emättimen paikallisten estrogeenihoitojen ei ole todettu lisäävän rintasyöpäriskiä.
Limakalvojen kuivuminen on yleinen oire vaihdevuosien jälkeen, ja rintasyöpähoidot voivat pahentaa oireita.
Hoitona voidaan aina käyttää hormonittomia kosteuttavia geelejä tai tabletteja. Liukuvoiteen käyttö yhdynnöissä on suositeltavaa.
Rintasyövän hoidon jälkeen voidaan käyttää paikallisia estrogeenejä.
Paikallishoitoa voidaan nykytiedon mukaan harkita myös aromataasinestäjää käyttävillä. Ensisijaisia ovat estriolia sisältävät valmisteet.

Vaihdevuodet alkavat suomalaisilla naisilla keskimäärin 51-vuotiaana (vaihteluväli 45–55 v). Vaihdevuosioireet voivat kuitenkin alkaa jo ennen kuukautisvuotojen loppumista. Tavallisimpia niistä ovat hikoilu, kuumat aallot ja unihäiriöt (1). Merkittävällä osalla naisista esiintyy myös emättimen limakalvojen kuivumista, mielialan vaihteluja ja nivelsärkyjä. Hankalimmiksi oireiksi koetaan usein mielialan lasku, unihäiriöt, kuumat aallot ja hikoilu.
Limakalvojen kuivuminen aiheuttaa emätin- ja virtsatietulehduksia sekä monenlaisia seksuaalihäiriöitä. Näitä ovat kiihottumis- ja kostumishäiriöt, yhdyntäkivut sekä seksuaalisen halun häiriöt. Estrogeenitason pienentyminen onkin yhteydessä useisiin elämänlaatuun oleellisesti vaikuttaviin haittoihin. Vaikka vaihdevuosioireista monet helpottavat muutamissa vuosissa, limakalvo-oireilla on taipumus lisääntyä ja pahentua iän myötä.
Rintasyöpä on naisten yleisin syöpä. Siihen sairastutaan usein vaihdevuosi-iän läheisyydessä tai pian sen jälkeen. Naisen elinaikainen sairastumisriski on länsimaissa yli 10 %. Rintasyöpä onkin vaihdevuosien hormonihoidon aloittajien yleinen huolenaihe.
Pitkäaikaiseen, yli 3–5 vuotta kestävään systeemiseen hormonihoidon käyttöön liittyy suurentunut todennäköisyys sairastua rintasyöpään. Tuoreimmat tutkimukset viittaavat siihen, että riski liittyy erityisesti yhdistelmähoitoon (sekä estrogeeni- että progestiiniosio). Pelkkä estrogeenihoito lisää rintasyöpäriskiä yhdistelmähoitoa vähemmän (2).
Osalle rintasyöpäpotilaista vaihdevuodet tulevat solunsalpaajahoitojen seurauksena ennenaikaisesti. He joutuvat siis kärsimään oireista muita aikaisemmin ja mahdollisesti pitempään. Syövän liitännäishoitona käytetään tätä nykyä usein aiempaa pitkäkestoisempia hormonihoitoja, jotka vähentävät estrogeenivaikutusta. Ne saattavat pahentaa ja pitkittää vaihdevuosioireita. Rintasyövän yleisyyden ja suotuisan ennusteen vuoksi elämänlaatua huonontavista jälkivaivoista kärsivien joukko on huomattava (3).
Emättimen limakalvo ja estrogeeni
Normaalin, toimivan limakalvon edellytykset ovat ehjä epiteelisolukko ja oikeanlainen mikrobifloora. Fertiili-ikäisen naisen emättimen limakalvo on terve, kostea ja paksu sekä emättimen epiteeli poimuinen. Estrogeeni auttaa säilyttämään paksun glykogeenirikkaan pintakerroksen, jossa laktobasillit viihtyvät. Ne pitävät pH:n happamana.
Estrogeenireseptoreita on emättimen, virtsaputken ja virtsarakon trigonumin limakalvolla. Menopaussin jälkeen estrogeenin puutos aiheuttaa glykogeenirikkaan pintakerroksen solujen häviämisen ja korvautumisen intermediaali- ja parabasaalikerroksen soluilla. Laktobasillit vähenevät, ja emättimen elastisuus ja kosteus häviävät. Tästä seuraa kipua ja kuivuutta sekä verenkierron vähenemistä. Emättimen pH suurenee.
Vagina-atrofian oireet ja löydökset
Vagina-atrofian oireista kärsii puolet 50–60-vuotiaista naisista, ja yli 70-vuotiailla prevalenssi on jo yli 70 %. Oireet alkavat monesti vasta vuosia kuukautisten poisjäännin jälkeen (n. 4–10 vuotta). Tavallisimpia oireita ovat kuivuus, polttelu ja kutina. Monella ovat haittana myös yhdyntäkivut ja virtsarakon toimintahäiriöt, kuten pakkovirtsankarkailu ja tiheävirtsaisuus. Herkkyys virtsatie- ja emätintulehduksille lisääntyvät (4).
Vulvovaginaalinen atrofia (genitourinary syndrome of menopause, GSM) määritellään tilaksi, jossa emättimen limakalvo ohenee ja sen verenkierto vähenee. Tämän seurauksena limakalvon poimuisuus vähenee, emättimen pituus lyhenee ja forniksit häviävät (kohdunsuu madaltuu). Myös ulkosynnyttimissä tapahtuu muutoksia, kun häpyhuulet kutistuvat (taulukko 1).
Rintasyövän sairastaneet kärsivät näistä oireista yhtä lailla – tai jopa enemmän (5). Heistä moni saa leikkaushoidon jälkeen sädehoidon lisäksi solusalpaajahoidon sekä liitännäishoidoksi pitkäaikaisia hormonihoitoja, jotka voivat osaltaan voimistaa limakalvo-oireita.
Seniili (atrofinen) vaginiitti aiheutuu estrogeenin puutteesta emättimen limakalvoilla ja samanaikaisesta tulehduksellisesta prosessista. Papa-näytteessä voidaan tällöin nähdä parabasaalisolujen ja intermediaalisten solujen lisääntymisen lisäksi sekafloora sekä runsaasti leukosyyttejä.
Vagina-atrofian hoito
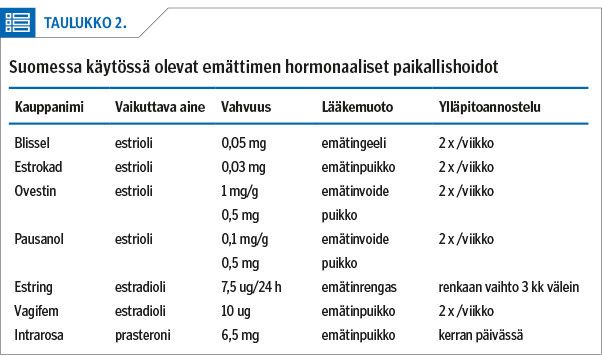
Atrofisen limakalvon hoitoon on monia vaihtoehtoja (6), sekä kosteuttavia hormonittomia valmisteita että hormonivalmisteita. Suomessa on markkinoilla estradiolia ja estriolia sisältäviä paikallishoitotuotteita (taulukko 2). Kaikki valmisteet on todettu tehokkaiksi ja turvallisiksi.
Limakalvo-oireista kärsivistä naisista 80–90 % saa merkittävän avun paikallisestrogeenin käytöstä. Lumekontrolloiduissa tutkimuksissa estrogeeni on todettu limakalvovaivojen hoidossa merkitsevästi paremmaksi kuin hormonittomat vaihtoehdot tai lumelääke (7). Emättimen oireiden helpottamisen lisäksi estrogeenia sisältävä paikallishoito vähentää genitaalialueen ärsytysoireita. Se saattaa vähentää virtsatieinfektioita ja pakkoinkontinenssia sekä etenkin öisiä virtsauskertoja (8).
Estradioli voidaan annostella joko emätintabletteina tai -renkaana. Estriolia on saatavilla emätinpuikkoina, geelinä tai -voiteena. On hyvä muistaa, että valmisteen sidosaineella ja valmistemuodolla on myös merkitystä.
Hoidon alussa tai emättimen ollessa voimakkaan atrofinen, hoitoannos annostellaan emättimeen joka ilta kahden viikon ajan. Tämän jälkeen hoito toteutetaan ns. ylläpitoannoksella, tyypillisesti kahdesti viikossa. Emätinrengas erittää estrogeenia kolmen kuukauden ajan ja on kätevä pitkäaikaishoidossa. Tuoreeseen katsaukseen on kerätty tiedot tutkimuksista, joissa on vertailtu vaginaalista estrogeenia lumelääkkeeseen tai ei-hormonaalisiin valmisteisiin. Tutkimustiedon perusteella kaikki estrogeenivalmisteet hoitavat kaikilla käytetyillä annoksilla tehokkaasti limakalvo-oireita; tehossa tai haittavaikutuksissa ei näytä olevan eroa (9).
Estrogeenia sisältävien paikallishoitovalmisteiden viralliset vasta-aiheet ovat todettu hormoniriippuvainen syöpä (erityisesti rintasyöpä ja aromataasinestäjän käyttö), allergia jollekin valmisteen komponentille sekä selvittämätön genitaaliverenvuoto. Vaginaalisen estrogeenin turvallisuudesta rintasyöpäpotilailla on kuitenkin vähän laadukkaita tutkimuksia. Päätelmät on tehty lyhytaikaisiin (alle viikon) estradiolitasojen muutoksiin vedoten erittäin pienillä, jopa alle 10 henkilön potilasmäärillä (10).
Rintasyövän hoitojen vaikutukset emättimen limakalvoihin
Solunsalpaajat saattavat aiheuttaa munasarjatoiminnan hiipumisen ja estrogeenivajauksen, mikä onkin rintasyöpähoitojen tavoite. Tähän liittyen kuukautiset jäävät pois ainakin tilapäisesti ja vaihdevuosi-ikä varhaistuu. Liitännäislääkehoidot vaikuttavat kuukautisrytmiin, heikentävät hedelmällisyyttä ja vaikuttavat gynekologiseen terveyteen muillakin tavoin. Premenopausaalisille naisille voidaan käyttää liitännäishoitoina SERM-valmisteita ja GnRH-analogeja, postmenopausaalisille aromataasinestäjiä ja fulvestranttia.
Tamoksifeeni on selektiivinen estrogeenireseptorin muuntelija (SERM), jolla on antagonistinen vaikutus rintakudoksessa. Postmenopausaalisella naisella se toimii kohdussa ja emättimessä heikkona estrogeeniagonistina. Aromataasinestäjälääkitys estää estrogeenin muodostusta androgeeneista munasarjojen ulkopuolella. Aromataasin toiminta voi estyä lähes kokonaan.
Sekä SERM-valmisteet (tamoksifeeni, toremifeeni) että aromataasinestäjät (anastrotsoli, letrotsoli ja eksemestaani) aiheuttavat haittavaikutuksina kuumia aaltoja, hikoilua, mielialamuutoksia ja limakalvo-oireita (11). GnRH-analogit aiheuttavat käytännössä aina sekä amenorrean että estrogeenivajaukseen liittyviä vaihdevuosioireita (3).
Hormonireseptoripositiivisten rintasyöpien liitännäishoitojen käyttö on viime vuosina yleistynyt, ja hoito voi jatkua kymmenenkin vuotta. Pitkittyneeseen aromataasinestäjälääkityksen käyttöön liittyy atrofisen vaginiitin oireita, ja tämä vaikuttaa potilaan elämänlaatuun (12). Hankalat haittavaikutukset voivat johtaa jopa hoidon keskeyttämiseen (13). Estrogeeniagonistivaikutuksensa vuoksi tamoksifeeni kuivattaa yleensä limakalvoja postmenopausaalisilla naisilla vähemmän kuin aromataasinestäjä.
Hormonien imeytyminen emättimen paikallishoidossa
Estradioli
Vaginaalisen estradiolihoidon alussa estradiolipitoisuus suurentuu, vaikkakin pysyy postmenopausaalisella matalalla tasolla (14). Imeytyminen on annosriippuvaista; pienellä annoksella (7,5 µg:n emätinrengas tai 10 µg:n emätintabletti) estradiolitasot suurentuvat, mutta eivät ylitä tavanomaista postmenopausaalista tasoa ≤ 20 pg/ml (15). Limakalvon kunnon parantuessa imeytyminen vähenee, ja hoidon jatkuessa pitoisuudet pienentyvät takaisin lähtötasolle.
Onko vaginaalisella estradiolilla systeemivaikutuksia? Suomalaisessa rekisteritutkimuksessa selvitettiin, vaikuttaako vaginaalinen estrogeenihoito kuolleisuuteen sydän- ja verisuonitauteihin (16). Tutkimukseen otettiin mukaan ne lähes 200 000 naista, jotka aloittivat hoidon vuosien 1994–2009 aikana. Vertailu tehtiin ikävakioituun taustaväestöön. Tutkimus osoitti, että vaginaalisen estrogeenin käyttäjien kuolleisuus oli pienempi (standardized mortality ratio, SMR = 0,64; 95 %:n LV 0,57–0,72). Tutkijat pohtivat, että tämä hyöty voi johtua valikoitumisesta (valmistetta ovat käyttäneet terveemmät naiset), mutta myös minimaalisella estrogeenin imeytymisellä voi olla merkitystä.
Estrioli
Estrioli on estradiolia heikompi estrogeeni, eikä se metaboloidu estradioliksi (17). Sen systeeminen imeytyminen on vähäisempää kuin estradiolilla ja metabolinen poistuma nopeampaa. Sillä on vähäisempi affiniteetti plasman proteiineihin. Toistaiseksi ei ole tutkimustietoa siitä, onko estrioli estradiolia turvallisempi vaihtoehto rintasyöpäpotilaille.
Prasteroni
Vaginaalinen dehydroepiandrosteroni (DHEA) eli prasteroni on testosteronin ja estradiolin esiaste, joten se vaikuttaa emättimen limakalvon estrogeeni- ja androgeenireseptorien kautta. Estrogeeni- ja testosteronitasot voivat verenkierrossa hieman kasvaa, mutta pysyvät matalalla postmenopausaalisella tasolla. 6,5 mg prasteronia emätinpuikkona päivittäin on tutkimusten mukaan yhtä tehokas kuin 0,3 mg suun kautta annosteltavaa konjugoitua estrogeenia (oral conjugated equine estrogens, CEE) tai 10 µg emättimeen annosteltavaa etinyyliestradiolia (18). Toistaiseksi ei ole tutkimustietoa prasteronin käytöstä rintasyövän sairastaneilla.
Paikallishoidot ja rintasyövän riski
Systeemisen hormonikorvaushoidon lisäksi myös paikallishoitoa pelätään rintasyöpäriskin vuoksi, vaikka paikallishoito suurentaa veren estrogeenipitoisuuksia vain vähän ja ohimenevästi (19).
Suomalaisessa yli 100 000 vaihdevuosien estrogeenihoitoa käyttävän naisen seurantatutkimuksessa oli noin 18 000 naista, jotka käyttivät estrogeenia vain emättimen kautta. Paikallishoidon ei todettu lisäävän rintasyöpään sairastumisen riskiä (20). Laajassa WHI-seurantatutkimuksessa oli mukana 45 663 iältään 50–79 vuotiasta naista, joilla ei ollut käytössä systeemistä hormonihoitoa. Heitä seurattiin 7 vuoden ajan. Naisista 4 100 käytti vaginaalista estrogeenia. Seurannan päätetapahtumia olivat mm. syövät ja sepelvaltimotauti. Tutkimuksessa ei todettu minkäänlaista viitettä rintasyövän lisääntymisestä paikallishoidon käyttäjillä (21).
Entä mitä sanoo julkaistu tieto aromataasinestäjien käytöstä ja paikallisestrogeenista? Aromataasinestäjähoidon aikana estradiolitasot supressoituvat erittäin pieniksi. Jos samanaikaisesti käytetään paikallista estradiolihoitoa, voidaan todeta ainakin ohimenevää estrogeenipitoisuuksien kasvua (22).
Sen sijaan tuoreen ruotsalaisen tutkimuksen mukaan estrioligeeli hyvin pienellä annoksella ei kasvata seerumin estrogeenitasoja tai aiheuta FSH-tason muutoksia aromataasinestäjän käyttäjillä (23). Hiljattain ilmestyneessä systemaattisessa katsauksessa analysoitiin aromataasinestäjän käyttäjien estrogeenitasoja paikallisen estrogeenihoidon aikana (24): tasojen kasvua ei todettu, kun mittaukset tehtiin 2, 4, 8 tai 12 viikon kuluttua estrogeenihoidon aloituksesta.
Paikallisen estrogeenihoidon käytön vaikutusta rintasyövän uusimisriskiin aromataasinestäjälääkityksen aikana ei juuri ole tutkittu.Le Rayn tutkimuksessa seurattiin 13 479 naista, jotka saivat rintasyöpähoidon jälkeen liitännäishoitoa (25). Heistä 2 673 sai jotakin aromataasinestäjää, 10 806 sai tamoksifeenia. Naisista 271 käytti samanaikaisesti paikallista estrogeenia, keskimäärin 3,5 vuoden seuranta-ajan.
Tutkimuksen johtopäätös oli, että paikallisestrogeenin käyttö ei yhteiskäytössä aromataasinestäjän tai tamoksifeenin kanssa lisännyt riskiä rintasyövän uusiutumiseen, verrattuna niiden naisten riskiin, jotka eivät paikallishoitoa käyttäneet (RR 0,78, 95 %:n LV 0,48–1,25). Tutkimuksessa oli kuitenkin mukana vain verrattain vähän aromataasinestäjän käyttäjiä.
Tuoreen yhdysvaltalaisen kyselytutkimuksen mukaan rintasyöpäpotilaita hoitavat lääkärit kokivat turvalliseksi kirjoittaa paikallisestrogeenejä naisille, joilla oli todettu estrogeenireseptorinegatiivinen rintasyöpä, mutta estrogeenireseptoripositiivisessa rintasyövässä suhtautuminen vaihteli (26). Yllättäen paikallishoitoa suositeltiin useammin aromataasinestäjiä käyttäville kuin tamoksifeenia käyttäville.
Estrogeenihoidon vaihtoehdot
Objektiivisen mikroskooppitutkimuksen perusteella limakalvon paksuneminen ja sen ns. maturaatioindeksin paraneminen (epiteelin kypsyneiden pintasolujen lisääntyminen) saadaan aikaan ainoastaan paikallisilla estrogeenivalmisteilla. Tutkimuksissa hormonittomilla valmisteilla (kosteuttavat valmisteet ja liukasteet) on kuitenkin saatu helpotusta limakalvo-oireisiin.
Kosteuttavat valmisteet
Kosteuttavien valmisteiden tarkoituksena on ylläpitää emättimen normaalia pH-arvoa ja kosteuttaa limakalvoja. Valmisteita tulisi käyttää useita kertoja viikossa 2–3 päivän välein. Hyaluronihappoa sisältävät valmisteet turvottavat limakalvoa. Lievissä atrofiaoireissa kosteuttavilla valmisteilla voidaan saada helpotusta oireisiin. Niitä voidaan käyttää myös muiden valmisteiden ohella. Tyrniöljyllä on tutkimusten mukaan positiivista vaikutusta limakalvo-oireiden hoidossa, joskaan se ei paranna limakalvon objektiivisesti arvioitua maturaatioindeksiä, kuten eivät muutkaan hormonittomat valmisteet (27).
Liukasteet
Liukasteet on luokiteltu joko kemikaaleiksi tai lääkinnällisiksi apuaineiksi. Niitä on helppo hankkia kaupoista ja apteekeista, ja ne ovat usein edullisia hinnaltaan. Vesipohjaiset liukasteet lähtevät iholta sekä limakalvoilta helposti vesipesussa ja sopivat herkällekin iholle. Silikonipohjaiset liukuvoiteet sisältävät yhdisteitä, joilla on öljyn kaltaisia ominaisuuksia. Silikonipohjaiset tuotteet kestävät käytössä paremmin, mutta niiden poistaminen voi vaatia pesua saippualla. Niillä on myös enemmän haittavaikutuksia kuin vesipohjaisilla liukasteilla.
Öljypohjaiset liukuvoiteet kuluvat pois nopeimmin, eivätkä ne sovellu käytettäväksi kondomin kanssa. Lisäksi niillä on epäilty olevan yhteyttä emätintulehduksiin, mutta tästä ei ole tarkkaa tietoa.
Lopuksi
Olemassa olevan tutkimustiedon perusteella useimmat rintasyövän sairastaneet naiset voivat syöpähoitojen päätyttyä käyttää paikallista estrogeenihoitoa. Nykyisten suositusten mukaan sitä voivat käyttää tarvittaessa myös tamoksifeenin käyttäjät.
Vaikka paikallisestrogeenia ei yleensä suositella aromataasinestäjiä käyttäville naisille, sitä on kuitenkin syytä harkita, jos oireet eivät hormonittomilla valmisteilla helpota. Ensisijainen valmiste siinä tapauksessa on estrioli, ja hoito kannattaa aloittaa pieniannoksisilla valmisteilla. Tuoreen meta-analyysin mukaan aromataasinestäjän käytön aikana aloitettu paikallinen estrogeenihoito (estradioli tai estrioli) ei näyttäisi aiheuttavan estrogeenitasojen suurentumista verenkierrossa (24).
Käynnissä on useita tutkimuksia paikallishoidosta pieniannoksisella estriolilla, estradiolilla tai testosteronilla aromataasinestäjiä käyttävillä naisilla (17,23,28,29). Näissäkin tutkimuksissa turvallisuusmittarina on pääsääntöisesti valmisteen imeytyminen ja metaboloituminen elimistössä. Rintasyövän uusiutumisen riskin tutkiminen vaatisi oikein tehdyissä tutkimusasetelmissa niin isoja potilasmääriä, että sellaisen toteuttaminen lienee tulevaisuudessakin varsin epätodennäköistä.
Artikkelia on päivitetty 5.2.2020. Taulukossa 2 ollut virhe on korjattu sähköiseen versioon.
Katja Kero: Luentopalkkio (Suomen Gynekologiyhdistys).
Aila Tiitinen: Ei sidonnaisuuksia.
- 1
- Savolainen-Peltonen H, Mikkola T. Vaihdevuosien hormonihoidon vaikutukset Suom Lääkäril 2018;73:143–145.
- 2
- Stuenkel CA, Davis SR, Gompel A ym. Treatment of Symptoms of the Menopause: An Endocrine Society Clinical Practice Guideline. J Clin Endocrinol Metab 2015;100:3975–4011.
- 3
- Leidenius M, Tasmuth T, Jahkola T ym. Rintasyövän hoidon aiheuttama pitkäaikainen sairastavuus. Duodecim 2010;126:1217–25.
- 4
- Gandhi J, Chen A, Dagur G ym. Genitourinary syndrome of menopause: an overview of clinical manifestations, pathophysiology, etiology, evaluation, and management. Obstet Gynecol 2016;215:704–711.
- 5
- Biglia N, Cozzarella M, Cacciari F ym. Menopause after breast cancer: a survey on breast cancer survivors. Maturitas 2003;45:29–38.
- 6
- Polo P, Auranen A. Vaihdevuosien hormonihoidon räätälöinti. Suom Lääkäril 2015;70:3363–3368.
- 7
- Lethaby A, Ayeleke RO, Roberts H. Local oestrogen for vaginal atrophy in postmenopausal women. Cochrane Database of Systematic Reviews 2016, Issue 8. Art. No.: CD001500. DOI: 10.1002/14651858.CD001500.pub3.
- 8
- Cody JD, Jacobs ML, Richardson K, Moehrer B, Hextall A. Oestrogen therapy for urinary incontinence in post–menopausal women. Cochrane Database Syst Rev 2012;10:CD001405.
- 9
- Biehl C, Plotsker O, Mirkin S. A systematic review of the efficacy and safety of vaginal estrogen products for the treatment of genitourinary syndrome of menopause. Menopause 2019;26:431–453.
- 10
- Kendall A. Dowsett M, Folkerd E, Smith I. Caution: Vaginal estradiol appears to be contraindicated in postmenopausal women on adjuvant aromatase inhibitors. Ann Oncol 2006;17:584–587.
- 11
- Sailas L, Leinonen P. Rintasyöpäpotilaan seuranta terveyskeskuksessa. Suom Lääkäril 2012;67:1900–1903.
- 12
- Ganz PA, Rowland JH, Desmond K, Meyerowitz BE, Wyatt GE. Life after breast cancer: understanding women’s health-related quality of life and sexual functioning. J Clin Oncol 1998;16:501–514.
- 13
- Cella D, Fallowfield LJ. Recognition and management of treatment-related side effects for breast cancer patients receiving adjuvant endocrine therapy. Breast Cancer Res Treat 2008;107:167–180.
- 14
- Labrie F, Cusan L, Gomez JL ym. Effect of one-week treatment with vaginal estrogen preparations on serum estrogen levels in postmenopausal women. Menopause 2009;16:30–6.
- 15
- Santen RJ. Vaginal administration of estradiol: effects of dose, preparation and timing on plasma estradiol levels. Climacteric 2015;18:121–34.
- 16
- Mikkola TS, Tuomikoski P, Lyytinen H ym. Vaginal estradiol use and the risk for cardiovascular mortality. Hum Reprod 2016;31:804–9.
- 17
- Donders G, Neven P, Moegele M ym. Ultra-low-dose estriol and Lactobacillus acidophilus vaginal tablets (Gynoflor(®)) for vaginal atrophy in postmenopausal breast cancer patients on aromatase inhibitors: pharmacokinetic, safety, and efficacy phase I clinical study. Breast Cancer Res Treat 2014;145:371–9.
- 18
- Labrie F, Archer DF, Koltun W ym; VVA Prasterone Research Group. Efficacy of intravaginal dehydroepiandrosterone (DHEA) on moderate to severe dyspareunia and vaginal dryness, symptoms of vulvovaginal atrophy, and of the genitourinary syndrome of menopause. Menopause 2016;23:243–56.
- 19
- Nilsson K, Heimer G. Low-dose oestradiol in the treatment of urogenital oestrogen deficiency - a pharmacokinetic and pharmacodynamic study. Maturitas 1992;15:121–7.
- 20
- Lyytinen H, Pukkala E, Ylikorkala O. Breast cancer risk in postmenopausal women using estrogen-only therapy. Obstet Gynecol 2006;108:1354–60.
- 21
- Crandall CJ, Hovey KM, Andrews CA ym. Breast cancer, endometrial cancer, and cardiovascular events in participants who used vaginal estrogen in the Women’s Health Initiative Observational Study. Menopause 2018;25:11–20.
- 22
- Wills S, Ravipati A, Venuturumilli P ym. Effects of vaginal estrogens on serum estradiol levels in postmenopausal breast cancer survivors and women at risk of breast cancer taking an aromatase inhibitor or a selective estrogen receptor modulator. J Oncol Pract 2012;8:144–148.
- 23
- Sánchez-Rovira P, Lindén Hirschberg A, Gil M, Antolín-Novoa S. 0.005% estriol vaginal gel in hormone receptor-positive postmenopausal women with early stage breast cancer in treatment with aromatase inhibitors (AIs) in the adjuvant setting. A phase II prospective, randomized, double-blind placebo-controlled study - “the Blissafe study” Cancer Research 2018, 78 (Suppl 4):P3-12-01.
- 24
- Pavlović R, Janković SM, Milovanović JR ym. The safety of local hormonal treatment for vulvovaginal atrophy in women with estrogen receptor-positive breast cancer who are on adjuvant aromatase inhibitor therapy: Meta-analysis. Clin Breast Cancer 21.8.2019. doi: 10.1016/j.clbc.2019.07.007
- 25
- Le Ray I ym, Local estrogen therapy and risk of breast cancer recurrence among hormone-treated patients: a nested case–control study. Breast Cancer Res Treat 2012;135:603–609.
- 26
- Richter LA, Han J, Bradley S ym. Topical estrogen prescribing patterns for urogenital atrophy among women with breast cancer: results of a national provider survey. Menopause 2019;26:714–719.
- 27
- Larmo PS, Yang B, Hyssälä J, Kallio HP, Erkkola R. Effects of sea buckthorn oil intake on vaginal atrophy in postmenopausal women: a randomized, double-blind, placebo-controlled study. Maturitas 2014;79:316–21.
- 28
- Sulaica E, Han T, Wang W, Bhat R, Trivedi MV, Niravath P. Vaginal estrogen products in hormone receptor-positive breast cancer patients on aromatase inhibitor therapy. Breast Cancer Res Treat 2016;157:203–210.
- 29
- Melisko ME, Goldman ME, Hwang J ym. Vaginal Testosterone Cream vs Estradiol Vaginal Ring for Vaginal Dryness or Decreased Libido in Women Receiving Aromatase Inhibitors for Early-Stage Breast Cancer: A Randomized Clinical Trial. JAMA Oncol 2017;3:313–319.
Topical estrogens and breast cancer
The risk of breast cancer is not elevated among postmenopausal women using vaginal estrogens. Vaginal atrophy presents with dryness and dyspareunia, and affects patients’ quality of life. Endocrine adjuvant therapies, especially aromatase inhibitors, can even increase the prevalence of these symptoms. Use of non-hormonal treatments such as vaginal lubricants and moisturizers is preferred as first-line treatment. If hormonal vaginal treatment is needed, a low-dose estriol product appears to be effective and safe.