Aikuisiällä alkaneen Huntingtonin taudin lääkehoito Suomessa
Lähtökohdat Huntingtonin taudin lääkehoidosta ei ole yksiselitteisiä suosituksia. Tutkimme keskushermostoon vaikuttavilla lääkkeillä toteutettua taudin oireenmukaista hoitoa Suomessa.
Menetelmät Kansallisista rekistereistä tunnistettiin vuosina 1987–2010 hoidetut potilaat. Lääkitykset selvitettiin sairauskertomuksista.
Tulokset Liikehäiriöitä hoidettiin ensisijaisesti neurolepteillä, yleisimmin haloperidolilla, joskin sen suhteellinen osuus pieneni. Tetrabenatsiinia käytettiin vähän, harvemmin kuin klonatsepaamia. Rauhoittavia lääkkeitä oli määrätty monille. Unen rakennetta häiritsemättömien unilääkkeiden käyttö sen sijaan oli vähäistä.
Hermostoon vaikuttavia lääkkeitä käyttävien potilaiden osuus kasvoi taudin edetessä. Miesten ja naisten tai nuorten ja vanhojen potilaiden välillä ei havaittu eroja.
Päätelmät Huntingtonin taudin motoristen oireiden hoito Suomessa ei eronnut kansainvälisestä käytännöstä. Unihäiriöiden ja mielialaoireiden lääkehoidossa on vielä kehitettävää.
Huntingtonin tauti (HD) on vallitsevasti periytyvä hermoston rappeumasairaus. Klassisia oireita ja löydöksiä ovat motoriikan, kognition sekä psyyken häiriöt. Niistä keskeisimpiä ovat korea, tasapaino- ja kävelyhäiriö, ajattelun jäykkyys ja hidastuminen, apatia, masennus, ahdistus sekä ärtyvyys. Lisäksi tautiin liittyy unihäiriöitä, painon laskua ja autonomisen hermoston toiminnan häiriöitä. Oireiden ilmeneminen vaihtelee potilaittain.
Diagnoosin asettamisen ehdoton edellytys on, että motoriset oireet ovat yksiselitteisesti todettavissa (1,2). Diagnostisissa selvittelyissä voi hyödyntää aivojen magneettikuvantamista: oireisella potilaalla on usein todettavissa häntätumakkeiden surkastuma. Diagnoosi on suositeltavaa vahvistaa HTT-geenin sytosiini–adeniini–guaniini -toistojakson pituuden määrittävällä testillä.
Taudinkulkuun vaikuttavaa hoitoa ei ole käytettävissä, vaan hoito on oireenmukaista lääkehoitoa ja yksilöllisesti kohdennettua kuntoutusta. Korean ensisijaisena lääkehoitona on käytetty tetrabenatsiinia tai neuroleptejä (3,4). Psykiatristen oireiden hoitoon taas on käytetty ensisijaisesti mielialalääkkeitä, erityisesti serotoniinin takaisinoton estäjiä (SSRI) ja tarvittaessa myös neuroleptejä (4,5,6) sekä mielialan tasaajia (5,6). Kognitiivisiin oireisiin tutkitusti tehoavaa lääkehoitoa ei ole (5,8).
Huntingtonin tauti on Suomessa harvinaisempi kuin muissa valkoihoisissa väestöissä (7), eikä lääkehoidon suomalaisista käytännöistä ole saatavilla aiempaa tutkimustietoa. Käypä hoito -suositusta ei ole, kuten ei myöskään suomenkielistä oppikirjatietoa lääkehoidon linjoista. Hoitavat lääkärit ovatkin joutuneet tekemään valinnat ulkomaisen tiedon, kliinisen kokemuksen tai kliinisen perimätiedon pohjalta. Kansainvälisestikään taudin oireenmukaisesta lääkehoidosta ei ole yksiselitteisiä suosituksia (4,8,9).
Tämän rekisteritutkimuksen tavoitteena oli selvittää, miten Huntingtonin taudin lääkehoito on toteutettu Suomessa 1980-luvulta 2010-luvulle ja miten hoitokäytännöt mahdollisesti muuttuivat ajanjaksolla.
Aineisto ja menetelmät
Tutkimukseen valittiin mukaan potilaat, joiden poistodiagnoosikoodi hoitoilmoitusrekisterissä oli 3334A (1.1.1987–31.12.1995) tai G10 (1.1.1996–31.12.2010). Lisäksi tutkittiin Väestöliitolta saadut tiedot perinnöllisyysneuvontaa saaneista Huntingtonin tautia sairastavista potilaista ja HUSLABilta ja Turun yliopiston lääketieteellisen biokemian ja genetiikan DNA-laboratoriolta saadut tiedot positiivisista geenitutkimuksista. Diagnoosit varmennettiin sairauskertomuksista, joista myös selvitettiin potilaiden kliininen kuva ja lääkitys taudin diagnoosivaiheessa sekä viiden vuoden kuluttua diagnoosista.
Aineisto kerättiin vuosina 2012–2013, ja suurimmalta osalta potilaista tietoja oli käytettävissä näihin vuosiin saakka. Tutkimuksessa keskityttiin niihin hermostoon vaikuttaviin lääkkeisiin, joita liikehäiriösairauksien oireenmukaisessa hoidossa yleensä käytetään (ATC-koodit N03–N07). Lääkitykseksi merkittiin se lääkeyhdistelmä, joka potilaalla oli käytössä kunkin vastaanoton tai sairaalahoitojakson jälkeen.
Vain yhdellä potilaalla oli nuoruusiän taudinmuoto. Hänellä ei ollut lääkityksiä diagnoosivaiheessa, eikä hänen lääkitystietojaan ollut saatavilla viiden vuoden kuluttua diagnoosista. Hänet jätettiin pois tutkimuksesta.
Tutkimus sai Varsinais-Suomen sairaanhoitopiirin eettisen toimikunnan puoltavan lausunnon (Dnro ETMK 19/180/2010) ja THL:n valtakunnallisen tutkimusluvan (Dnro THL/1456/5.05.00/2010).
Muuttujien jakaumaa arvioitiin Shapiro-Wilkin ja Kolmogorov-Smirnovin testeillä, ja tulosten perusteella käytettiin joko Studentin t-testiä tai Mann-Whitneyn U-testiä tilastollisten erojen havaitsemiseksi. Sukupuoli- ja ikäryhmäeroja tutkittaessa tiedot ristiintaulukoitiin ja arvioitiin χ2-testillä. P-arvoja alle 0,05 pidettiin tilastollisesti merkitsevinä. Analyyseissä käytettiin IBM SPSS Statistics -ohjelmaa.
Tulokset
Lääkitys diagnoosivaiheessa
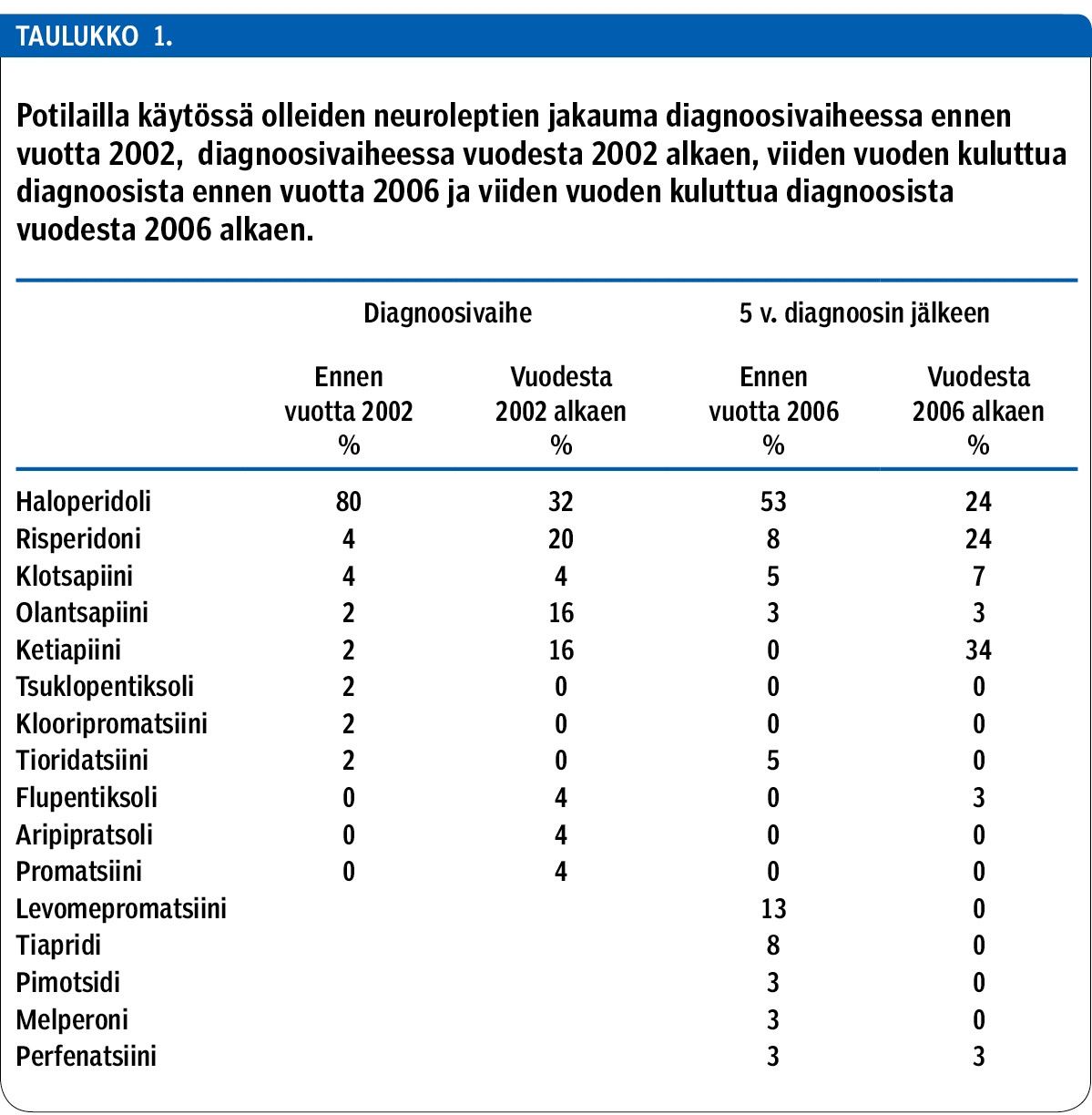
Tutkimuskohorttiin kuului 206 potilasta, joista 176:n (85,4 %) diagnoosivaiheen lääkitystiedot olivat käytettävissä (keski-ikä 53,8 ± 11,8 vuotta, naisia 51 %). Diagnoosivaiheessa 73 potilasta (42 %, 95 %:n luottamusväli 34–49 %) oli ilman lääkitystä (ATC-koodit N03–N07). Neuroleptilääkitys oli käytössä 68 potilaalla (39 %, 95 %:n LV = 31–46 %). Yleisimmin käytetyt neuroleptit olivat haloperidoli, risperidoni ja ketiapiini (taulukko 1). Neuroleptien käytön yleisyydessä ei ollut eroa miesten ja naisten välillä (p-arvo = 0,60) eikä yli ja alle 55-vuotiaiden välillä (p-arvo = 0,41). Vain yhdellä potilaalla oli käytössä korean hoitoon rekisteröity tetrabenatsiini.
Antidepressantti (N06) oli käytössä 34 potilaalla (19 %, 95 %:n LV = 13–25 %), joista kahdella monoamiini-inhibiittori ja muilla SSRI- tai SNRI-lääke. Anksiolyytti (N05B), sedatiivi (N05C) tai klonatsepaami oli käytössä 46 potilaalla (26 %, 95 %:n LV = 20–33 %) ja lyhytvaikutteinen bentsodiatsepiinijohdos (N05CF) 10 potilaalla.
Lääkitys viiden vuoden kuluttua diagnoosista
Käytettävissä oli 81 potilaan (69,8 %) lääkitystiedot viiden vuoden kuluttua diagnoosista (keski-ikä 57,7 ± 10,1 vuotta, naisia 52 %). Vain kahdeksan potilasta (10 %, 95 %:n luottamusväli 3–16 %) oli täysin lääkitsemättömiä (ATC-koodit N03–N07), kun taas neuroleptejä käyttävien potilaiden osuus oli kaksinkertainen (n = 61, 75 %, 95 %:n luottamusväli 66–85 %) verrattuna diagnoosihetkeen. Yleisimmin käytetyt neuroleptit olivat yhä haloperidoli, risperidoni ja ketiapiini (taulukko 1). Neuroleptien käytön yleisyydessä ei ollut eroa miesten ja naisten välillä (p-arvo = 0,14) eikä yli ja alle 59-vuotiaiden välillä (p-arvo = 0,75). Kaksi potilasta käytti tetrabenatsiinia.
Antidepressantti oli käytössä 29 potilaalla (36 %, 95 %:n LV = 25–46 %), joista viittä hoidettiin monoamiini-inhibiittoreilla. Anksiolyytti, sedatiivi tai klonatsepaami oli käytössä 41 potilaalla (51 %, 95 %:n LV = 40–62 %) ja lyhytvaikutteinen bentsodiatsepiinijohdos kuudella potilaalla.
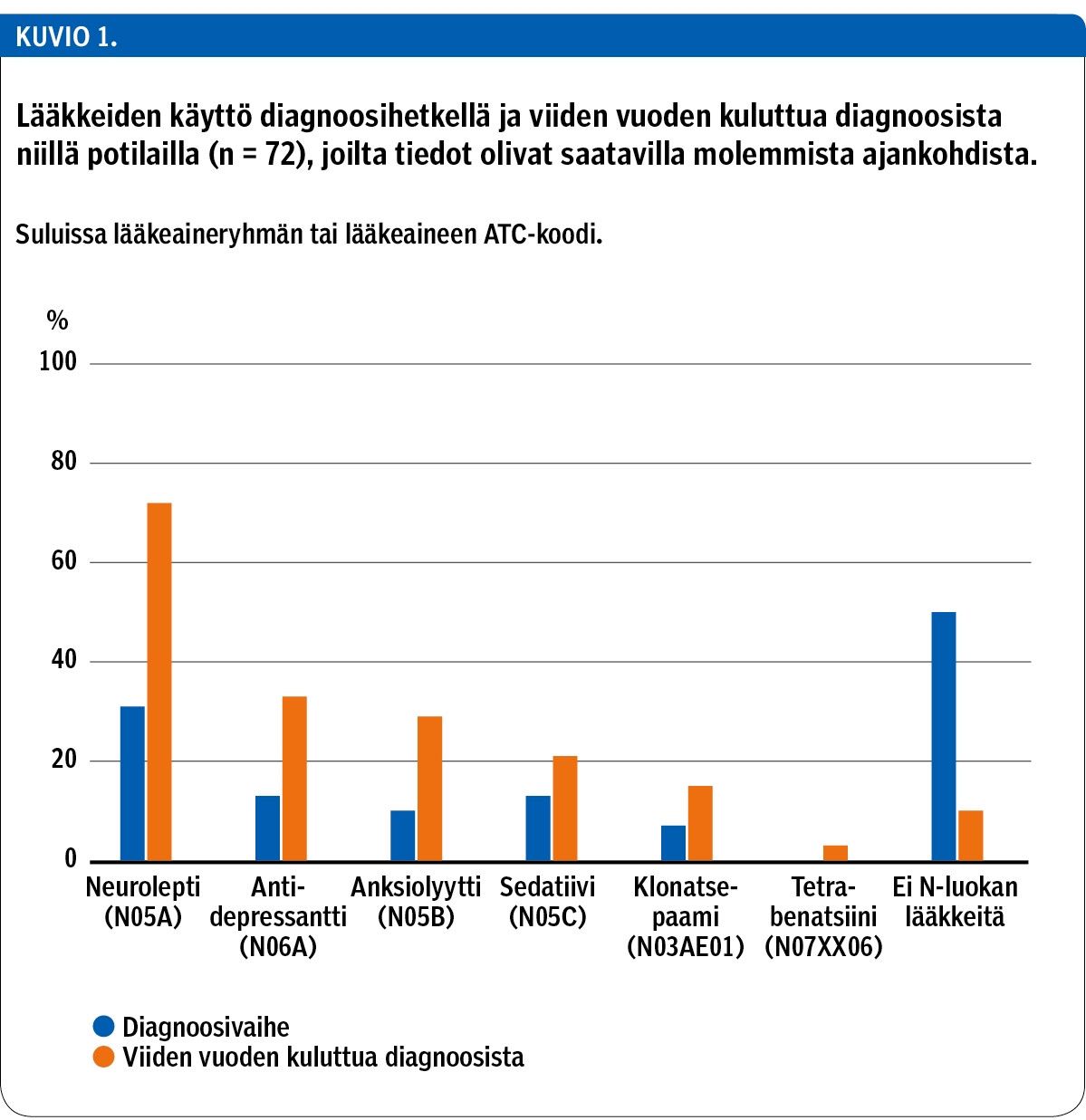
Tässä vaiheessa kyseisistä 81 potilaasta 18 (22 %) asui pysyvästi hoitolaitoksessa, 15 (19 %) itsenäisesti kotona ja loput tuetusti kotona tai kodinomaisessa asumisyksikössä. Hoitolaitoksessa asuvista 61 % sai neuroleptiä, 61 % rauhoittavaa lääkettä ja 50 % antidepressanttia. Itsenäisesti kotona asuvista taas 53 % käytti neuroleptiä, 53 % rauhoittavaa lääkettä ja 20 % antidepressanttia. Kaikkien lääkeaineryhmien käyttö lisääntyi taudin edetessä potilailla (n = 72), joilta oli käytettävissä lääkitystiedot sekä diagnoosivaiheesta että viiden vuoden kuluttua diagnoosista (kuvio 1).
Yhdistelmäkäyttö ja harvoin käytetyt lääkkeet
Diagnoosivaiheessa kahden tai useamman keskushermostoon vaikuttavan lääkkeen yhdistelmää käytti 46 potilasta (26 %) (Liitekuvio 1A artikkelin sähköisessä versiossa, www.laakarilehti.fi > sisällysluettelot > 32/2018). Viiden vuoden kuluttua diagnoosista yhdistelmälääkitys oli käytössä 52 potilaalla (64 %) (liitekuvio 1B).
Diagnoosivaiheessa neuroleptien käyttö vaihteli sen mukaan, lääkittiinkö potilasta lisäksi anksiolyytillä, sedatiivilla tai klonatsepaamilla. Viiden vuoden kuluttua diagnoosista eroja ei ollut (taulukko 2). Harvoin käytettyjä lääkkeitä (käyttäjiä < 10 % potilaista) olivat amantadiini, biperideeni, karbamatsepiini, levodopa/karbidopa -yhdistelmävalmiste, lyhytvaikutteinen bentsodiatsepiinijohdos, melatoniini, melatoniiniagonisti, memantiini, rivastigmiini ja valproaatti.
Muutokset tutkimusjakson aikana
Neuroleptilääkitys oli diagnoosivaiheessa muita useammin käytössä niillä potilailla, jotka oli diagnosoitu ennen vuotta 2002. Muita eroja lääkkeiden käytössä ei havaittu tutkimusajankohdan alku- ja loppupuolen välillä (kuvio 2).
Pohdinta
Suomessa Huntingtonin tautiin liittyvän korean hoidossa käytetään lähes yksinomaan neuroleptejä, joista haloperidoli on selvästi yleisin. Hermostoon vaikuttavien lääkkeiden käyttö lisääntyy taudin edetessä.
Cochrane-yhteisö on arvioinut, että käytettävissä olevan näytön taso ei riitä suosituksen antamiseen Huntingtonin taudin motoristen tai muiden oireiden hoidosta (10).
American Academy of Neurology (AAN) sen sijaan on julkaissut tautiin liittyvän korean hoitosuosituksen. Lääkkeiksi suositellaan tetrabenatsiinia, amantadiinia tai rilutsolia (11). Suositusta on kuitenkin kritisoitu, ja sen asema kliinisenä hoitosuosituksena on kyseenalaistettu (4,8,12). Tutkimuksemme perusteella suomalainen hoitokäytäntö eroaa merkittävästi AAN:n suosituksesta, sillä koreaa hoidettiin yleensä neurolepteillä. AAN:n suosittelemien lääkkeiden käyttö oli hyvin vähäistä. Lisäksi klonatsepaamilla oli joissakin tapauksissa hoidettu myös motorisia oireita, mitä käytäntöä tutkimusnäyttö ei tue (8). Korean hoito Suomessa ei kuitenkaan oleellisesti eroa kansainvälisestä käytännöstä: hoitoon käytetään neuroleptejä tai tetrabenatsiinia (3,8).
Tetrabenatsiinin ja neuroleptien suosio ensisijaisena vaihtoehtona vaihtelee maittain (3). Tutkimuksessamme tetrabenatsiinin käyttäjien osuus oli pieni, kuten joissain aiemmissa ulkomaisissa tutkimuksissa (13,14), mutta myös suurempia osuuksia on raportoitu (15,16). Vaikka tetrabenatsiinilla on osoitettua tehoa koreaan, sen ei ole osoitettu parantavan potilaan yleistä toimintakykyä. Lääkkeen mahdollisia sivuvaikutuksia ovat parkinsonismi ja vakavat psyykkiset oireet (8,9,17). On myös todennäköistä, että tetrabenatsiinin useita neuroleptejä huomattavasti kalliimpi hinta vaikuttaa hoitopäätöksiin.
Tutkimustuloksemme kuvastavat tilannetta Suomessa vuosina 1987–2010, ja on mahdollista, että Huntingtonin taudin lääkehoidossa on sen jälkeen tapahtunut muutoksia. Vuoden 2010 jälkeen ei kuitenkaan ole julkaistu hoitoa linjaavia suosituksia tai asiantuntijalausuntoja, eikä markkinoille ole tullut uusia lääkkeitä. Esimerkiksi tetrabenatsiinin euromääräinen myynti on Suomessa lisääntynyt vain 15 % vuosien 2013 ja 2016 välillä (Fimea). Näin ollen tuloksemme kuvastanevat melko hyvin myös nykytilannetta.
Neuroleptien tehosta korean hoidossa on vain vähän tutkimusnäyttöä – ja sekin ristiriitaista. Käyttö perustuukin lähinnä kliiniseen kokemukseen (18). Neuroleptit saattavat pahentaa esimerkiksi dystoniaa ja etenkin negatiivisia motorisia oireita, kuten bradykinesiaa, jotka ovat Huntingtonin taudissa yleisiä ja erityisen haitallisia. Joillakin potilailla kuitenkin neuroleptien käyttö on aiheellista samanaikaisten psyykkisten oireiden takia (5,6,19). Lääkeaineryhmän kokonaiskäyttö ei kerro siitä, kuinka paljon sitä käytetään nimenomaan liikehäiriön hoitoon.
Korean hoitoon on ehdotettu päätöksenteon tueksi vuokaavioita, joissa huomioitaisiin myös potilaan psyykkinen tila (3,4,8,12). Päätöstä tehtäessä on arvioitava, onko koreasta potilaalle sellaista haittaa, että lääkkeiden käyttöön liittyvät riskit kannattaa ottaa (9). Yleisemminkin oireenmukaisen lääkityksen hyötyjä ja tarpeellisuutta tulisi arvioida säännöllisesti. Tässä auttaa, että lääkehoidolle asetetaan selvät tavoitteet.
Suomessa neuroleptien käyttö oli diagnoosivaiheessa yhtä yleistä kuin Euroopassa keskimäärin, mutta meillä käyttö näyttää yleistyvän nopeammin taudin edetessä (13). Keskimääräistä yleisempi käyttö voi selittyä sillä, että Suomessa ei ole Huntingtonin taudin hoitoon perehtyneitä keskuksia. Tästä johtunee, että tutummat ja laajakirjoisemmat, sekä motorisiin että psykiatrisiin oireisiin tehoavat lääkkeet ovat meillä suositumpia.
Neuroleptejä käyttävien potilaiden osuus kuitenkin pieneni tutkimusjakson aikana. Tämä johtunee osin diagnostisen viipeen lyhenemisestä (20) ja siten tutkittujen potilaiden lievemmästä taudinkuvasta tarkastelujakson loppupuolella. Neurolepteistä käytetyin oli haloperidoli. Sen osuus käytöstä oli diagnoosivaiheessa 80 %, kun diagnoosi oli tehty ennen vuotta 2002 ja 32 %, kun diagnoosi oli tehty vuosina 2002–2010. Haloperidoli on suosituin neurolepti Huntingtonin taudin hoidossa myös Saksassa ja Italiassa, joissa sen osuus on 24–32 % kaikista neurolepteistä. Britanniassa suosituin on sen sijaan olantsapiini (16), ja Suomessa tutkimusjakson aikana suosituimmaksi neuroleptiksi ylsi ketiapiini.
Näyttöä minkään neuroleptin paremmuudesta ei ole (18), joten lääke valitaan empiirisesti potilaan kokonaistilanteen ja hoitavan lääkärin kokemuksen ja tottumusten perusteella. Kansainvälisessä kyselyssä Huntingtonin taudin asiantuntijat pitivät ensisijaisina vaihtoehtoina risperidonia (43 % vastaajista), olantsapiinia (39 % vastaajista), tiapridia (29 % vastaajista) ja haloperidolia (24 % vastaajista) (3).
Mielialalääkkeiden käyttö oli suomalaisilla potilailla selvästi harvinaisempaa kuin muilla (13,16,21), kun taas rauhoittavien lääkkeiden käyttö oli tavallista. Rauhoittavia lääkkeitä (anksiolyytit, sedatiivit, klonatsepaami) käytti Suomessa diagnoosivaiheessa joka neljäs potilas ja viiden vuoden kuluttua diagnosoinnista joka toinen. Britanniassa anksiolyytti tai hypnootti on käytössä 35,9 %:lla potilaista (21). Nämä osuudet vaikuttavat suurilta ottaen huomioon, että lääkkeet voivat pahentaa tautiin kuuluvaa tasapainohäiriötä. Unihäiriötä oli monissa tapauksissa hoidettu rauhoittavilla lääkkeillä ja vanhan polven fentiatsiinineurolepteillä. Suositeltavampia olisivat kuitenkin melatoniinin kaltaiset lääkkeet, jotka eivät häiritse unen rakennetta (22, 23). Antidepressanttien käytön suhteellinen vähäisyys, rauhoittavien lääkkeiden yleisyys sekä neuroleptiä käyttävien potilaiden osuuden nopea kasvu ensimmäisten viiden hoitovuoden aikana herättävät kysymyksen, onko Huntingtonin tautiin liittyvien mielialaoireiden lääkehoito Suomessa optimaalista (4). Kuitenkin valtaosalla potilaista, jotka käyttivät mielialalääkkeitä, käytössä oli SSRI- tai SNRI-ryhmän lääke kansainvälisten asiantuntijasuositusten mukaisesti (4,6).
Tämän tutkimuksen vahvuutena on valtakunnallinen kattavuus ja tietojen kerääminen yli neljännesvuosisadan ajalta. Heikkoudet liittyvät ensisijaisesti takautuvaan tutkimusasetelmaan ja tietojen keräämiseen sairauskertomuksista. Taudin seurannan ja sairauskertomusmerkintöjen kirjaamisen käytännöt vaihtelivat huomattavasti, eikä lääkityksiä aina ollut merkitty kattavasti. Potilasmäärien ero havaintopisteissä johtuukin ensisijaisesti näistä sekoista. Kuolemista johtuva kato oli viiden vuoden kuluttua diagnosoinnista vain 19 potilasta. Sairauskertomustietojen perusteella ei aina ollut mahdollista määrittää lääkkeiden täsmällisiä käyttöindikaatioita eikä näin ollen myöskään sitä, oliko niillä saavutettu toivottu vaikutus. Tietoja ravintolisien tai luontaistuotteiden käytöstä oli merkitty hyvin harvoin, vaikka niiden käyttö saattaa vaikuttaa potilaan päätöksentekoon ja joissain tapauksissa lääkevalintoihinkin.
Tutkimuksemme mukaan Huntingtonin taudin lääkehoito perustuu Suomessa vahvasti neurolepteihin, joista yleisimmin on käytössä haloperidoli. Motoristen oireiden lääkehoito ei eroa merkittävästi kansainvälisistä käytännöistä. Hoidossa lienee kuitenkin vielä parannettavaa, sillä mielialalääkityksen käyttö on vähäistä ja rauhoittavien lääkkeiden käyttö runsasta.
Jussi Sipilä: Luentopalkkiot (Boehringer-Ingelheim, Merck, Pfizer), matka-, majoitus- ja kokouskulut (Abbvie, Medtronic, Merck Serono, Novartis, Nordic Lundbeck, Orion, Sanquin), korvaus esitteen tuottamisesta (Rinnekoti-Säätiö).
Valtteri Kaasinen: Konsultointi (Abbvie, Lundbeck), asiantuntijalausunnot (Abbvie, Zambon), luentopalkkiot (Abbvie, GE Healthcare, Medtronic, Nordic Infucare, Orion Pharma), matka-, majoitus- ja kokouskulut (Abbvie, Lundbeck, Medtronic, Nordic Infucare).
Kari Majamaa: Luentopalkkiot (Biogen, Sanofi, UCB), matka-, majoitus- ja kokouskulut (Merck).
Tästä asiasta tiedettiin
Huntingtonin taudin oireiden hoidosta ei ole olemassa kansainvälisen konsensuksen saavuttanutta näyttöön perustuvaa suositusta.
Motoristen oireiden hoitona käytetään neuroleptejä ja tetrabenatsiinia, joiden suhteellinen suosio vaihtelee.
Mieliala-, käytös- ja unihäiriöt ovat helpotettavissa, mutta kognitiivisiin oireisiin tehoavaa lääkitystä ei ole.
Tämä tutkimus opetti
Huntingtonin taudin motorisia oireita hoidettiin Suomessa neurolepteillä, joista suosituimmat olivat haloperidoli ja ketiapiini. Tetrabenatsiinin käyttö sen sijaan oli erittäin vähäistä.
Huomattava osa potilaista käytti rauhoittavia lääkkeitä, jotka saattavat pahentaa taudista aiheutuvia tasapaino-ongelmia.
Potilaiden mieliala- ja unihäiriöiden lääkehoito vaikuttaa Suomessa puutteelliselta.
- 1
- Ross CA, Aylward EH, Wild EJ ym. Huntington disease: natural history, biomarkers and prospects for therapeutics. Nat Rev Neurol 2014;10:204–16.
- 2
- Craufurd D, MacLeod R, Frontali M ym. Diagnostic genetic testing for Huntington’s disease. Pract Neurol 2015;15:80–4.
- 3
- Burgunder JM, Guttman M, Perlman S ym. An international survey-based algorithm for the pharmacologic treatment of chorea in Huntington’s disease. PLoS Curr Huntington Dis 2011;1. doi: 10.1371/currents.RRN1260
- 4
- Zielonka D, Mielcarek M, Landwehrmeyer GB. Update on Huntington’s disease: advances in care and emerging therapeutic options. Parkinsonism Relat Disord 2015;21:169–78.
- 5
- Phillips W, Shannon KM, Barker RA. The current clinical management of Huntington’s disease. Mov Disord 2008;23:1491–504.
- 6
- Videnovic A. Treatment of Huntington disease. Curr Treat Options Neurol 2013;15:424–38.
- 7
- Sipilä JOT, Hietala M, Siitonen A ym. Epidemiology of Huntington’s disease in Finland. Parkinsonism Relat Disord 2015;21:46–9.
- 8
- Killoran A, Biglan KM. Current therapeutic options for Huntington’s disease: good clinical practice versus evidence-based approaches? Mov Disord 2014;29:1404–13.
- 9
- Jankovic J, Roos RAC. Chorea associated with Huntington’s disease: to treat or not to treat? Mov Disord 2014;29:1414–18.
- 10
- Mestre T, Ferreira J, Coelho MM ym. Therapeutic interventions for symptomatic treatment in Huntington’s disease. Cochrane Database Syst Rev 2009;3:CD006456. doi: 10.1002/14651858.CD006456.pub2
- 11
- Armstrong MJ, Miyasaki JM. Evidence-based guideline: pharmacological treatment of chorea in Huntington disease. Report of the guideline development subcommittee of the American Academy of Neurology. Neurology 2012;79: 597–603.
- 12
- Reilmann R. Pharmacological treatment of chorea in Huntington’s disease – good clinical practice versus evidence-based guideline. Mov Disord 2013;28:1030–3.
- 13
- Keogh R, Frost C, Owen G ym. Medication use in early-HD participants in track-HD: an investigation of its effects on clinical performance. PLoS Curr Huntington Dis 2016;8. doi: 10.1371/currents.hd.8060298fac1801b01ccea6acc00f97cb
- 14
- Zarowitz BJ, O’Shea T, Nance M. Clinical, demographic, and pharmacologic features of nursing home residents with Huntington’s disease. J Am Med Dir Assoc 2014;15:423–8.
- 15
- Désaméricq G, Dolbeau G, Verny C ym. Effectiveness of anti-psychotics and related drugs in the huntington french-speaking group cohort. PLoS One 2014;9:e85430. doi: 10.1371/journal.pone.0085430
- 16
- Priller J, Ecker D, Landwehrmeyer B ym. A Europe-wide assessment of current medication choices in Huntington’s disease. Mov Disord 2008;23:1788.
- 17
- Huntington Study Group. Tetrabenazine as antichorea therapy in Huntington disease: a randomized controlled trial. Neurology 2006;66:366–72.
- 18
- Frank S. Treatment of Huntington’s disease. Neurotherapeutics 2014;11:153–60.
- 19
- Groves M, van Duijn E, Anderson K ym. An international survey-based algorithm for the pharmacologic treatment of irritability in Huntington’s disease. PLoS Curr Huntington Dis 2011;3. doi: 10.1371/currents.RRN1259
- 20
- Sipilä JOT. Huntington’s diseasein Finland. Epidemiologic, genetic and clinical studies. Väitöskirja, Annales Universitatis Turkuensis 2017:71–2.
- 21
- Sackley C, Hoppitt TJ, Calvert M ym. Huntington’s disease: current epidemiology and pharmacological management in UK primary care. Neuroepidemiology 2011;37:216–21.
- 22
- van Wamelen DJ, Roos RA, Aziz NA. Therapeutic strategies for circadian rhythm and sleep disturbances in Huntington disease. Neurodegener Dis Manag 2015;5:549–9.
- 23
- Morton AJ. Circadian and sleep disorder in Huntington’s disease. Exp Neurol 2013;243:34–
Drug treatment of adult-onset Huntington’s disease in Finland
Background No universally accepted evidence-based guidelines are available for the drug treatment of symptoms in Huntington’s disease (HD) and expert opinion differs between regions globally.
Methods Persons with a diagnosis of HD in Finland in 1987–2010 were identified from national registries and patient charts were used to verify the diagnosis and gather clinical information.
Results Movement disorders of Finnish HD patients were mainly treated with neuroleptics. Of these, haloperidol was the most common although its proportion declined during the study period. Tetrabenazine was used very rarely, less often than clonazepam. Drugs with sedative potential were used quite often. Sleep medications that do not disrupt sleep architecture were seldom utilized. Drug treatment did not differ between men and women or between young and old patients.
Conclusions It seems that Finnish patients with HD are treated largely following international consensus, although the treatment of affective and sleep disorders might be optimized.