Neuroborrelioosin oireet, diagnostiikka ja hoito
Neuroborrelioosin yleisimmät oireet ja löydökset ovat kivulias meningoradikuliitti, kasvohermohalvaus ja lymfosytaarinen meningiitti.
Oireisto ilmaantuu yleensä muutaman viikon kuluessa infektion alusta.
Diagnostiikka perustuu kliinisen kuvan lisäksi seerumin borreliavasta-aineisiin sekä aivo-selkäydinnestelöydöksiin.
Neuroborrelioosi voidaan hoitaa 2–4 viikon doksisykliinihoidolla suun kautta tai 2–3 viikon suonensisäisellä keftriaksonihoidolla.

Lymen borrelioosi on pohjoisen pallonpuoliskon yleisin puutiaisvälitteinen infektiosairaus. Sen aiheuttaa spirokeettoihin kuuluva bakteeri Borrelia burgdorferi sensu lato (s.l. eli "laajassa merkityksessä", myöhemmin borrelia), jonka alalajeista B. afzelii, B. garinii ja B. burgdorferi sensu stricto (s.s. eli "ahtaassa merkityksessä") aiheuttavat valtaosan tautitapauksista Euroopassa. Suomen puutiaisissa kaksi ensin mainittua ovat tavallisimmat alalajit. Pohjois-Amerikassa borrelioosin pääasiallinen aiheuttaja on B. burgdorferi s.s., joka on muita alalajeja nivelhakuisempi. B. garinii on puolestaan tavallisin neuroborrelioosin aiheuttaja, vaikkakin myös muut alalajit voivat hakeutua keskushermostoon.
Suomessa borreliaspirokeettaa levittävät Ixodes-suvun puutiaisista I. ricinus ja I. persulcatus. Borrelia kolonisoituu puutiaisen suolistoon ja siirtyy sieltä sylkeen puutiaisen ruokaillessa. Puutiaisen on oltava kiinnittyneenä ihoon vähintään 12–24 tuntia, jotta spirokeetat ehtivät siirtyä syljen välityksellä ihmiseen. Suomessa noin viidennes puutiaisista kantaa borreliabakteeria, mutta alueiden välillä on vaihtelua, sillä Ahvenanmaalla 23 %, Etelä-Suomessa 20 %, Keski-Suomessa 15 % ja Oulun seudulla 21 % puutiaisista on infektoituneita (1,2). On arvioitu, että keskimääräinen riski saada borrelioosi yksittäisestä puutiaisen puremasta on noin 2 % (3).
Borreliaspirokeetat leviävät iholta verenkierron ja mahdollisesti myös imusuonten kautta muualle elimistöön, tyypillisesti hermostoon ja niveliin (4). Tavallisin borreliainfektion ilmentymä on iholle puutiaisen piston kohdalle ilmaantuva hiljalleen laajeneva erythema migrans -ihottuma, joka todetaan 80–90 %:lla infektoituneista (5). Harvinaisempi borrelioosin varhaisvaiheen iholöydös on useimmiten korvalehdessä, kivespussissa tai nännin seudussa todettava kyhmy eli borrelialymfosytooma.
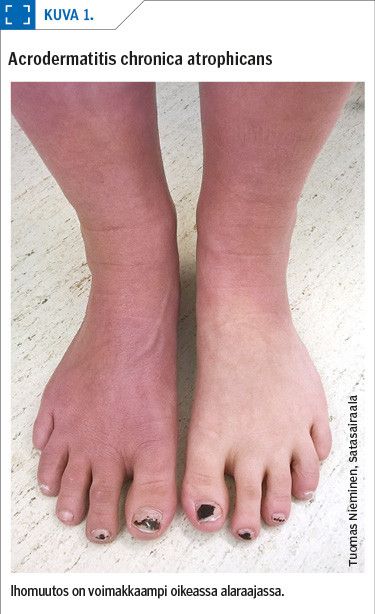
Arviolta 3–12 %:lle borreliatartunnan saaneista kehittyy neurologisia oireita, mutta borrelian aiheuttamat niveltulehdukset ovat Euroopassa neuroborrelioosia harvinaisempia (6,7). Lymen borrelioosi voi harvoin aiheuttaa myös sydän- tai silmäoireita tai pitkäkestoisen surkastuttavan ihoinfektion, joka tunnetaan nimellä acrodermatitis chronica atrophicans.
Suomessa borrelioosin ilmaantuvuus on suurin rannikkoseuduilla, erityisesti Ahvenanmaalla. Ilmaantuvuus koko Suomessa on keskimäärin 40/100 000, mutta Ahvenanmaalla yli 1 000/100 000 (8). Borrelioosin ilmaantuvuutta seurataan laboratorioiden ilmoittamien positiivisten vasta-aine- ja nukleiinihaponosoitustestitulosten avulla. Niiden perusteella ilmaantuvuus on ollut 2000-luvulla kasvussa, joskin kasvu on tasaantunut vuoden 2017 jälkeen.
Viime vuosina mikrobiologian laboratoriot ovat raportoineet Tartuntatautirekisteriin hieman yli 2 000 borrelioositapausta vuosittain. Nämä löydökset edustavat lähinnä levinneitä infektioita. Vasta-ainetesti ei kuulu erythema migransin rutiinidiagnostiikkaan, sillä akuutissa infektiossa vasta-aineita ei ole välttämättä ehtinyt vielä muodostua. Erythema migrans -tapaukset diagnosoidaan kliinisin perustein ja raportoidaan julkisen terveydenhuollon avohoidon hoitoilmoitusjärjestelmään (8).
Oleellista borrelioositartuntojen ehkäisemisessä on puutiaisten puremien välttäminen peittävällä pukeutumisella ja tarvittaessa hyönteiskarkotteilla sekä iholle kiinnittyneiden puutiaisten välitön poistaminen – eli päivittäiset punkkisyynit. Poistetun puutiaisen testaamista borreliabakteerin kantajuuden varalta apteekeista saatavilla testeillä ei suositella, koska tulos ei kerro tartunnan saamisen todennäköisyydestä.
Pohjois-Amerikassa eräissä tilanteissa Ixodes-suvun puutiaisen pureman jälkeen antibioottiprofylaksina käytetään 200 mg:n kerta-annosta doksisykliiniä. Sitä suositellaan, mikäli puutiainen on ollut kiinnittyneenä yli 36 tuntia, kyseessä on suuren ilmaantuvuuden alue (yli 10/100 000 kolmena vuonna, jolloin puutiaisten borreliakantajuus on yleensä yli 20 %), ja annos voidaan antaa 72 tunnin kuluessa puutiaisen poistosta (9). Doksisykliiniprofylaksilla voidaan estää noin 2/3 tartunnoista, ja se pitäisi antaa 51 potilaalle, jotta yksi borrelioositartunta estetään (10). Nykyinen tutkimustieto ei puolla doksisykliinin kerta-annoksen lisäksi muiden antibioottien profylaktista käyttöä.
Euroopassa ei toistaiseksi ole suositeltu antibioottiprofylaksia puutiaisen pureman jälkeen, vaikka olosuhteet monissa Euroopan maissa – mukaan lukien Etelä-Suomen rannikkoseudut – ovat paikoitellen samankaltaiset kuin Pohjois-Amerikassa.
Oireet
Neurologiset oireet alkavat yleensä muutaman viikon kuluessa (vaihteluväli 1–12 viikkoa tai jopa pidempi) puutiaisen puremasta, minkä vuoksi neuroborrelioosidiagnooseja tehdään etenkin kesäkuun ja joulukuun välisenä aikana (11). Puutiaisen pureman tai erythema migrans -ihomuutoksen on huomannut tai muistaa alle puolet potilaista, joten näiden puuttuminen ei sulje pois neuroborrelioosin mahdollisuutta.
Neuroborrelioosi voidaan jakaa oireiden keston perusteella akuuttiin, eli alle 6 kuukautta kestäneeseen ja myöhäiseen eli yli 6 kuukautta kestäneeseen tautimuotoon. Tapauksista 95 % on diagnoosivaiheessa akuutteja (11). Useimmiten neuroborrelioosi oireilee perifeeristen hermojen ja aivokalvojen tulehduksena, ja aivojen tai selkäytimen parenkyymin tulehtumisen aiheuttamat oireet ovat harvinaisia.
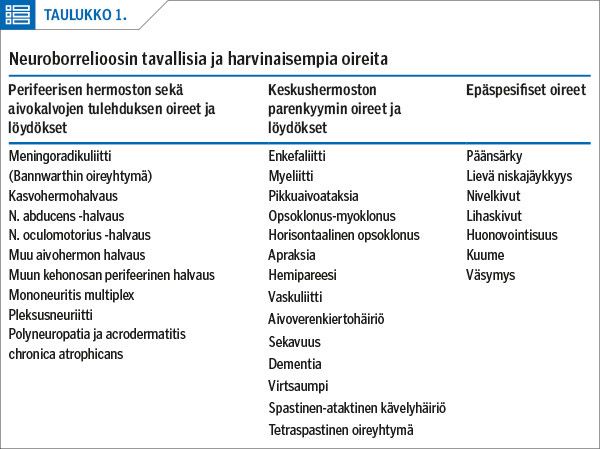
Tavallisin taudinkuvista on kivulias meningoradikuliitti, jota kutsutaan Bannwarthin oireyhtymäksi (taulukko 1). Meningoradikuliitissa kivun voimakkuus ja paikka voivat vaihdella. Kipu paikantuu usein reiteen, vatsaan, selkään tai niska-hartiaseutuun, mutta se voi sijaita missä tahansa keholla. Tyypillisesti kipu voimistuu öisin, jopa niin että jotkut potilaat kertovat nousseensa öisin suihkuun oireita lievittääkseen. Radikulaarinen oireisto voi olla myös motorispainotteinen, mutta sensorinen oireisto on selvästi yleisempi.
Bannwarthin oireyhtymään liittyy usein lymfosytaarinen meningiitti sekä perifeerisen hermon halvaus (12). Perifeerisen hermon halvauksista yleisin on kasvohermohalvaus, mutta mikä tahansa aivohermo tai muu perifeerinen hermo saattaa sairastua. Aivohermon halvaus voi olla myös molemminpuolinen. Harvinainen akuutti keskushermoston parenkyymin infektio voi ilmetä enkefaliittina tai myeliittinä.
Lapsilla neuroborrelioosin tavallisin ilmentymä on kasvohermohalvaus, johon voi liittyä meningiitti. Kivulias meningoradikuliitti on lapsilla harvinainen.
Varsinaisten neurologisten oireiden lisäksi potilaalla on usein epäspesifisiä subjektiivisia oireita, kuten päänsärkyä, nivel- ja lihaskipuja sekä väsymystä; monet kuvaavat tilaa flunssaisena oloksi ilman hengitystieoireita. Yleisoireet ilman neurologisia oireita ja löydöksiä eivät viittaa neuroborrelioosiin, mutta ne voivat liittyä borreliabakteerien disseminaatioon.
Myöhäisen neuroborrelioosin tavallisimpia ilmentymiä on acrodermatitis chronica atrophicans -ihomuutokseen liittyvä polyneuropatia, joskin pelkkä krooninen polyneuropatia lienee vain harvoin borrelioosin aiheuttama (13). Tämä sinipunerva ihomuutos on naisilla tavallisempi kuin miehillä ja se ilmenee raajojen ojentajapuolilla tois- tai molemminpuolisena (kuva 1) (14). Myöhäinen perifeerisen hermoston neuroborrelioosi voi ilmentyä myös mononeuropatiana tai radikulopatiana. Vaskuliitti, krooninen progressiivinen enkefaliitti tai enkefalomyeliitti ovat mahdollisia keskushermoston parenkyymin myöhäisen neuroborrelioosin ilmentymiä.
Diagnostiikka
Neuroborrelioosin diagnostiikka perustuu tietoon mahdollisesta puutiaisaltistuksesta ja erythema migrans -ihottumasta, neurologisiin oireisiin ja kliinisiin löydöksiin sekä seerumin vasta-ainepositiivisuuteen ja aivo-selkäydinnestelöydöksiin. Euroopassa aivo-selkäydinnestetutkimusta suositellaan aina neuroborrelioosia epäiltäessä. Kliinisesti ilmeisissä tapauksissa, varsinkin jos paranemista on jo ehtinyt tapahtua, kajoavasta toimenpiteestä joskus pidättäydytään. Tulos saadaan usein viiveellä, joten negatiivinen tulos ei aina ehdi lyhentää empiirisesti aloitettua hoitoa. Kuitenkin erotusdiagnostiikan kannalta siitä on hyötyä.
Neuroborrelioosia voidaan pitää varmana, jos potilaalla on sille tyypilliset oireet ilman muuta selittävää syytä ja aivo-selkäydinnesteessä todetaan lymfosytaarinen pleosytoosi (vähintään 5 valkosolua/µl) ja intratekaalinen vasta-ainemuodostus borreliaa kohtaan.
Borrelioosin diagnostiikassa on syytä pitäytyä luotettavissa, akkreditoitujen laboratorioiden tarjoamissa testeissä. Kuvantamistutkimukset eivät ole välttämättömiä neuroborrelioosin diagnostiikassa, mutta niitä käytetään joskus muiden neurologisten sairauksien poissulkemiseksi (15). Neuroborrelioosipotilaan kuvantamistutkimuksissa ei välttämättä todeta poikkeavia löydöksiä, mutta kuvantaminen voi paljastaa neuriitin, meningiitin, myeliitin, enkefaliitin tai vaskuliitin.
Serologia
Borreliavasta-aineiden määrittäminen seerumista ja aivo-selkäydinnesteestä on neuroborrelioosin diagnostiikan kulmakiviä. Seerumista vasta-aineet määritetään kaksivaiheista testausta käyttäen. Ensin näytteestä tehdään herkempi seulontatutkimus, ja mikäli vasta-aineita todetaan, sama näyte tutkitaan uudelleen toisella menetelmällä. Menetelmät vaihtelevat laboratorioittain.
Vasta-aineiden muodostumiseen kuluu aikaa, ja siksi taudin alkuvaiheessa niitä ei välttämättä todeta. IgG-vasta-aineita kehittyy lähes kaikille 6–8 viikon kuluessa oireiden alusta. IgM-vaste on nopeampi, mutta jos IgG-reaktiota ei kehity lainkaan oireiden kestettyä viikkoja, pelkkä IgM-löydös ei ole viitteellinen borrelioosille (16). Joskus IgM-löydös voi olla merkki vanhasta serologisesta jäänteestä tai ristireaktiosta esimerkiksi herpes simplex- tai Epstein–Barrin virukselle.
Vasta-ainetasot laskevat useimmilla ajan kuluessa, mutta lasku ei korreloi luotettavasti hoitovasteeseen, joten vasta-aineiden seuranta hoidetun taudin jälkeen on tarpeetonta.
Neuroborrelioosissa käynnistyy intratekaalinen vasta-ainemuodostus borreliaa kohtaan. Seerumin vasta-aineet tulee määrittää samanaikaisesti tai korkeintaan kahden vuorokauden erolla aivo-selkäydinnestenäytteen vasta-aineiden kanssa. Näiden näytteiden avulla lasketaan intratekaalisen vasta-ainetuotannon IT-indeksi, jonka suurentunut arvo kertoo intratekaalisesta vasta-ainemuodostuksesta ja tukee neuroborrelioosin diagnoosia. Mikäli IT-indeksi on matala, aivo-selkäydinnesteessä todetut vasta-aineet ovat tihkuneet seerumista veri-aivoesteen läpi.
Borreliavasta-aineiden määrittämistä potilailta, joilla on ainoastaan epäspesifisiä oireita, kuten väsymystä, nivelkipuja ja lihassärkyjä, ei suositella. Tästä voidaan harkinnan mukaan poiketa, mikäli potilaalla on tiedossa puutiaisen pisto tai muu merkittävä puutiaisaltistus ja hänelle kehittyy akuutteja, aiemmasta poikkeavia, disseminaatioon sopivia oireita. Oireettomia henkilöitä ei pidä testata esimerkiksi puutiaisen piston jälkeen, sillä vasta-ainepositiivisuus oireettomalla henkilöllä ei edellytä hoitoa.
Suomessa seroprevalenssi aikuisväestössä oli 3,9 % vuonna 2011 ja lienee samaa luokkaa tälläkin hetkellä (17).
CXCL13
CXCL13 on kemokiini, jota mononukleaariset solut alkavat tuottaa borrelian tunkeuduttua subaraknoidaalitilaan. Se houkuttelee paikalle B-soluja, ja tämä aiheuttaa neuroborrelioosille tyypillisen lymfosytaarisen meningiitin.
Aivo-selkäydinnesteen CXCL13-pitoisuus suurenee nopeasti infektion alkuvaiheessa, jopa päiviä ennen vasta-ainetuotannon käynnistymistä. Tuoreessa meta-analyysissä optimaaliseksi CXCL13-pitoisuuden raja-arvoksi määritettiin 162 pg/ml: sillä saavutettiin 89 %:n sensitiivisyys ja 96 %:n spesifisyys neuroborrelioosin diagnostiikassa (18).
Aivo-selkäydinnesteen CXCL13-pitoisuus pienenee nopeasti hoidon alettua, joten se soveltuu tarvittaessa hoidon tehon seurantaan, mikäli potilas ei toivu odotetusti. Rutiiniluonteiset aivo-selkäydinnestenäytekontrollit ovat tarpeettomia, mutta tutkimus kannattaa uusia, mikäli potilaan oireet voimistuvat uudelleen paranemisprosessin jo käynnistyttyä tai oireilu jatkuu voimakkaana hoidosta huolimatta. CXCL13:n avulla voidaan tunnistaa myös uusi neuroborrelioosi sellaisella potilaalla, jolla on jo aiemmin hoidettu neuroborrelioosi ja intratekaalinen vasta-ainetuotanto on edelleen käynnissä.
CXCL13 ei ole täysin spesifinen neuroborrelioosille. Neurosyfiliksen aiheuttaja, spirokeetta Treponema pallidum, voi myös saada aivo-selkäydinnesteen CXCL13-pitoisuuden suureksi, ja suurentuneita pitoisuuksia on tavattu myös keskushermostolymfoomaa, HIV-infektiota, kryptokokkoosia ja trypanosomiaasia sairastavilla potilailla. Seerumin CXCL13-pitoisuuden mittaaminen ei ole hyödyllistä neuroborrelioosin diagnostiikassa, sillä pitoisuudet eivät ole siinä merkittävästi suurentuneita (19).
Aivo-selkäydinnesteen CXCL13-tutkimus on nykyisin tilattavissa jokaisen sairaanhoitopiirin laboratoriosta.
Aivo-selkäydinnesteen borrelia-PCR ja viljely
Aivo-selkäydinnesteen borrelia-PCR-testin herkkyys on korkeintaan 40 %, joten negatiivinen testitulos ei sulje pois neuroborrelioosia (16). Tutkimuksesta voi kuitenkin olla hyötyä taudin alkuvaiheessa, jolloin vasta-aineita ei ole vielä ehtinyt muodostua.
Borreliaviljely on hidas ja varsin epäherkkä menetelmä, joten se ei ole kliinisessä käytössä, vaikka se olisi periaatteessa varmin tapa osoittaa borrelia-infektio.
Hoito
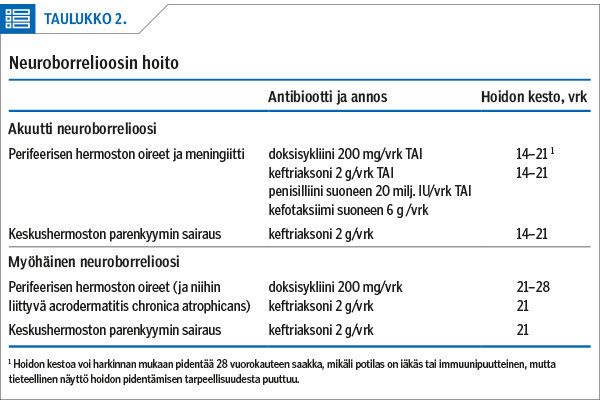
Neuroborrelioosi voidaan hoitaa 2–4 viikon kestoisella doksisykliini- tai keftriaksonihoidolla (taulukko 2). Vaikka doksisykliini on suun kautta otettava lääke, se on keftriaksoniin verrattuna yhtä tehokas akuutin, perifeerisiin hermoihin ja aivokalvoihin levinneen taudin hoidossa (20,21). Koska doksisykliini on helpompi antaa ja edullisempi, sitä voidaan pitää ensisijaisena hoitovaihtoehtona. Sen tehoa syvissä keskushermostoinfektioissa, kuten enkefaliitissa, myeliitissä ja vaskuliitissa, ei ole osoitettu satunnaistetuissa tutkimuksissa, mutta yksittäisessä potilassarjassa myös syvistä keskushermosto-oireista kärsineet potilaat toipuivat (22). Kansainvälisissä suosituksissa keskushermoston parenkyymi-infektioon (mm. enkefaliitti, myeliitti) suositellaan kuitenkin suoneen annettavaa keftriaksonia.
Doksisykliiniä voidaan käyttää joko annoksella 100 mg kahdesti päivässä tai 200 mg kerran päivässä. Keftriaksonin annostus suoneen neuroborrelioosin hoidossa on 2 g kerran päivässä. Amoksisilliini läpäisee veri-aivoesteen huonosti, eikä se siksi sovellu neuroborrelioosin hoitoon.
Suomalaisessa hoitotutkimuksessa satunnaistettiin 210 potilasta, joilla epäiltiin neuroborrelioosia, saamaan joko doksisykliiniä 100 mg kahdesti päivässä suun kautta 4 viikon ajan tai keftriaksonia 2 g kerran päivässä suoneen kolmen viikon ajan (21). Satunnaistetuista potilaista 99:llä oli varma neuroborrelioosi ja 88:lla mahdollinen. Laboratoriovastausten valmistumisen jälkeen 23 potilaalla ei lopulta ollutkaan neuroborrelioosia. Potilaat arvioivat vointinsa VAS-asteikolla 0–10 (10 = huonoin) ennen hoidon aloitusta sekä 4 ja 12 kuukauden kuluttua hoidon alusta. Molemmissa antibioottihoitoryhmissä potilaat paranivat yhtä hyvin.
Hoidon optimaalisesta kestosta ei toistaiseksi ole julkaistu satunnaistettuja tutkimuksia. Tutkimuksissa hoidon kesto on ollut 10–28 vuorokautta. Yleensä potilaat eivät ole hyötyneet yli 4 viikkoa kestävistä hoidoista (23,24), poikkeuksena Lymen artriittia sairastavat potilaat, joille antibioottihoito voidaan kertaalleen toistaa, mikäli vaste ensimmäiseen hoitoon jää huonoksi (25).
Euroopassa akuutin neuroborrelioosin hoidon kestoksi on suositeltu 14 vuorokautta sekä keftriaksonia että doksisykliiniä käytettäessä (11). Myös suoneen annettava penisilliini ja kefotaksiimi ovat tehokkaita lääkkeitä, mutta niiden käyttö on ollut Suomessa vähäisempää. Myöhäisvaiheen neuroborrelioosissa, oireiden kestettyä yli 6 kuukautta, suositeltu hoidon kesto on 21 vuorokautta (11). Suomessa hoidon pituus on tavallisesti ollut 21–28 vuorokautta oireiston kestosta riippumatta.
Lähiaikoina on valmistumassa satunnaistettu kaksoissokkoutettu tutkimus, jossa verrataan neuroborrelioosipotilaiden 2 viikon ja 6 viikon kestoista doksisykliinihoitoa (26). Tämän tutkimuksen tulos selventänee, hyötyykö potilas yli 2 viikon kestoisesta antibioottihoidosta.
Ennuste
Valtaosa neuroborrelioosin sairastaneista toipuu hyvin. Akuutisti sairaiden kivuliaat radikuliittioireet paranevat varsin hyvin hoidon aikana. Pitkään kestäneiden oireiden poistuminen voi kestää jopa kuukausia, mikä kuvastaa hermoston hidasta paranemista vaurion jälkeen.
Hoidon jälkeen noin 30 % potilaista kokee jälkioireita, joista osa on subjektiivisia oireita, kuten väsymystä ja muistivaikeuksia (27). Tauti voi aiheuttaa pysyviä hermovaurioita, ja niiden riski lisääntyy diagnoosin ja hoidon viivästyessä. Neurologisia löydöksiä on ollut 16 %:lla potilaista vuoden kuluttua hoidon jälkeen (21). Akuutti neuroborrelioosi voi parantua myös spontaanisti; tämä havaittiin ennen hoidon vakiintumista 1980-luvulla (28).
Asianmukaisen antibioottihoidon jälkeen oireilemaan jäävien potilaiden hoito on oireenmukaista. Toistuvista tai pitkittyneistä antibioottikuureista ei ole hyötyä. Mikäli epäillään hoidon epäonnistumista tai uusintainfektiota, tulee aivo-selkäydinnestenäyte tutkia uudelleen infektion osoittamiseksi sekä arvioida mahdollisten muiden sairauksien osuus oireiden taustalla (29).
Elisa Kortela: Apurahat (Biomedicum Helsinki -säätiö, Suomalainen Lääkäriseura Duodecim), matka- ja majoituskulut (MSD Finland).
Jukka Hytönen: Konsultointipalkkiot (Labquality, Reagena), apurahat laitokselle (Suomen Akatemia, Business Finland, Jane ja Aatos Erkon säätiö, Valtion tutkimusrahoitus), luentopalkkiot (Labquality).
Jarmo Oksi: Konsultointipalkkiot (GlaxoSmithKline, MSD Finland, Roche, TerveMedia Oy), luentopalkkiot (Biocodex, GlaxoSmithKline, MSD Finland, Orion Pharma), matka-, majoitus ja kokouskulut (Gilead, Grifols, MSD).
Mari Kanerva: Konsultointipalkkio (Pfizer), luentopalkkio (GSK, Orion).
- 1
- Laaksonen M, Klemola T, Feuth E ym. Tick-borne pathogens in Finland: comparison of Ixodes ricinus and I. persulcatus in sympatric and parapatric areas. Parasit Vectors 2018;11(1):556.
- 2
- Wilhelmsson P, Lindblom P, Fryland L, Ernerudh J, Forsberg P, Lindgren PE. Prevalence, diversity, and load of Borrelia species in ticks that have fed on humans in regions of Sweden and Aland Islands, Finland with different Lyme borreliosis incidences. PLoS One 2013;8(11):e81433.
- 3
- Wilhelmsson P, Fryland L, Lindblom P ym. A prospective study on the incidence of Borrelia burgdorferi sensu lato infection after a tick bite in Sweden and on the Aland Islands, Finland (2008-2009). Ticks Tick Borne Dis 2016;7:71–9.
- 4
- Hyde JA. Borrelia burgdorferi keeps moving and carries on: a review of borrelial dissemination and invasion. Front Immunol 2017;8:114.
- 5
- Huppertz HI, Bohme M, Standaert SM, Karch H, Plotkin SA. Incidence of Lyme borreliosis in the Wurzburg region of Germany. Eur J Clin Microbiol Infect Dis 1999;18:697–703.
- 6
- Sajanti E, Virtanen M, Helve O ym. Lyme borreliosis in Finland, 1995-2014. Emerg Infect Dis 2017;23:1282–8.
- 7
- Bacon RM, Kugeler KJ, Mead PS, (CDC) CfDCaP. Surveillance for Lyme disease--United States, 1992-2006. MMWR Surveill Summ 2008;57(10):1–9.
- 8
- THL. Borrelioosin seuranta ja esiintyvyys Suomessa. Terveyden ja hyvinvoinnin laitos 2020 (päivitys 10.6.2020). https://thl.fi/fi/web/infektiotaudit-ja-rokotukset/taudit-ja-torjunta/taudit-ja-taudinaiheuttajat-a-o/borrelia/borrelioosin-seuranta-ja-esiintyvyys-suomessa.
- 9
- Lantos PM, Rumbaugh J, Bockenstedt LK ym; Clinical Practice Guidelines by the Infectious Diseases Society of America (IDSA), American Academy of Neurology (AAN), and American College of Rheumatology (ACR): 2020 Guidelines for the Prevention, Diagnosis and Treatment of Lyme Disease. Clin Infect Dis 2021;72:1–8.
- 10
- Harms MG, Hofhuis A, Sprong H ym. A single dose of doxycycline after an ixodes ricinus tick bite to prevent Lyme borreliosis: An open-label randomized controlled trial. J Infect 2021;82:98–104.
- 11
- Mygland A, Ljøstad U, Fingerle V ym. EFNS guidelines on the diagnosis and management of European Lyme neuroborreliosis. Eur J Neurol 2010;17:8–16, e1–4.
- 12
- Ogrinc K, Lusa L, Lotrič-Furlan S ym. Course and outcome of early European Lyme neuroborreliosis (Bannwarth syndrome): clinical and laboratory findings. Clin Infect Dis 2016;63:346–53.
- 13
- Mygland A, Skarpaas T, Ljøstad U. Chronic polyneuropathy and Lyme disease. Eur J Neurol 2006;13:1213–5.
- 14
- Gade A, Matin T, Rubenstein R, Hardin CA. Acrodermatitis Chronica Atrophicans. Treasure Island (FL): StatPearls Publishing 2021.
- 15
- Lindland ES, Solheim AM, Andreassen S ym. Imaging in Lyme neuroborreliosis. Insights Imaging 2018;9:833–44.
- 16
- Dessau RB, van Dam AP, Fingerle V ym. To test or not to test? Laboratory support for the diagnosis of Lyme borreliosis: a position paper of ESGBOR, the ESCMID study group for Lyme borreliosis. Clin Microbiol Infect 2018;24:118–24.
- 17
- van Beek J, Sajanti E, Helve O ym. Population-based Borrelia burgdorferi sensu lato seroprevalence and associated risk factors in Finland. Ticks Tick Borne Dis 2018;9:275–80.
- 18
- Rupprecht TA, Manz KM, Fingerle V ym. Diagnostic value of cerebrospinal fluid CXCL13 for acute Lyme neuroborreliosis. A systematic review and meta-analysis. Clin Microbiol Infect 2018;24:1234–40.
- 19
- Wutte N, Berghold A, Löffler S ym. CXCL13 chemokine in pediatric and adult neuroborreliosis. Acta Neurol Scand 2011;124:321–8.
- 20
- Ljøstad U, Skogvoll E, Eikeland R ym. Oral doxycycline versus intravenous ceftriaxone for European Lyme neuroborreliosis: a multicentre, non-inferiority, double-blind, randomised trial. Lancet Neurol 2008;7:690–5.
- 21
- Kortela E, Kanerva MJ, Puustinen J ym. Oral doxycycline compared to intravenous ceftriaxone in the treatment of Lyme neuroborreliosis: a multicentre, equivalence, randomized, open-label trial. Clin Infect Dis 2021;72:1323–31.
- 22
- Bremell D, Dotevall L. Oral doxycycline for Lyme neuroborreliosis with symptoms of encephalitis, myelitis, vasculitis or intracranial hypertension. Eur J Neurol 2014;21:1162–7.
- 23
- Oksi J, Nikoskelainen J, Hiekkanen H ym. Duration of antibiotic treatment in disseminated Lyme borreliosis: a double-blind, randomized, placebo-controlled, multicenter clinical study. Eur J Clin Microbiol Infect Dis 2007;26:571–81.
- 24
- Berende A, ter Hofstede HJ, Vos FJ ym. Randomized trial of longer-term therapy for symptoms attributed to Lyme disease. N Engl J Med 2016;374:1209–20.
- 25
- Arvikar SL, Steere AC. Diagnosis and treatment of Lyme arthritis. Infect Dis Clin North Am 2015;29:269–80.
- 26
- Solheim AM, Ljostad U, Mygland A. Six versus two weeks treatment with doxycycline in Lyme neuroborreliosis: the protocol of a multicentre, non-inferiority, double-blinded and randomised controlled trial. BMJ Open 2019;9(6):e027083.
- 27
- Dersch R, Sommer H, Rauer S, Meerpohl JJ. Prevalence and spectrum of residual symptoms in Lyme neuroborreliosis after pharmacological treatment: a systematic review. J Neurol 2016;263:17–24.
- 28
- Kruger H, Reuss K, Pulz M ym. Meningoradiculitis and encephalomyelitis due to Borrelia burgdorferi: a follow-up study of 72 patients over 27 years. J Neurol 1989;236:322–8.
- 29
- Kullberg BJ, Vrijmoeth HD, van de Schoor F, Hovius JW. Lyme borreliosis: diagnosis and management. BMJ 2020;369:m1041.
Lyme neuroborreliosis: manifestations, diagnostics and treatment
Lyme borreliosis is caused by spirochetes of the Borrelia burgdorferi sensu lato complex (hereinafter borrelia), which are transmitted to humans by ticks of the genus Ixodes. Approximately 3–12% of patients with Lyme borreliosis will develop neurological symptoms. The most typical presentations of acute Lyme neuroborreliosis are painful meningoradiculitis (Bannwarth syndrome), facial nerve palsy and lymphocytic meningitis. Besides the facial nerve, any other cranial or peripheral nerve may be involved. Patients with acute neuroborreliosis often also have non-specific symptoms such as headache, neck stiffness, or myalgia. Parenchymal central nervous system manifestations, such as encephalitis or myelitis, are rare. Late neuroborreliosis, with a symptom duration of more than six months, may manifest as mononeuropathy, radiculopathy, polyneuropathy with a skin manifestation called acrodermatitis chronica atrophicans, encephalitis, or cerebral vasculitis.
Diagnosis of neuroborreliosis relies on serology and analysis of cerebrospinal fluid. The diagnosis of definite neuroborreliosis is based on neurological symptoms suggestive of neuroborreliosis in the absence of other obvious causes, cerebrospinal fluid lymphocytic pleocytosis, and intrathecal borrelia-specific antibody production. Demonstration of increased cerebrospinal fluid CXCL13 concentration is a useful indicator of acute neuroborreliosis during the time interval before antibody production starts.
Acute neuroborreliosis may be treated with oral doxycycline 100 mg twice a day for 14–28 days or intravenous ceftriaxone 2 g daily for 14–21 days. If symptoms have lasted for more than six months, the recommended duration of antimicrobial treatment is 21–28 days. In the case of parenchymal central nervous system manifestations, ceftriaxone is recommended for the treatment. Most patients with neuroborreliosis will have a prompt recovery within weeks to months after appropriate therapy.