Polio on vihdoinkin häviämässä maailmasta – vai onko sittenkään?
Tehokkaiden rokotusten ansiosta polio on häviämässä koko maailmasta. Suomessa tautia todettiin viimeksi vuonna 1985.
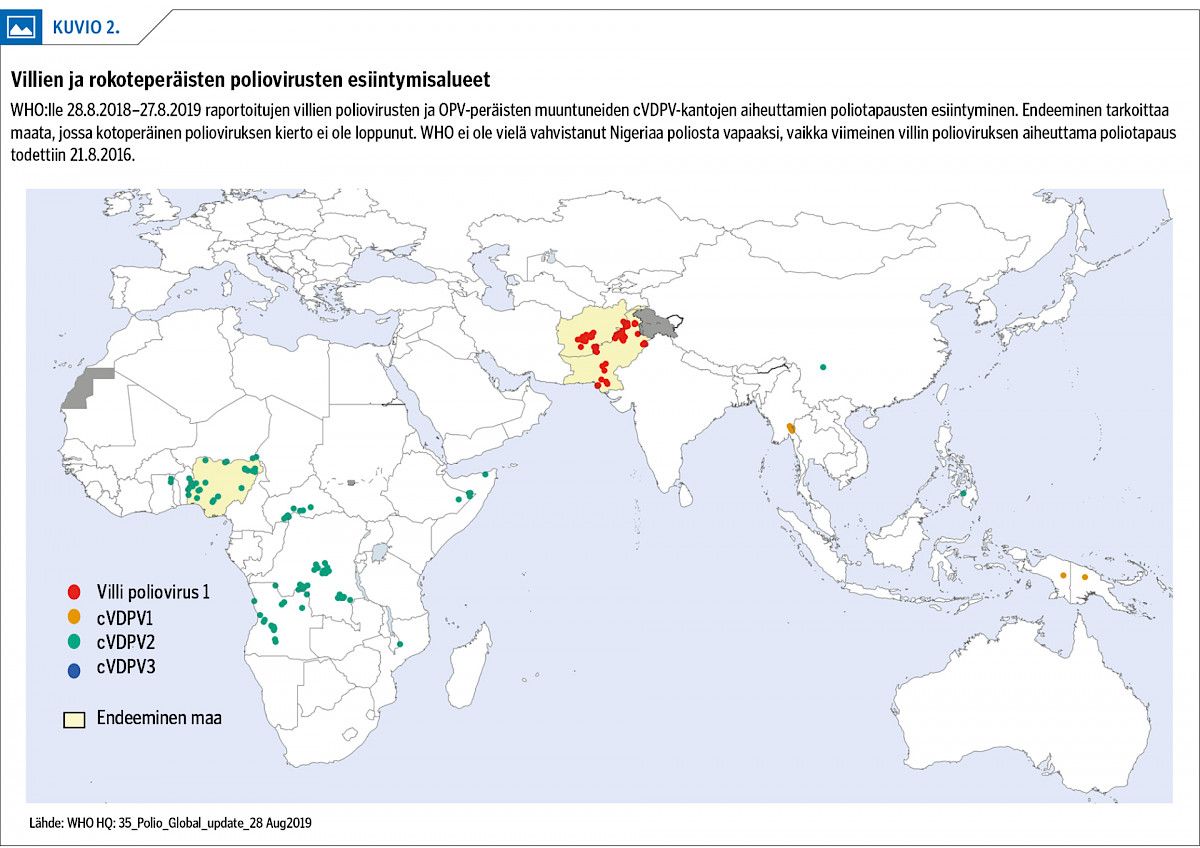
Luonnonmukainen eli villi tyypin 1 poliovirus on viime vuosina aiheuttanut enää muutamia kymmeniä poliotapauksia Afganistanissa ja Pakistanissa.
Uudeksi ongelmaksi ovat ilmaantuneet muuntuneiden rokotevirusten aiheuttamat polioepidemiat alueilla, joilla rokotuskattavuus oli heikentynyt.

Polio eli lapsihalvaus on häviämässä ihmiskunnasta sinnikkään kansainvälisen yhteistyöohjelman ansiosta. Poliovirustartunnan saaneista pienellä osalla (1–0,1 %) virus pääsee suoliston limakalvolta imusuoniin ja verenkiertoon ja sieltä edelleen keskushermostoon aiheuttaen vammauttavan neurologisen taudin. Viruksen mielipaikkoja ovat selkäytimen etusarven motoriset neuronit, joiden tuho johtaa vastaavien lihassäikeiden halvaantumiseen.
Halvausoireisen taudin voi aiheuttaa mikä tahansa polioviruksen kolmesta serotyypistä. Taudin torjumiseksi kehitettiin kaksikin rokotetta jo kuusi vuosikymmentä sitten: Salkin inaktivoitu poliovirusrokote (IPV) ja Sabinin oraalinen, eläviä heikennettyjä viruksia sisältävä poliorokote (OPV).
Koko maailmaa koskevasta polionhävitysohjelmasta (Global Polio Eradication Initiative, GPEI) sovittiin WHO:n jäsenvaltioiden kesken vuonna 1988 (1). Kansainvälisen ohjelman johtotiimin muodostivat WHO, UNICEF, Rotary International ja Yhdysvaltain tartuntatautien seurantakeskus CDC. Ohjelma käytti alun perin yksinomaan oraalista rokotetta väestön immunisointiin.
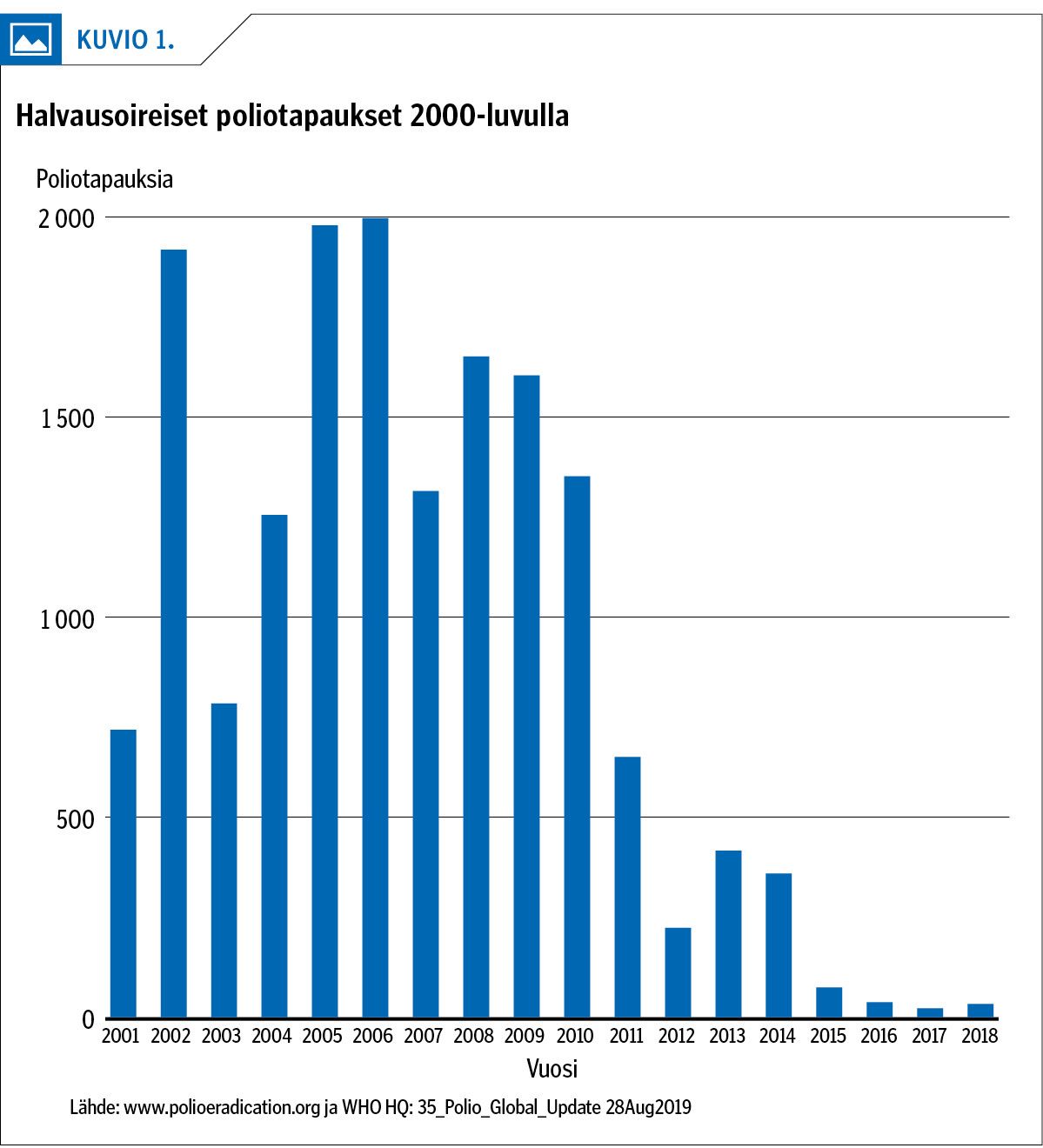
Alkuperäisenä tavoitteena oli hävittää polio ihmiskunnasta vuoteen 2000 mennessä. Alku näyttikin hyvältä: 10 vuoden kuluessa taudin ilmaantuminen maailmassa väheni yli 99 % ja esiintymisalue supistui kaikista maanosista Afrikkaan, Lähi-itään ja Etelä-Aasiaan. Tämän jälkeen erilaiset takaiskut ja operatiiviset ongelmat monissa kehittyvissä maissa pysäyttivät menestystarinan, ja seuraavan vuosikymmenen aikana uusia sairastumisia diagnosoitiin vuosittain 500–2 000 (2). Uusi jyrkkä lasku tapausten ilmaantumisessa alkoi vuonna 2009 (kuvio 1).
Polionhävitysohjelma nyt
Viime aikoina uusien tapausten esiintyminen on rajoittunut Afganistaniin ja Pakistaniin (kuvio 2). Uusien tapausten määrä kääntyi taas kasvuun vuonna 2018, ja marraskuun alkuun mennessä vuonna 2019 on raportoitu jo lähes 100 uutta poliotapausta (2).
Nykyajan liikkuva elämäntapa ja monissa maissa hauras laumaimmuniteetti väestössä mahdollistavat viruksen leviämisen oireettomien kantajien mukana. Näin tauti voi palata maihin, joissa viruksen kotoperäinen kierto on jo saatu loppumaan. Kun sisällissota murensi lasten rokotusohjelman Syyriassa vuonna 2013, syntyi polioepidemia (3). Tuorein esimerkki on huhtikuulta 2019, jolloin luonnonmukainen, villi tyypin 1 poliovirus löytyi jätevedestä Iranissa (4).
Polio on yhä WHO:n luokittelun mukaan kansainvälinen terveysuhka. Jäsenmailta edellytetään yksityiskohtaista toimintasuunnitelmaa mahdollisen polioepidemian varalle (5). Poliorokotteen tehosteannosta suositellaan Afganistaniin ja Pakistaniin matkustaville ja matkan suuntautuessa eräisiin muihin maihin, joissa poliota on esiintynyt äskettäin tai joissa tartuntariskin arvellaan muuten olevan erityisen suuri (6).
Vuosituhannen vaihteessa uudeksi ongelmaksi ilmaantuivat väestössä kiertävien oraalisesta rokotteesta peräisin olevien, muuntuneiden rokotevirusten (circulating vaccine-derived poliovirus, cVDPV) aiheuttamat polioepidemiat alueilla, joilla rokotuskattavuus oli heikentynyt (7). Niitä esiintyy edelleen (taulukko 1) (2). Tästä syystä eradikaatio-ohjelma pyrkii asteittain eroon oraalisen rokotteen käytöstä.
Tyypin 2 elävän viruksen käyttö lasten perusrokotuksissa lopetettiin maailmanlaajuisesti vuonna 2016. Se ei kuitenkaan lopettanut muuntuneiden tyypin 2 rokotevirusten aiheuttamia epidemioita (2). Niinpä tyypin 3 elävän rokoteviruksen käytön lopettamisessa ei hätäillä, vaikka villi tyypin 3 poliovirus julistettiin hävitetyksi 17.10.2019. Tyypin 1 elävän viruksen käyttö rokotteessa on välttämätöntä niin kauan kuin villi tyypin 1 virus kiertää ihmisissä. Oraalisen rokotteen valmistaminen on halvempaa kuin inaktivoitua virusta sisältävän, ja annostelu on helpompaa ja turvallisempaa, kun ruiskuja ja neuloja ei tarvita. Oraalisen rokotteen teho poliovirustartuntaa vastaan on myös parempi. Inaktivoitu rokotekin toki antaa täyden suojan poliotautia vastaan.
Polionhävitysohjelman loppukiriä Afganistanissa ja Pakistanissa on vaikeuttanut rokottajien turvallisuuden heikentyminen. Poliorokottajiksi tekeytyneiden CIA:n agenttien toteuttama Osama bin Ladenin piilopaikan paljastaminen ja murha vuonna 2011 laukaisivat koston kierteen, jonka aikana useampi oikea rokottaja on saanut surmansa. Haasteista huolimatta ohjelma pyrkii intensiivisesti pysäyttämään viruksen kierron viimeisissäkin pesäkkeissä.
Mihin tieto polion ja poliovirusten häviämisestä perustuu?
Polionhävitysohjelma edellyttää jokaiselta WHO:n jäsenvaltiolta vuosittain kansallisesta seurantajärjestelmästä riippumattoman asiantuntijaryhmän (National Certification Committee, NCC) raportin polioon sairastuneista ja muista poliovirushavainnoista sekä itsenäisen arvion siitä, olisiko maan seurantajärjestelmä havainnut, jos väestössä olisi edellisen kalenterivuoden aikana kiertänyt villi poliovirus tai muuntunut rokotevirus. Kansalliset raportit tarkastaa ja niiden luotettavuuden arvioi alueellinen asiantuntijaryhmä (Regional Certification Commission, RCC).
Kansallisen asiantuntijaryhmän lausunnon perustana olevat numerotiedot rokotuskattavuudesta ja seurannan havainnoista saadaan kansallisten toimijoiden, kuten THL:n, tilastoista.
Kansallisten raporttien perusteella Euroopan alueen asiantuntijaryhmä (EURO-RCC-Polio) on viime aikoina jakanut alueensa maat kolmeen luokkaan polion paluuriskin suhteen: vähäisen, kohtalaisen ja suuren riskin maihin. Arvioitua riskiä lisäävät rokotuskattavuuden vajavuudet, seurantajärjestelmän otaksutut heikkoudet ja muut tekijät, kuten kansallinen suunnitelma polioepidemian varalta ja selvitys maan laboratorioissa säilytettyjen polioviruskantojen ja niitä mahdollisesti sisältävien kliinisten tai ympäristönäytteiden turvallisuusriskeistä.
Viime vuosina suuren riskin maita Euroopassa ovat olleet Ukraina, Bosnia-Hertsegovina ja Romania. Reilu kolmannes WHO:n Euroopan alueen jäsenmaista on luokiteltu kohtalaisen riskin maiksi (8).
Rokotuskattavuustiedot
Rokotuksista kysytään yleistä rokotuskattavuutta (WHO:n suositus vähintään 3 annosta 12 kk:n ikään mennessä), alueellisia eroja ja toteutettuja kampanjoita ja niiden kattavuutta. Rokotuskattavuustiedoissa voi olla monenlaisia ongelmia mm. siksi, että väestönlaskentaa ei kaikissa maissa tehdä joka vuosi eikä syntyvien lasten määrää seurata keskitetysti. Kattavuustietojen hankintaperiaatteet ja luotettavuuden arviointi vaihtelevat suuresti maittain. Tietoja on erityisen vaikeaa saada pakolaisista, turvapaikanhakijoista ja syrjityistä tai muutoin vaikeasti tavoitettavista vähemmistöistä.
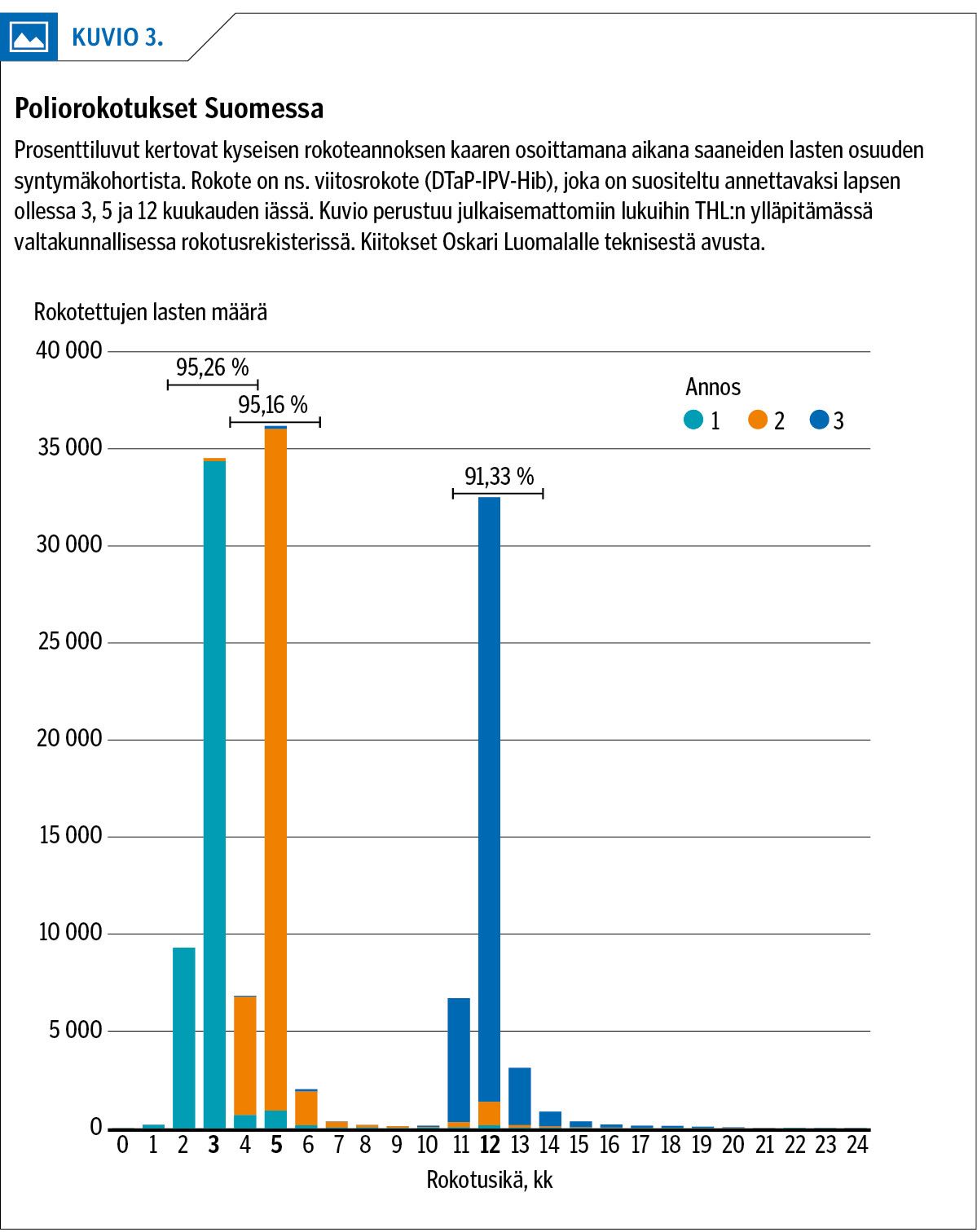
Euroopan alueen asiantuntijaryhmä on usein vaatinut lisäselvityksiä ennen lopullista kannanottoaan maan rokotuskattavuudesta. Inaktivoidun rokotteen saatavuusongelmat, byrokratia rokotteiden hankinnassa, maan poliittisten olojen sekavuus ja resurssipula vaivaavat monia maita myös Euroopassa. Kolmen annoksen rokotuskattavuuden jääminen koko maassa alle 95 %:iin tai useilla maan alueilla alle 90 %:iin on tavallisin syy sijoittumiseen kohtalaisen riskin luokkaan. Tästä syystä Suomikin on kuulunut tähän joukkoon viime vuosina (kuvio 3).
AFP-seuranta
Polion seurantatiedot voivat perustua joko polion kaltaisten tapausten etiologian selvittämiseen tai suoraan polioviruksen etsimiseen eri lähteistä.
Suomessa ja monessa muussa maassa tartuntatauteja koskeva lainsäädäntö velvoittaa lääkärin ilmoittamaan polioepäilystä välittömästi kansalliseen seurantakeskukseen. Maassa, jossa poliota ei ole ollut vuosikymmeniin, polion mahdollisuus tulee ymmärrettävästi mieleen vasta, kun oireiston kaikki muut mahdolliset syyt on suljettu pois. Yksittäisen poliotapauksen virusetiologian varmistus voi viivästyä, mutta alueellinen ryvästymä luultavasti alkaisi Suomessakin soittaa hälytyskelloja.
Polionhävitysohjelmalle tällainen passiivinen ilmoitusvelvollisuus ei riitä, vaan kultainen standardi on tautiepäilypohjainen äkillisten velttohalvaustapausten AFP-seuranta (acute flaccid paralysis). Jokaisesta alle 15-vuotiaasta äkillisesti velttohalvausoireiseen tautiin sairastuneesta tulee tehdä ilmoitus kansalliseen seurantakeskukseen, ja hänestä tulee ottaa kaksi ulostenäytettä vähintään 24 tunnin välein, ennen kuin taudin alusta on kulunut 14 vrk. Näytteet tulee toimittaa kylmäketjussa WHO:n akkreditoimaan viruslaboratorioon, jossa niistä etsitään polioviruksia tarkan protokollan mukaan. Tämä ohje sopii käytännöksi myös Suomessa polioepäilyn syntyessä (5).
Jos villejä polioviruksia tai muuntuneita rokotekantoja ei löydy, tulos kelpaa näytöksi siitä, että poliota ei esiinny, mikäli näin tutkittuja alle 15-vuotiaita velttohalvauspotilaita on ollut vuodessa vähintään 1/100 000 kohdeväestössä. Näin paljon katsotaan ilmenevän muista syistä syntyviä velttohalvausoireisia sairastumisia vuosittain.
AFP-seuranta on toiminut hyvin monissa maissa, joissa se käynnistettiin ns. kotoperäisen polioviruskierron aikana. Vaikka polionhävitysohjelman viivästyminen onkin aiheuttanut ymmärrettävää peliväsymystä monissa maissa, koko maailmaa koskevat AFP-seurantamittarit näyttävät yhä vakuuttavilta: äkillisen velttohalvauksen vuoksi tutkittujen tautiepäilyjen määrä on kasvanut vuosituhannen alusta kolminkertaiseksi. Vuonna 2018 tapauksia tutkittiin yli 96 000.
Tämä ei kuitenkaan ole koko totuus. Maissa, joissa poliota ei ole todettu vuosiin, löysä velttohalvausoirediagnoosi ei ole innostanut kliinikoita eikä terveydenhoitojärjestelmiä, jotka ovat tottuneet etsimään täsmällisempiä neurologisia oireyhtymiä, Guillain–Barrén oireyhtymää ym. Niinpä Suomessa, muussa läntisessä Euroopassa, Yhdysvalloissa ja monessa muussa maassa AFP-seurantaa ei joko yritettykään käynnistää tai se ei päässyt lähellekään laadukkuuden raja-arvoa (1/100 000 lasta).
AFP-seurannan paras ominaisuus on, että se voidaan ulottaa periaatteessa koko väestöön maassa kuin maassa. Spontaania primaariraportointia voidaan tarkentaa sairaaloiden potilaskertomuksista. Suurin ongelma on lähtökohdan, äkillisesti alkavan velttohalvauksen, epämääräisyys.
Lisääntyneen polioriskin alueilla AFP-seurantaa on WHO:n kehotuksesta tehostettu ja saatu tutkimuksiin jopa 3/100 000 lasta vuosittain. Hyvä kun tutkitaan, mutta herää kysymys, kuinka paljon seula vuotaa, kun hyvän laadun kriteeriksi hyväksytään 1/100 000.
WHO:n perinteisen kannan mukaan AFP-seuranta kyllä paljastaa uudelleenkin alkaneen polioviruskierron, koska ennen pitkää ilmaantuvat ensimmäiset halvauspotilaat. Nykynäkemys on, että tosielämässä asia ei aina ole näin suoraviivainen. Tälle saatiin lisätukea vuonna 2013, kun Israelin palestiinalaisalueilla löytyi villejä tyypin 1 viruksia jätevesistä melkein vuoden ajan, mutta edes tehostettu AFP-seuranta ei löytänyt yhtään poliovirusta erittävää potilasta. Israel oli joitakin vuosia aiemmin siirtynyt pelkän inaktivoidun rokotteen käyttöön. Viruskierron lopettamiseksi toteutettiin kaksi oraalista rokotuskampanjaa. Jätevesilöydökset loppuivat, vaikka kampanjojen kattavuus oli kaukana tavoitellusta (9).
Polioviruskierron seuranta
Jokaista polioon sairastunutta henkilöä kohti ympäröivässä väestössä voi olla satoja, rokotetussa väestössä tuhansia oireettomia henkilöitä, jotka erittävät virusta ulosteisiinsa viikkokausia. Polionhävitysohjelman terminologiassa suoraan viruksiin kohdistuva seuranta on lisäseurantaa (supplementary surveillance) tai täydentävää seurantaa (complementary surveillance). Polioviruskierron suora seuranta kuulostaa loogiselta, mutta senkään tulosten tulkinta ei ole ongelmatonta.
Enterovirusseurannaksi sanotaan enterovirusinfektioiden rutiinidagnostiikan löydösten keräämistä ja analyysiä poliovirusten löytämiseksi. Alkuperäisenä ajatuksena on ollut kattaa seurannalla neurologisia infektioita sairastavat potilaat; heistähän usein etsitään mm. enteroviruksia.
Poliovirusseurannan herkkyyden kannalta tähän lähestymistapaan liittyy kuitenkin useita teoreettisia ja käytännön ongelmia. Harvassa maassa virusdiagnostiikkaa tehdään tasaisesti läpi koko väestön syrjäseutuja myöten. Enterovirusinfektioiden vuosittain vaihteleva ilmaantuminen tekee mahdottomaksi sen kaltaisen laatukriteerin kuin 1/100 000 AFP-potilasta.
Sitä paitsi poliovirus kyllä aiheuttaa joskus aivokalvotulehdusta, mutta silloinkaan sitä ei yleensä löydy likvorista. Tavallinen enterovirus-PCR ei erottele polioviruksia muista enteroviruksista. Nämä ongelmat voidaan toki korjata, jos likvorin enterovirus-PCR-löydöksen ollessa positiivinen tehdään ulostenäytteen soluviljely polioviruksen suhteen. Harvassa maassa tähän kuitenkaan pystytään systemaattisesti ja kattavasti.
Käytännössä Euroopan alueen asiantuntijaryhmä on hyväksynyt enterovirusseurannan tulokset yhdeksi perusteeksi sille, että poliota ei esiinny maassa, jos riittäväksi katsottu määrä (väestön koosta riippuen) ulostenäytteitä on tutkittu soluviljelmissä ja kohtalaisesta osasta niistä on löydetty muita enteroviruksia kuin polioviruksia.
Polioviruksen etsiminen jätevesistä on ollut Suomessa keskeinen seurantamenetelmä jo vuosikymmenien ajan (Liite 1 artikkelin sähköisessä versiossa, www.laakarilehti.fi > Sisällysluettelot > 49/2019). Viime vuosina myös polionhävitysohjelma on ryhtynyt käyttämään sitä yhä laajemmin lisäseurantamenetelmänä kaikkialla maailmassa.
Poliovirukset joutuvat viemäriverkostoon ulosteiden mukana, ja ottamalla näytteitä suurten kaupunkien jätevedenpuhdistamoilta voidaan seurata suurtenkin väestöryhmien viruseritystä. Viruspitoisuus laimenee viemäriverkostossa niiden ihmisten vesiosuuksilla, jotka eivät eritä poliovirusta. Niinpä jätevesinäyte pitää väkevöidä virusten osoittamiseksi. Tähän tarkoitukseen on useita menetelmiä, joista yksi yleisimmistä on Suomessa alun perin kehitetty ja validoitu ns. kaksikerrosmenetelmä (Liite 1) (10). Viime vuosina jätevesitutkimuksia – ilman viemäriverkostoakin – on käytetty sujuvasti Afganistanissa, Pakistanissa, Nigeriassa ja monessa muussa kehittyvässä maassa. Näin on saatu tietoa polioviruksen esiintymisestä alueilla, joilla ei ole raportoitu polioon sairastuneita (11).
Jätevesitutkimuksia ei voi toteuttaa missään koko väestön kattavana AFP-seurannan tapaan. Vaikka maassa olisi kattava viemäriverkosto, on sellaisen jatkuva kattava seuranta työlästä ja kallista, sillä näytteet tutkitaan edelleen soluviljelmissä. Muussa virusdiagnostiikassa viljelyn syrjäyttäneiden PCR-menetelmien soveltaminen tähän näytemateriaaliin ei ole onnistunut riittävällä herkkyydellä. Menetelmäkehitys (12,13) saattaa muuttaa tilannetta tulevaisuudessa.
Joka tapauksessa näytteenottokohdat täytyy valita huolellisesti panos-hyötyarvioinnin perusteella ja näytemäärää on säädeltävä resurssien määräämissä rajoissa. Ensisijaisia näytteenottokohteita ovat väestöryhmät, joissa äskettäin on todettu villejä polioviruksia tai rokoteperäisiä kantoja tai joissa rokotuskattavuus on heikentynyt. Lisäksi tärkeitä ovat väestöryhmät, joilla on kontakteja sellaiseen väestöryhmään, jossa esiintyy yhä polioviruskiertoa.
Euroopan alueen asiantuntijaryhmä EURO-NCC-Polio ottaa jätevesitutkimusten tulokset huomioon kansallisia seurantaraportteja arvioidessaan samalla lailla kuin enterovirusseurannan tulokset. Näytteiden tulee kattaa merkittävä osa väestöstä ja huomattavasta osasta tulee löytyä muita enteroviruksia. Jos villejä polioviruksia tai rokoteperäisiä kantoja löytyy jätevesistä, on selvää, että viruksia kiertää vastaavalla alueella myös ihmisissä. Kielteistä tulosta on sen sijaan vaikeaa tulkita. Tarkkoja laatukriteerejä ei ole voitu asettaa.
Suomessa seuranta kattaa noin kolmasosan väestöstä ja muita enteroviruksia löytyy lähes jokaisesta näytteestä. Näytteenottopaikkojen valintakriteereinä ovat väestötiheys (suurimmat kaupungit), kansainvälisen liikenteen solmukohdat ja turvapaikanhakijoiden vastaanottokeskukset paikkakunnalla; näytteenottopaikat ovat Helsinki, Espoo, Turku, Tampere ja Rovaniemi. Seurannan laadukkuutta osoittaa myös se, että jätevesistä löytyy lähes joka vuosi myös yksittäisiä oraalisesta OPV-rokotteesta peräisin olevia polioviruksia (ns. Sabin-kantoja), vaikka meillä tätä rokotetta ei käytetä (Liitetaulukko 1).
Jätevesistä on myös löytynyt Suomessa (14) ja muissakin maissa (15,16,17) samantapaisesti pitkälle muuntuneita OPV-rokoteperäisiä viruksia (aVDPV) kuin mitä tiedetään syntyvän immuunipuutteisilla henkilöillä kroonisissa tai pitkittyneissä infektioissa (iVDPV). Suomessa tällainen muuntunut, taudinaiheuttamiskykyinen virus löytyi viimeksi Tampereen jätevedestä joulukuussa 2013 (Liitetaulukko 1). Tällaisten aVDPV-kantojen erittäjiä ei ole onnistuttu selvittämään. Pitkittynyt viruseritys ei tiettävästi ole johtanut polioepidemiaan, mutta se on huomioon otettava riski rokottamattomassa väestössä.
Lopuksi
WHO:ta on kritisoitu sekä kansainvälisten että kansallisten resurssien liiallisesta sitomisesta yhteen tautiin keskittyvään vertikaaliseen polionhävitysohjelmaan. Toisaalta ohjelman puitteissa kehittyvissä maissa luotu infrastruktuuri, tiedonkulku- ja materiaalilogistiikkajärjestelyt ja erityisesti hyvin koordinoitu laboratorioverkosto (Global Polio Laboratory Network) ovat sujuvasti hyödynnettävissä myös muiden, varsinkin rokotuksin torjuttavien infektiotautien seurantaan (18).
Kumpaankin poliorokotetyyppiin liittyy näin hävitysohjelman loppuvaiheessa merkittävä turvallisuusriski. Rokoteperäisten virusten riskien välttämiseksi oraalisen OPV-rokotteen viruskantoja on muokattu geneettisesti stabiilimmiksi, mutta uusien rokotekandidaattien paremman turvallisuuden dokumentointi on käytännössä mahdotonta tutkimuksen keinoin, kun tauti on lähes kokonaan hävinnyt. Inaktivoidut IPV-rokotteet ovat turvallisia, mutta niiden tuotannossa käytetään yhä villejä viruksia, ja vaarana on niiden karkaaminen tuotantolaitoksista väestöön inhimillisten virheiden vuoksi (19). Näiden viruskantojen korvaaminen kesytetyillä viruksilla on todennäköistä, ennen kuin IPV:n käytöstä ehkä joskus kaukana tulevaisuudessa luovutaan.
Polionhävitysohjelma on lähempänä onnistumistaan kuin koskaan aikaisemmin, mutta ei vielä maalissa. Varmaa tietoa siitä, että villejä tai rokoteperäisiä muuntuneita viruksia ei ole muualla kuin niissä muutamassa maassa, joissa niiden yhä tiedetään kiertävän, on käytännössä mahdotonta saada seurantamenetelmien havaitsemisherkkyyden ja väestötason kattavuuden rajoitusten takia.
Uskoa kielteisiltä näyttäviin tuloksiin vahvistaa vain aika. WHO:n perinteisen tulkinnan mukaan alue voidaan julistaa poliosta vapaaksi, kun AFP-seurannassa viimeisestä halvausoireisen potilaan polioviruslöydöksestä on kulunut kolme vuotta ilman virushavaintoja. Enterovirus- ja jätevesiseurantojen väestötason kattavuus on aina vajavainen, joten vain niihin perustuva näyttö polioviruksen poissaolosta vaatii vielä pitemmän seuranta-ajan. Tämän epävarmuuden kanssa meidän on elettävä.
Tapani Hovi: WHO:n Euroopan alueen Certification of Eradication of Poliomyelitis’ -asiantuntijaryhmän jäsen.
Hanna Nohynek, Carita Savolainen-Kopra: THL:n tutkimusyhteistyö rokotevalmistajien kanssa (GSK, Pfizer).
Soile Blomqvist: Ei sidonnaisuuksia.
- 1
- WHO. Global eradication of poliomyelitis by the year 2000. Geneve: World Health Organization, 1988 WHA41.28.
- 2
- www.polioeradication.org
- 3
- Mbaeyi C, Ryan MJ, Smith P ym. Response to a large polio outbreak in a setting of conflict - Middle East. MMWR Morb Mortal Wkly Rep 2017;66:227–31.
- 4
- http://polioeradication.org/where-we-work/iran/
- 5
- Savolainen-Kopra C, Blomqvist S, Nohynek H, Salminen M, Tiittala P. Kansallinen valmiussuunnitelma polion paluun torjumiseksi 2018-2020. THL 2018. http://urn.fi/URN:ISBN:978-952-343-106-5
- 6
- https://thl.fi/sv/web/rokottaminen/rokotteet/poliorokote/poliorokotukset-riskimaista-saapuville-ja-lahipiirille
- 7
- Kew O, Morris-Glasgow V, Landaverde M ym. Outbreak of poliomyelitis in Hispaniola associated with circulating type 1 vaccine-derived poliovirus. Science 2002;296:356–9.
- 8
- 32nd Meeting o f-the European Regional Commission for Certification of Poliomyelitis Eeradication RCC Rreport 2018. http://www.euro.who.int/en/health-topics/communicable-diseases/poliomyelitis/publications
- 9
- Kaliner E, Kopel E, Anis E ym. The Israeli public health response to wild poliovirus importation. Lancet Infect Dis 2015;15:1236–42.
- 10
- Poyry T, Stenvik M, Hovi T. Viruses in sewage waters during and after a poliomyelitis outbreak and subsequent nationwide oral poliovirus vaccination campaign in Finland. Appl Environ Microbiol 1988;54:371–4.
- 11
- Cowger TL, Burns CC, Sharif S ym. The role of supplementary environmental surveillance to complement acute flaccid paralysis surveillance for wild poliovirus in Pakistan - 2011-2013. PLoS One 2017;12(7):e0180608.
- 12
- Furtak V, Roivainen M, Mirochnichenko O ym. Environmental surveillance of viruses by tangential flow filtration and metagenomic reconstruction. Euro Surveill 2016;21(15). doi: 10.2807/1560-7917.ES.2016.21.15.30193.
- 13
- Hindiyeh MY, Moran-Gilad J, Manor Y ym. Development and validation of a real time quantitative reverse transcription-polymerase chain reaction (qRT-PCR) assay for investigation of wild poliovirus type 1-South Asian (SOAS) strain reintroduced into Israel, 2013 to 2014. Euro Surveill 2014;19(7):20710. Erratum: Euro Surveill 2014;19(8):20717.
- 14
- Roivainen M, Blomqvist S, Al-Hello H ym. Highly divergent neurovirulent vaccine-derived polioviruses of all three serotypes are recurrently detected in Finnish sewage. Euro Surveill. 2010 May 13;15(19):pii/19566.
- 15
- Blomqvist S, Savolainen C, Laine P ym. Characterization of a highly evolved vaccine-derived poliovirus type 3 isolated from sewage in Estonia. J Virol 2004;78:4876–83.
- 16
- Hovi T, Paananen A, Blomqvist S ym. Characteristics of an environmentally monitored prolonged type 2 vaccine derived poliovirus shedding episode that stopped without intervention. PLoS One 2013;8(7).
- 17
- Shulman LM, Manor Y, Sofer D ym. Neurovirulent vaccine-derived polioviruses in sewage from highly immune populations. PLoS One 2006;1:e69.
- 18
- Diop OM KO, de Gourville EM, Pallansch MA. The Global Polio Laboratory Network as a platform for the viral vaccine-preventable and emerging diseases laboratory networks. J Infect Dis 2017;216:S299–307.
- 19
- Duizer E, Ruijs WL, van der Weijden CP, Timen A. Response to a wild poliovirus type 2 (WPV2)-shedding event following accidental exposure to WPV2, the Netherlands, April 2017. Euro Surveill 2017 May 25;22(21). doi: 10.2807/1560-7917.ES.2017.22.21.30542
Poliomyelitis is finally disappearing from the world – or is it?
This review briefly describes the history of poliomyelitis and the progress of the World Health Organization (WHO)-coordinated Global Polio Eradication Initiative established in 1988. Two of the three poliovirus serotypes have been eradicated from circulation in humans, but serotype 1 is still causing disease, albeit with a small number of cases annually and – in recent years – only in Afghanistan and Pakistan. Circulating vaccine-derived polioviruses are now causing more disease than wild ones. However, we still seem to be closer than ever to finally eradicating the disease.
The main topic of this review is a discussion of the reliability of the background information on which the above view is based. Conclusions on the global situation are based on national annual reports on vaccination coverage, polio surveillance, and national preparedness for potential future outbreaks. The reports are critically assessed by so-called regional expert commissions for the certification of poliomyelitis eradication (RCC). This review assesses the strengths and weaknesses of the surveillance methods, the gold standard being acute flaccid paralysis (AFP) surveillance, i.e. search and investigation of suspected clinical cases, as well as supplementary approaches, enterovirus surveillance and environmental surveillance. European RCC experience shows that several countries do have suboptimal vaccination coverage at least in some parts of the country, and weaknesses in the performance of surveillance activities. It is likely that the situation is not much better in the five other WHO Regions. In partially immunized populations, the poliovirus may circulate for long periods without causing typical cases of paralysis. Consequently, wild poliovirus may still hide in some relatively remote populations, with the risk of reemergence of local outbreaks. We will need several years of careful follow-up after the last recognized case to be sure that wild virus circulation has ceased.