Primaarinen sklerosoiva kolangiitti – hepatologian merkittävin haaste
• Primaarinen sklerosoiva kolangiitti (PSC) on sappiteiden krooninen tulehduksellinen sairaus, joka voi johtaa maksakirroosiin ja altistaa merkittävästi sappitie- ja paksusuolen syövälle.
• PSC:n diagnostiikka, seulonta ja seuranta on vaikeaa: hyviä kajoamattomia seulontamenetelmiä ei ole, ja sappitiesyöpäriskin seuranta tulee harkita yksilöllisesti riskitekijöiden perusteella.
• Tautiin on tulossa sen etenemistä estävä ja hidastava lääkehoito.
• Oikein ajoitettu maksansiirto parantaa potilaiden elämänlaatua ja ennustetta ja on ainoa parantava PSC:n hoito.
• Diagnostiikka, hoito ja seuranta kannattaa keskittää.
Primaarinen sklerosoiva kolangiiti (PSC) on krooninen maksan ulkoisia ja sisäisiä sappiteitä ahtauttava tulehduksellinen sappitiesairaus, jonka etiologiaa ei tunneta (1). Pitkälle edettyään se johtaa kirroosiin (1). Krooniseen tulehdukseen liittyvä tauti altistaa sappitiehytkasvaimille eli sappitiesyövälle (kolangiokarsinoomalle) (1). Tavallinen sairastumisikä on 30–40 vuotta, mutta tautia todetaan myös lapsilla (2).
PSC voidaan luokitella joko vain maksan sisäisiä tai useimmiten myös ulkoisia sappiteitä käsittäväksi taudiksi. Osalla potilaista tautiin liittyy autoimmuunimaksatulehdus: aikuisista noin 5 %:lla ja lapsista jopa 50 %:lla. Tällöin PSC-muutosten lisäksi todetaan suuri transaminaasi- ja immunoglobuliini-G-pitoisuus sekä positiiviset sileälihas- tai tumavasta-aineet (2). Noin 60–80 %:lla taustalla on lisäksi tulehduksellinen suolistotauti (IBD), tavallisimmin haavainen paksusuolitulehdus (3). IBD-potilaista 2–10 %:lle kehittyy PSC. Maksasairaus voi ilmaantua jopa vuosia ennen IBD:n puhkeamista, mutta useimmiten vasta sen jälkeen.
Miten tauti todetaan?
PSC todetaan useimmiten oireettomana IBD-potilaalta, jolla on mitattu suurentuneet maksa-arvot, etenkin plasman alkalinen fosfataasi (P-afos) (4) ja lapsilla plasman glutamyylitransferaasi (P-GT) (5). Tauti olisi tärkeää diagnosoida varhain, koska ajoissa aloitettu lääkehoito on tehokkaampi kuin jo runsaiden sappitiehytmuutosten ja maksakirroosin kehityttyä. Taudin varhaistoteaminen on kuitenkin haasteellista. Oireet, kuten vatsakivut, kutina, keltaisuus ja kuumeilujaksot, ovat merkkejä jo pitkälle edenneestä, komplisoituneesta taudista (6). Herkkiä ja spesifisiä verinäytteisiin perustuvia seulontamenetelmiä ei ole, toisin kuin esimerkiksi primaarisella biliaarisella kolangiitilla, jota voidaan seuloa mitokondriovasta-ainetutkimuksella (MitoAb) (6).
Taudin seulontatestinä käytetään P-afos-arvoa (7), vasta-ainetutkimuksia (S-pANCA) (8), maksan ja sappiteiden magneettikuvausta ja magneettikolangiopankreatografiaa (MRCP) (6,9); tavanomaisella magneettikuvauksella selvitetään maksan parenkyymimuutoksia, porttilaskimon tilaa ja poissuljetaan imusolmukesuurentumat, MRCP:llä taas saadaan kolmiulotteinen kuva sappitiepuustosta.
Yleensä P-afos-arvon kasvua on pidetty herkimpänä seulontakriteerinä, mutta normaali pitoisuus ei sulje tautia pois. Jos IBD-potilaan P-afos ja S-pANCA-vasta-aineet ovat suurentuneet, kyseessä on lähes poikkeuksetta PSC (6). S-IgG4-määritys on tarpeen immunoglobuliini G4:ään liittyvän sappitietulehduksen poissulkemiseksi; sen hoito ja seuranta poikkeavat täysin PSC:n hoidosta ja seurannasta.
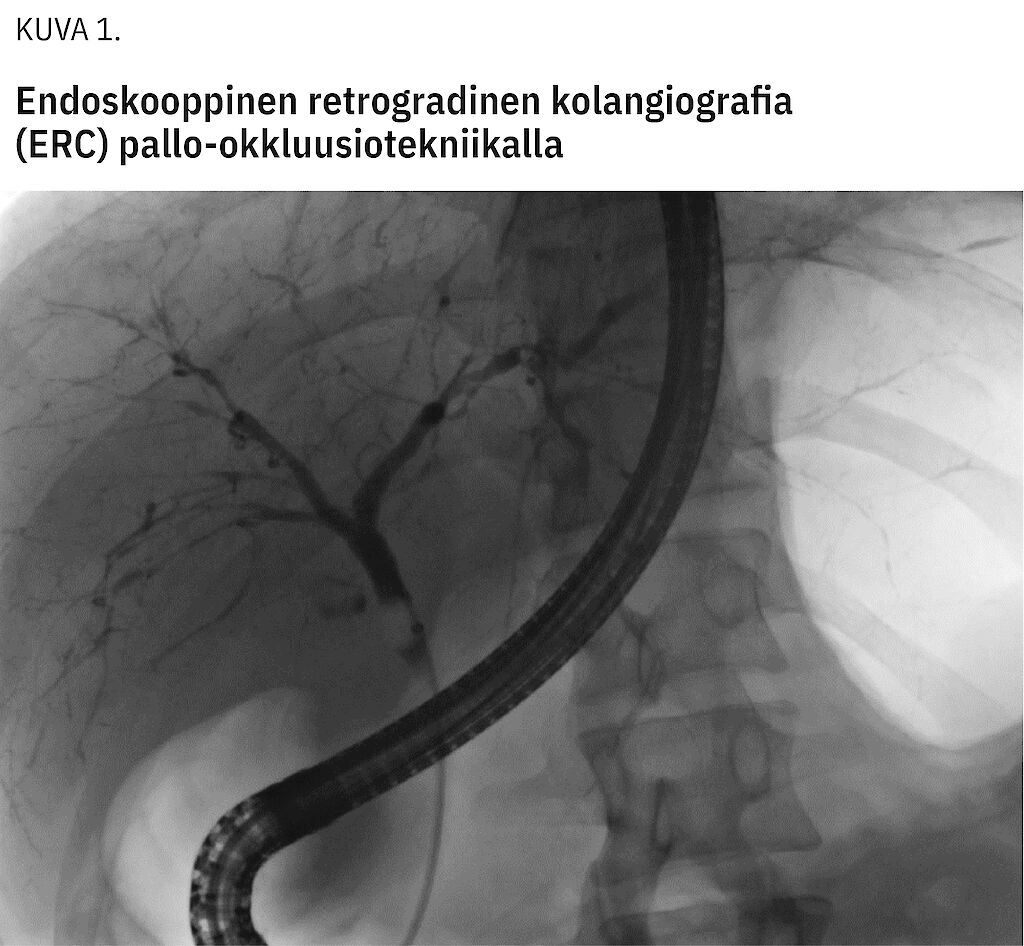
MRCP:n tarkkuus ei riitä taudin varhaismuotojen toteamiseen, ja se tuottaa myös vääriä positiivisia tuloksia (10,11). PSC:n varma diagnoosi perustuukin endoskooppiseen retrogradiseen kolangiografiaan (ERC), jonka avulla voidaan myös ottaa sappiteistä näytteitä ja tehdä toimenpiteitä, kuten laajentaa sappitiehytahtaumia (12,13) (kuva 1). Magneettikuvaus ja MRCP ovat korvanneet ERC:n taudin seulontatutkimuksena siihen liittyvien komplikaatioiden, kuten haima- (4–9 %) ja sappitietulehduksen (2–8 %) vuoksi (14), mutta ERC on kuitenkin tarkempi etenkin maksansisäisten sappitiemuutosten toteamiseen (kuva 1) (15).
Maksan kudosnäytteiden ongelmana on PSC:hen liittyvien muutosten läiskittäisyys, eikä normaali näyte sulje tautia pois. Jopa pitkälle edenneessä sappitietaudissa kudosnäyte saattaa olla vielä normaali (16). Maksabiopsiassa havaitaan tyypillinen löydös, sipulikuorimainen fibroosi, vain 15 %:lla potilaista (16). Liitetaulukossa 1 on esitetty PSC:n erotusdiagnostiikka. Taulukkoon 1 taas on koottu suositeltavat tutkimukset tautia epäiltäessä ja diagnoosivaiheessa.
Kun PSC todetaan eikä potilaalla ole tiedossa olevaa IBD:tä, on paksusuolen tähystys aina aiheen. PSC:hen liittyvä tulehduksellinen suolistosairaus muodostaa oman alatyyppinsä, jota luonnehtii lieväasteinen limakalvotulehdus, koko paksusuolen käsittävä tauti, usein normaali peräsuolen limakalvo ja ohutsuolen loppuosan tulehdus sekä merkittävästi suurentunut syöpäriski (3).
Mikä taudin aiheuttaa?
PSC:n etiologia tunnetaan edelleen huonosti, mutta siihen vaikuttavat sekä perinnölliset että ympäristötekijät (17,18,19,20,21). Syntymekanismista on esitetty neljä eri hypoteesia: PSC:tä on pidetty autoimmuunitautina tai toksisten sappihappojen aiheuttamana sappitiehytvauriona. Taudin läheinen liittyminen tulehduksellisiin suolistosairauksiin on herättänyt hypoteesin ”vuotavasta suolesta” ja mikrobiston osuudesta sen syntyyn ja näiden johtamisesta portaaliseen endotoksemiaan. Neljäntenä hypoteesina PSC:n synnystä on esitetty T-imusolujen poikkeavaa kotiutumista, jolloin tulehtuneessa suolessa aktivoituneet T-solut laukaisevat enterohepaattisessa kierrossa portaalisen tulehduksen. PSC on monitekijäinen tauti, jossa on voimakas HLA-assosiaatio.
Kuinka tavallinen PSC on?
PSC:n ilmaantuvuus vaihtelee voimakkaasti: Norjassa sen ilmaantuvuus on vuodessa 100 000:ta asukasta kohti 1,3 (22), kun taas Alaskassa PSC:tä ei esiinny lainkaan. Kelan erityiskorvattavuustietoihin (202/K83.0) sekä potilasrekisteriin perustuvan tutkimuksen mukaan PSC:n ilmaantuvuus on Suomessa 100 000:ta asukasta kohti 1,29–1,36 ja esiintyvyys 16–32. Ilmaantuvuus on lisääntynyt Suomessa ajan myötä IBD:n tapaan (23). PSC:n esiintyvyyttä IBD-potilailla selvittäneessä tutkimuksessa todettiin magneettikolangiopankreatografian avulla PSC:hen sopivia muutoksia 8,5 %:lla potilaista (24).
PSC:n tavanomainen kulku
PSC saattaa edetä kirroosiin, loppuvaiheen maksasairauteen, ja vaatia maksansiirtoa 20 vuoden kuluessa. Maksasolusyövän riski kirroosipotilailla näyttää olevan pieni (22).
PSC:n vakavin komplikaatio on sappitiesyöpä, joka kehittyy 10–20 %:lle potilaista (22). Sappitiesyövän ennuste on erittäin huono, ja se on PSC-potilaiden tavallisin yksittäinen kuolinsyy. Osalla potilaista se on PSC:n ensioire. PSC lisää sappitiesyövän riskiä merkittävästi, 398-kertaisesti (22). Riski lisääntyy noin 1,5 % sairastamisvuotta kohden (22). PSC:tä sairastavilla IBD-potilailla on viisinkertainen riski sairastua myös paksusuolen karsinoomaan verrattuna potilaisiin, joilla on vain IBD (22).
Miten seurata tautia?
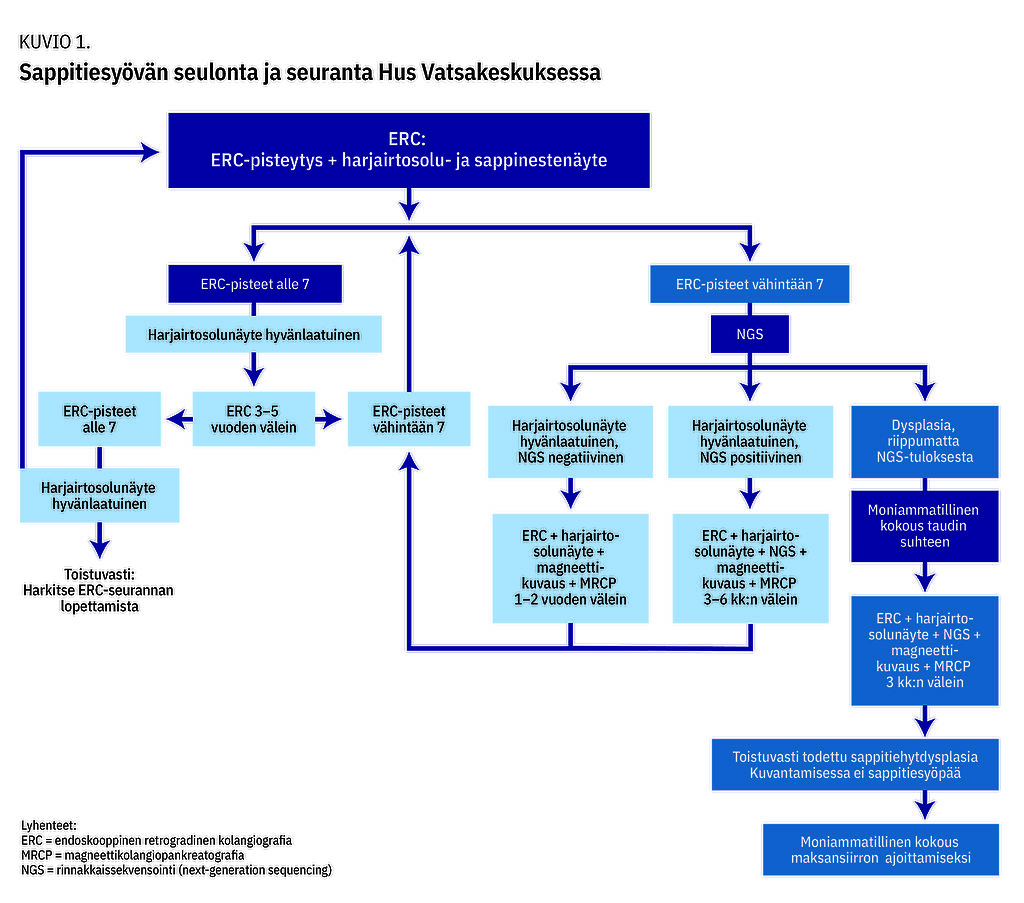
Seuranta kohdistuu sappitiemuutosten etenemiseen, kirroosin ja sen komplikaatioiden kehittymiseen sekä sappitiesyövän varhaistoteamiseen (kuvio 1).
Sappitiemuutosten eteneminen : Perustaudin etenemisen seuranta on hankalaa. P-afos-tasot ovat vaihtelevia ja ennustavat huonosti taudin etenemistä. Tuoreessa tutkimuksessa, jossa analysoitiin eri väestötekijöiden ja laboratorioarvojen merkitystä sappitiemuutosten etenemisen arvioinnissa, todettiin ainoastaan sappitie-epiteelin tulehdusta mittaavien muuttujien interleukiini-8:n ja kalprotektiinin pitoisuuksien sappinesteessä ennustavan taudin etenemistä (25).
Kirroosin kehittymisen suhteen on eniten näyttöä elastografiasta ja fibroosi-indekseistä, kuten Enhanced Liver Fibrosis (ELF) -tutkimuksesta (26).
Sappitiesyövän kehittymisen seuranta on edelleen kiistanalaista ja varhaisdiagnostiikka haastavaa. Oireiden, kuten kipujen, kutinan tai keltaisuuden, nopea paheneminen, yleistilan huononeminen, laihtuminen ja kuumeilu sekä P-afos- ja bilirubiinitasojen ja usein syöpäantigeeni 19-9:n (CA 19-9) pitoisuuksien nopea kasvu viittaavat sappitiesyövän kehittymiseen.
ERC-tutkimuksessa nähtävien striktuurojen erottaminen syöpämuutoksista on mahdotonta ilman solunäytteitä. Sekä eurooppalaisissa että yhdysvaltalaisissa ohjeissa suositellaan magneettikuvausta vuosittain jokaiselle PSC-potilaalle, jolla on suuria sappiteitä käsittävä PSC (27,28). Eurooppalaisissa hoito-ohjeissa ei enää suositella CA 19-9:n seurantaa. Vuosittainen CA 19-9:n mittaus ja magneettikuvaus- ja MRCP-seuranta sekä löydösten perusteella tehtävä ERC-tutkimus ovat kuitenkin osoittautuneet riittämättömiksi sappitiesyövän toteamiseen tarpeeksi ajoissa, jotta sillä olisi ollut vaikutusta potilaiden eloonjäämiseen (29).
Hus Vatsakeskuksessa seulonta perustuu edelleen sekä magneettikuvaus- ja MRCP- että ERC-tutkimukseen (kuvio 1) (12,13). ERC harjasolunäytteineen tehdään kaikille PSC-potilaille taudin vaikeusasteesta riippumatta diagnoosin vahvistamiseksi, PSC:n etenemisen arvioimiseksi ja sappiteiden solumuutosten toteamiseksi sekä endoskooppisen hoidon tarpeen arvioimiseksi ja yksilöllisen seurantasuunnitelman laatimiseksi. Toistuvasti (vähintään kolmesti) todettu lieväasteinen sappitiehytdysplasia on Suomessa aihe maksansiirron arviointiin (30). Geenianalyysi rinnakkaissekvensointimenetelmällä (next-generation sequencing, NGS) voi auttaa tunnistamaan tarkemmin pahanlaatuisuuteen viittaavia geenimuutoksia (31).
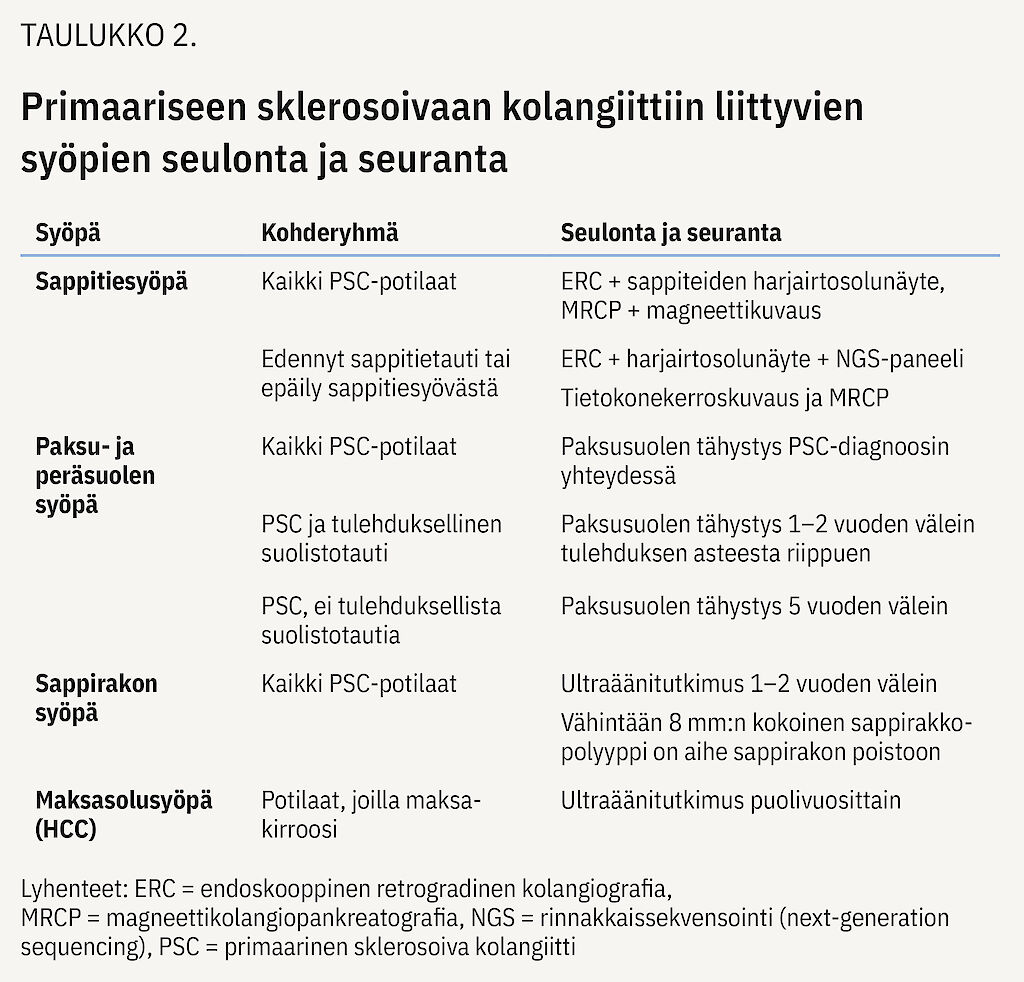
Paksusuolen syöpä : Paksusuolen tähystys biopsioineen tulisi tehdä 1–3 vuoden välein paksusuolen dysplasian seurantaa ajatellen (15,28), tulehduksen asteen mukaan. Tutkimus olisi toistettava viiden vuoden välein niillekin potilaille, joiden paksusuoli näyttää diagnoosin yhteydessä tähystyksessä normaalilta, tai jo aiemmin, jos heillä on suolisto-oireita (27) (taulukko 2).
Miten tautia hoidetaan?
Lääkehoito
PSC:n lääkehoitoa on tutkittu kortikosteroideilla ja muun muassa monoklonaalisilla vasta-aineilla, mutta tulokset ovat jääneet negatiivisiksi. Ursodeoksikoolihaposta (UDCA) on julkaistu useita tutkimuksia (28), ja sen on osoitettu lisäävän bikarbonaatin ja sappihappojen eritystä sekä suojaavan sappiteitä toksisempien sappihappojen aiheuttamalta vauriolta. Cochrane-analyysissä kuitenkin todettiin, että UDCA-hoito ei vähentänyt kuolleisuutta, maksan vajaatoiminnan kehittymistä, siirtoja eikä portahypertension komplikaatioiden kehittymistä, vaikka se laski merkittävästi bilirubiini-, afos-, asat- sekä GT-tasoja (32).
UDCA:n ja metronidatsolin yhdistelmällä tehdyssä 80 potilaan tutkimuksessa todettiin P-afos-pitoisuuksien, Mayo Risk Score -tuloksen ja maksan tulehdusmuutosten paranevan pelkkään UDCA-hoitoon nähden kolmen vuoden seurannassa (33). Muista antibiooteista on tutkittu vankomysiiniä, minosykliiniä ja rifaksimiinia, mutta tutkimukset ovat olleet potilasmääriltään pieniä ja lyhytkestoisia.
Norukoolihappo on UDCA:n johdannainen, jonka tutkimuksesta on juuri julkaistu faasin III ensimmäisen kahden vuoden seurannan tulokset. P-afos laski alle 1,5-kertaiseksi viitealueen ylärajaan nähden, eikä 15,1 %:lla nähty maksan kudosnäytteessä huononemista (lumelääkeryhmässä 4,2 %). Kyseessä on ensimmäinen lääke, jonka on osoitettu hidastavan PSC:n etenemistä (34). Uutena lupaavana lääkeryhmänä tutkitaan ohutsuolen loppuosan sappihappojen kuljettajaproteiinin estäjiä (ibat-estäjiä) voliksibaattia ja maraliksibaattia.
Vaikka näyttöä vaikutuksesta kuolleisuuteen ei UDCA-hoidolla ole saatu, se parantaa kuitenkin maksan biokemiallisia muutoksia ja vähentää sekä paksusuolen että sappiteiden solumuutosten riskiä. Euroopan maksayhdistyksen (EASL) ohjeistus (27) suosittaa UDCA:n käyttöä perustuen sen tehoon maksa-arvoihin ja ennusteindikaattoreihin.
Endoskooppinen hoito
Merkittävät maksanulkoiset ja hilusalueen sappitieahtaumat on aiheellista laajentaa tähystämällä ja kerätä niistä sytologiset näytteet (15). Jos tauti on edennyt pitkälle, mahdollisten sappitiedysplasioiden kehittymistä on syytä seurata systemaattisesti ERC:n yhteydessä otettavin harjairtosolunäyttein ennen sappitiesyövän kehittymistä (12,13) (kuvio 1). Merkittävien ahtaumien (dominanttien striktuuroiden) laajentamisen on oireista riippumatta osoitettu parantavan potilaan ennustetta (35).
Maksansiirto
Maksansiirto on tällä hetkellä pitkälle edenneen PSC:n ainoa tehokas hoito. Koska tautiin liittyy lisääntynyt sappitiesyövän riski, potilas on lähetettävä siirtoarvioon ajoissa, ennen sappitiesyövän kehittymistä, jotta siirto olisi mahdollinen.
PSC on yksi kolmesta tavallisimmasta maksansiirron aiheesta Pohjoismaissa vuorotellen maksasolusyövän ja alkoholikirroosin kanssa. PSC-potilaiden maksansiirron arvion aiheet on tiivistetty liitetaulukkoon 2.
Lopuksi
PSC:n diagnostiikka, seuranta ja hoito vaativat yhteistyötä gastroenterologien, patologien, radiologien, onkologien ja maksakirurgien kanssa.
Sappitiesyövän kehittymisen tunnistaminen on hankalaa. Syöpä kehittyy kuitenkin monivaiheisesti, ja dysplasian varhainen tunnistaminen ja potilaiden ohjaaminen ajoissa maksansiirtoon parantaa todennäköisesti potilaiden kokonaisennustetta.
Kirjoittajilla ei ole sidonnaisuuksia.
- 1
- Hirschfield GM, Karlsen TH, Lindor KD, Adams DH. Primary sclerosing cholangitis. Lancet 2013;382:1587–99.
- 2
- Tenca A, Färkkilä M, Arola J, Jaakkola T, Penagini R, Kolho KL. Clinical course and prognosis of pediatric-onset primary sclerosing cholangitis. United European Gastroenterol J 2016;4:562–9.
- 3
- Loftus EV, Harewood GC, Loftus CG, Tremaine WJ, Harmsen WS, Zinsmeister AR ym. PSC-IBD: a unique form of inflammatory bowel disease associated with primary sclerosing cholangitis. Gut 2005;54:91–6.
- 4
- Tischendorf JJ, Hecker H, Krüger M, Manns MP, Meier PN. Characterization, outcome, and prognosis in 273 patients with primary sclerosing cholangitis: A single center study. Am J Gastroenterol 2007;102:107–14.
- 5
- Deneau MR, Mack C, Abdou R, Amin M, Amir A, Auth M ym. Gamma Glutamyltransferase Reduction Is Associated With Favorable Outcomes in Pediatric Primary Sclerosing Cholangitis. Hepatol Commun 2018;2:1369–78.
- 6
- Barner-Rasmussen N, Sjöblom N, Arola J, Boyd S, Kautiainen H, Färkkilä M. The role of serology, liver function tests and imaging in screening of primary sclerosing cholangitis: the HelPSCreen score. Scand J Gastroenterol 2023;58:1491–8.
- 7
- de Vries EM, Wang J, Leeflang MM, Boonstra K, Weersma RK, Beuers U ym. Alkaline Phosphatase at Diagnosis of Primary Sclerosing Cholangitis and One Year Later: Evaluation of Prognostic Value. Liver Int 2016;36:1867–75.
- 8
- Wunsch E, Norman GL, Milkiewicz M, Krawczyk M, Bentow C, Shums Z ym. Anti-glycoprotein 2 (anti-GP2) IgA and anti-neutrophil cytoplasmic antibodies to serine proteinase 3 (PR3-ANCA): antibodies to predict severe disease, poor survival and cholangiocarcinoma in primary sclerosing cholangitis. Aliment Pharmacol Ther 2021;53:302–13.
- 9
- Grigoriadis A, Imeen Ringe K, Bengtsson J, Baubeta E, Forsman C, Korsavidou-Hult N ym. Development of a prognostic MRCP-score (DiStrict) for individuals with large-duct primary sclerosing cholangitis. JHEP Rep 2022;4:100595.
- 10
- Tenca A, Mustonen H, Lind K, Lantto E, Kolho KL, Boyd S ym. The role of magnetic resonance imaging and endoscopic retrograde cholangiography in the evaluation of disease activity and severity in primary sclerosing cholangitis. Liver Int 2018;38:2329–39.
- 11
- Vanhanen E, Ovissi A, Kolho KL, Tenca A. Magnetic resonance cholangiography in the diagnosis of dominant strictures in pediatric-onset primary sclerosing cholangitis. Dig Liver Dis 2023;55:1496–1501.
- 12
- Boyd S, Tenca A, Jokelainen K, Mustonen H, Krogerus L, Arola J ym. Screening primary sclerosing cholangitis and biliary dysplasia with endoscopic retrograde cholangiography and brush cytology: risk factors for biliary neoplasia. Endoscopy 2016;48:432–9.
- 13
- Boyd S, Mustonen H, Tenca A, Jokelainen K, Arola J, Färkkilä MA. Surveillance of primary sclerosing cholangitis with ERC and brush cytology: risk factors for cholangiocarcinoma. Scand J Gastroenterol 2016;52:242–9.
- 14
- Ismail S, Kylänpää L, Mustonen H, Halttunen J, Lindström O, Jokelainen K ym. Risk factors for complications of ERCP in primary sclerosing cholangitis. Endoscopy 2012;44:1133–8.
- 15
- Aabakken L, Karlsen TH, Albert J, Arvanitakis M, Chazouilleres O, Dumonceau JM ym. Role of endoscopy in primary sclerosing cholangitis: European Society of Gastrointestinal Endoscopy (ESGE) and European Association for the Study of the Liver (EASL) Clinical Guideline. Endoscopy 2017;49:588–608.
- 16
- Burak KW, Angulo P, Lindor KD. Is there a role for liver biopsy in primary sclerosing cholangitis? Am J Gastroenterol 2003;98:1155–8.
- 17
- Melum E, Franke A, Schramm C, Weismüller TJ, Gotthardt DN, Offner FA ym. Genome-wide association analysis in primary sclerosing cholangitis identifies two non-HLA susceptibility loci. Nat Genet 2011;43:17–9.
- 18
- Tenca A, Färkkilä M, Jalanko H, Vapalahti K, Arola J, Jaakkola T ym. Environmental Risk Factors of Pediatric-Onset Primary Sclerosing Cholangitis and Autoimmune Hepatitis. J Pediatr Gastroenterol Nutr 2016;62:437–42.
- 19
- Boonstra K, de Vries EM, van Geloven N, van Erpecum KJ, Spanier M, Poen AC ym. Risk factors for primary sclerosing cholangitis. Liver Int 2016;36:84–91.
- 20
- Haruta I, Kikuchi K, Hashimoto E, Nakamura M, Miyakawa H, Hirota K ym. Long-term bacterial exposure can trigger nonsuppurative destructive cholangitis associated with multifocal epithelial inflammation. Lab Invest 2010;90:577–88.
- 21
- Tabibian JH, Talwalkar JA, Lindor KD. Role of the microbiota and antibiotics in primary sclerosing cholangitis. Biomed Res Int 2013;2013:389537.
- 22
- Boonstra K, Weersma RK, van Erpecum KJ, Rauws EA, Spanier BW, Poen AC ym. Population-based epidemiology, malignancy risk, and outcome of primary sclerosing cholangitis. Hepatology 2013;58:2045–55.
- 23
- Barner-Rasmussen N, Pukkala E, Jussila A, Färkkilä M. Epidemiology, risk of malignancy and patient survival in primary sclerosing cholangitis: a population-based study in Finland. Scand J Gastroenterol 2020;55:74–81.
- 24
- Lunder AK, Hov JR, Borthne A, Gleditsch J, Johannesen G, Tveit K ym. Prevalence of Sclerosing Cholangitis Detected by Magnetic Resonance Cholangiography in Patients With Long-term Inflammatory Bowel Disease. Gastroenterology 2016;151:660–9.e4.
- 25
- Färkkila M, Åberg F, Alfthan H, Jokelainen K, Puustinen L, Kautiainen H ym. Surrogate markers of bile duct disease progression in primary sclerosing cholangitis - A prospective study with repeated ERCP examinations. JHEP Rep 2024;6:101161.
- 26
- de Vries EMG, Färkkilä M, Milkiewicz P, Hov JR, Eksteen B, Thorburn D ym. Enhanced liver fibrosis test predicts transplant-free survival in primary sclerosing cholangitis, a multi-centre study. Liver Int 2017;37:1554–61.
- 27
- European Association for the Study of the Liver. EASL Clinical Practice Guidelines on sclerosing cholangitis. J Hepatol 2022;77:761–806.
- 28
- Bowlus CL, Arrivé L, Bergquist A, Deneau M, Forman L, Ilyas SI ym. AASLD practice guidance on primary sclerosing cholangitis and cholangiocarcinoma. Hepatology 2023;77:659–702.
- 29
- Villard C, Friis-Liby I, Rorsman F, Said K, Warnqvist A, Cornillet M ym. Prospective surveillance for cholangiocarcinoma in unselected individuals with primary sclerosing cholangitis. J Hepatol 2023;78:604–13.
- 30
- Boberg KM, Jebsen P, Clausen OP, Foss A, Aabakken L, Schrumpf E. Diagnostic benefit of biliary brush cytology in cholangiocarcinoma in primary sclerosing cholangitis. J Hepatol 2006;45:568–74.
- 31
- Boyd S, Mustamäki T, Sjöblom N, Nordin A, Tenca A, Jokelainen K ym. NGS of brush cytology samples improves the detection of high-grade dysplasia and cholangiocarcinoma in patients with primary sclerosing cholangitis: A retrospective and prospective study. Hepatol Commun 2024;8:e0415.
- 32
- Poropat G, Giljaca V, Stimac D, Gluud C. Bile acids for primary sclerosing cholangitis. Cochrane Database Syst Rev 2011:CD003626.
- 33
- Färkkilä M, Karvonen AL, Nurmi H, Nuutinen H, Taavitsainen M, Pikkarainen P ym. Metronidazole and ursodeoxycholic acid for primary sclerosing cholangitis: a randomized placebo-controlled trial. Hepatology 2004;40:1379–86.
- 34
- Trauner M, Trivedi P, Denk G, Färkkilä M, Schirmacher P ym. Norucholic acid for the treatment of primary sclerosing cholangitis: 96-week analysis of a pivotal phase 3 trial (LBO 001). J Hepatol 2025;82:Supplement 1, S9.
- 35
- Tenca A, Kolho KL, Consonni D, Jokelainen K, Färkkilä M. Dominant stricture in paediatric-onset primary sclerosing cholangitis is associated with impaired prognosis in a long-term follow-up. United European Gastroenterol J 2024;12:717–25.