Luustoetäpesäkkeiden hoito tähtää parempaan elämänlaatuun
• Syövän luustoetäpesäkkeiden hoidon tavoite on lievittää elämänlaatua heikentäviä oireita.
• Luustopesäke aiheuttaa tyypillisesti kipua ja lisää patologisen murtuman riskiä.
• Oireenmukaisen hoidon keinot ulottuvat kipulääkityksestä kirurgiaan ja kohdennettuihin säde- ja lääkehoitoihin.
• Hoidon valintaa ohjaavat luustoetäpesäkkeiden luonne ja oireisuus. Huomioon otetaan myös potilaan kokonaistilanne ja hoitotoimenpiteiden mahdolliset haitat.
Levinnyttä kiinteän elimen syöpää sairastavista potilaista suurimmalle osalle kehittyy luustoon etäpesäkkeitä. Erityisen tavallisia ne ovat edenneessä eturauhassyövässä, jopa 90 %:lla potilaista. Luustoetäpesäkkeet aiheuttavat kipua ja patologisia murtumia, palliatiivisen sädehoidon tai kirurgian tarvetta, selkäydinpinnettä ja hyperkalsemiaa. Näiden ns. luustokomplikaatioiden riski on suurin rinta-, eturauhas- ja munuaissyöpää sekä ei-pienisoluista keuhkosyöpää sairastavilla (1).
Luustoetäpesäkkeitä esiintyy tavallisimmin nikamissa, lantiossa, kylkiluissa, reisi- ja olkavarren proksimaaliosissa sekä kallossa. Ne ovat luonteeltaan joko skleroottisia, lyyttisiä tai sekamuotoisia (2). Skleroottisissa pesäkkeissä luun rakentajasolujen eli osteoblastien toiminta on kiihtynyt, kun taas lyyttisissä pesäkkeissä luun hajottajasolujen eli osteoklastien toiminta on vallitseva.
Suurin murtumariski liittyy lyyttisiin etäpesäkkeisiin. Eturauhas- ja rintasyövän luustoetäpesäkkeiden komplikaatioriskiä lisää se, että niiden hoidossa käytettävät hormonaaliset lääkkeet aiheuttavat osteoporoosia (3,4).
Luustokomplikaatiot heikentävät elämänlaatua, aiheuttavat sairaalahoidon tarvetta ja lyhentävät potilaan elinajan ennustetta. Luustoetäpesäkkeisiin kohdistuvalla sädehoidolla, radiolääkehoidoilla, syövän etenemistä jarruttavalla lääkehoidolla sekä luustolääkityksellä komplikaatioiden riskiä voidaan vähentää (4,5).
Kliininen kuva ja diagnostiikka
Luustoetäpesäkkeet voivat olla oireettomia, mutta noin 65 %:lle potilaista ne aiheuttavat hoitoa vaativaa kipua, joka on luonteeltaan jomottavaa, jatkuvaa ja liikkuessa voimistuvaa (5). Erityisesti lyyttinen metastaasi voi aiheuttaa murtuman jopa ilman traumaa.
Levinnyttä syöpää sairastavista 5 %:lle kehittyy selkäydinpinne, jossa raajojen lihasvoimat sekä ulosteen ja virtsan pidätyskyky heikkenevät. Ensioireena voi olla raajoihin tai kylkiin heijastuva selkärangan alueen kipu. Joskus kipu voi tuntua vyömäisenä. Akuutti neurologinen puutosoire on aina hätätilanne, joka edellyttää päivystyksellisiä tutkimus- ja hoitotoimia (6).
Laaja-alaisesti luustoon levinnyt syöpä voi aiheuttaa hyperkalsemiaa, jonka tavallisia oireita ovat mm. väsymys, lihasheikkous, ruoansulatuskanavan oireet ja jano. Hyperkalsemiaan voi liittyä myös neurologisia oireita ja hyperkalseeminen kriisi, joka vaatii välittömiä hoitotoimia (7).
Yleisimmin käytetty kuvantamismenetelmä luustoetäpesäkkeitä epäiltäessä on vartalon varjoainetehosteinen tietokonetomografiatutkimus (TT). Luustokartan eli luuston gammakuvauksen avulla luuston tilanteesta on mahdollista saada laajempi kuva ennen kohdennetumpia kuvauksia, sillä se sisältää myös raajat ja kallon (8,9).
Selkäydinpinnettä epäiltäessä ensisijainen tutkimus on selkärangan magneettikuvaus kontrastiaineella. Ranka on syytä kuvata kokonaan, sillä samanaikainen usean kohdan pinne todetaan 20–35 %:lla potilaista (10,11).
Hoitovaihtoehdot
Ulkoinen sädehoito
Ulkoinen sädehoito on tehokas tapa hoitaa luustoetäpesäkkeiden aiheuttamaa kipua. Kertafraktiohoidon tai useampaan hoitokertaan ositetun hoitojakson on todettu olevan yhtä tehokkaita kivunlievityksessä, eikä niiden haittavaikutuksissa ole eroja (12). Potilaista 60–80 % saa sädehoidosta osittaisen ja 25–30 % täydellisen kivunlievityksen (12). Aika sädehoidon vaikutuksen alkuun vaihtelee muutamasta päivästä jopa neljään viikkoon ja lopullinen vaste saavutetaan 4–8 viikon aikana. Vaste jatkuu keskimäärin 3–6 kuukautta.
Kivunlievityksen kesto on kertafraktiohoidolla lyhyempi kuin jaksoittaisella hoidolla, ja siksi kertahoidon jälkeen sädehoito joudutaan uusimaan useammin (20 % vs. 8 %). Suurin osa potilaista kuitenkin hyötyy uusintasädehoidosta. Kertafraktiona toteutettua hoitoa pidetäänkin ensisijaisena komplisoitumattoman luustoetäpesäkkeen aiheuttaman kivun hoidossa. Jos kyseessä on komplisoitunut pesäke (selkäydinkanavaan kasvava pehmytkudosmassa, sen aiheuttama selkäydinpinne tai kantavan luun murtumavaaran aiheuttava etäpesäke), tulee ensisijaisesti harkita fraktioitua hoitoa (13). Kantavan luun murtumalle altistavan pesäkkeen hoitovaihtoehtona voi olla myös profylaktinen kirurginen toimenpide.
Stereotaktista eli suuren kerta-annoksen sädehoitoa voidaan antaa yksittäisiin luustoetäpesäkkeisiin, kun niitä on vähän. Tavoitteena on taudin jarruttaminen. Stereotaktisella sädehoidolla ei ole saavutettu tehokkaampaa kivunlievitystä kuin perinteisellä fraktioinnilla eikä myöskään elämänlaatueroa, mutta uusintasädehoitojen tarve on vähäisempi (14). Lisäksi on saatu joitakin lupaavia tuloksia siitä, että stereotaktisella sädehoidolla saattaa olla vaikutusta taudin etenemättömyysaikaan eturauhassyövän vähäetäpesäkkeisessä vaiheessa (15).
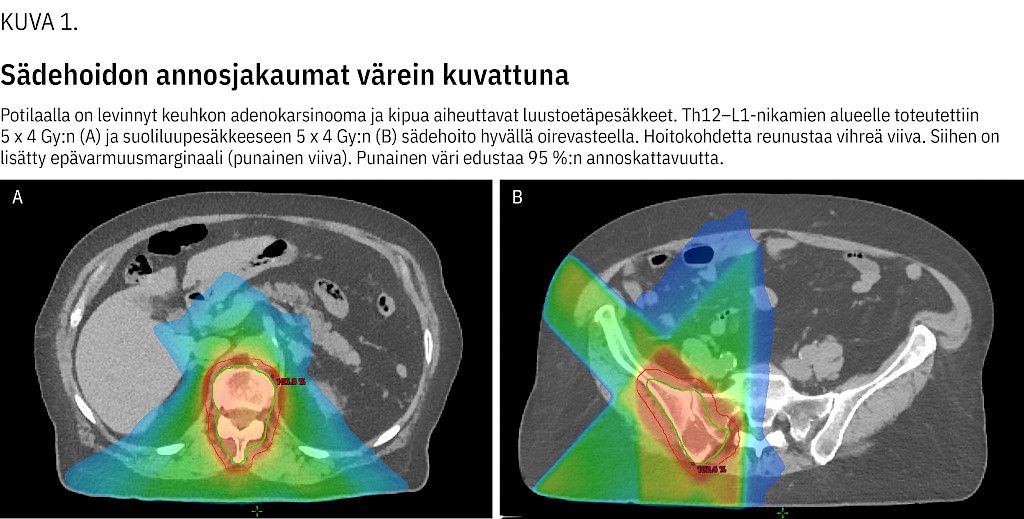
Ennen sädehoidon aloittamista potilaalle tehdään annossuunnittelua varten TT-kuvaus. Kuvasarjaan määritetään hoitokohde, jonka pohjalta laaditaan annossuunnitelma (kuva 1).
Sädehoitokerta asetteluineen kestää 10–15 minuuttia. Jotta hoito voidaan toteuttaa turvallisesti, potilaan tulee olla yhteistyökykyinen ja pysyä hoitojen ajan selällään liikkumatta kovalla korkealle nostetulla hoitopöydällä. Potilaan yleiskunnon tulisi olla kohtalaisen hyvä ja elinajan ennusteen yli 3 kk, jotta sädehoito ehtisi hyödyttää häntä. Riittävästä kipulääkityksestä tulee huolehtia.
Sädehoito on yleensä hyvin siedettyä. Siitä voi kuitenkin hoitokohteen mukaan aiheutua mm. väsymystä, hoitoalueen kivun hetkellistä pahenemista, suolisto- ja rakkoärsytystä, suun ja nielun limakalvojen ärsytystä sekä pahoinvointia. Sädehoidon aikana ja pari päivää sen jälkeen kipu hoidetulla alueella voi pahentua väliaikaisesti, ennen kuin sädehoidon kipua lievittävä vaikutus alkaa 2–4 viikkoa sädehoidon jälkeen. Sädehoidon akuutit haitat väistyvät yleensä 2–4 viikon kuluessa. Palliatiivisesta sädehoidosta ei yleensä aiheudu pitkäaikaishaittoja. Joskus sädehoito saattaa aiheuttaa nikamamurtuman (kompressiomurtuma eli puristusmurtuma), kun kasvainkudos pienenee tai poistuu sädehoidon vaikutuksesta.
Selkäydinpinteen hoidon aloittamisella on aina kiire, koska hoitamattomana tilanne johtaa pysyvään neurologiseen haittaan ja toimintakyvyn menetykseen. Alkuhoito on suuriannoksinen kortikosteroidi, ellei vasta-aiheita ole. Kirurgisesta tai onkologisesta hoidosta (sädehoito, systeeminen hoito) konsultoidaan päivystyksellisesti. Mikäli potilaan motoriikka ja sensoriikka ovat tallella ennen hoidon aloittamista, niiden voi olettaa säilyvän.
Radiolääkehoidot
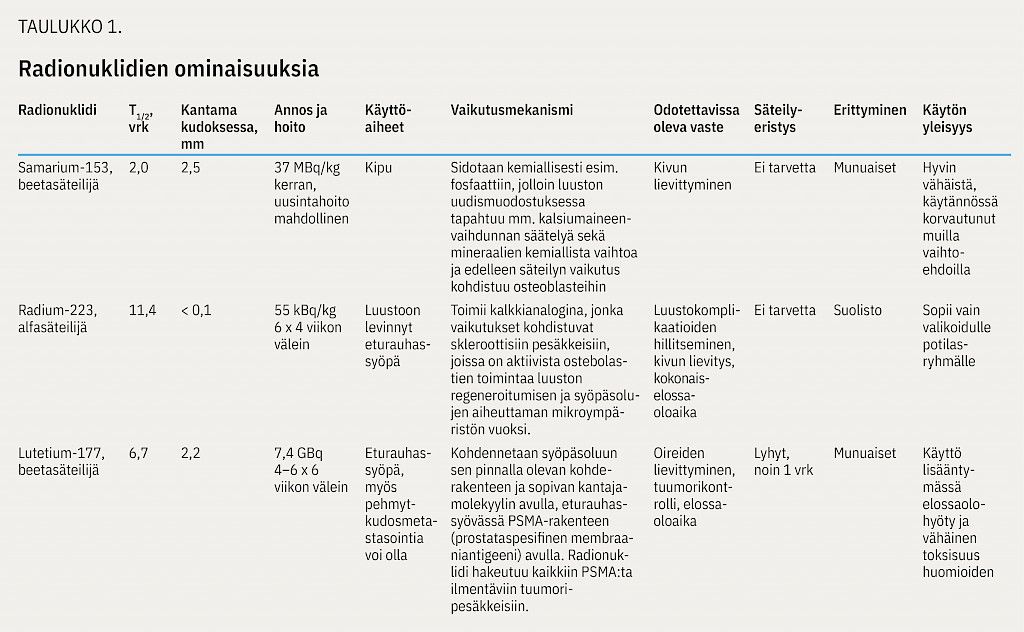
Radiolääkehoitoja voidaan antaa radionuklidin mukaan sekä oireita lievittävällä että taudin etenemistä jarruttavalla tavoitteella. Radiolääkehoito soveltuu erityisesti laaja-alaisen oireisen luustotaudin hoitoon. Tarkoituksena on kerryttää radionuklidin hajoamisesta syntyvästä säteilystä mahdollisimman suuri annos etäpesäkealueen kudokseen ja samalla minimoida terveiden kudosten vaurioita. Solutasolla aiheutuvien säteilybiologisten tapahtumasarjojen myötä luustoetäpesäkkeitä synnyttävien syöpäsolujen toiminta estyy ja hidastuu, samalla kun osteoblastien aktiivisuus heikkenee ja periosteaalisten kipureseptoreiden ärsytys vähenee (16,17,18,19,20,21). Luustoetäpesäkkeiden hoitoon soveltuvien radionuklidien ominaisuuksia on kuvattu taulukossa (taulukko 1).
Vasteet ilmenevät viiveellä. Radiolääkkeiden haittoja ovat luuydinsuppressio sekä munuaistoksisuus, joka liittyy radionuklidin biologiseen poistumiseen elimistöstä. Kumulatiivisten luuydinhaittojen vuoksi radiolääkkeitä käytetään usein monoterapiana, mutta yhteiskäyttö luustolääkkeiden kanssa on tavallista eikä luustolääkkeitä tarvitse tauottaa. Kliinisissä lääketutkimuksissa selvitetään lisäksi mahdollisuuksia yhdistää radiolääkehoito mm. immuno-onkologisten hoitojen kanssa (22).
Radiolääkehoitoihin liittyvät säteilyturvallisuuden erityispiirteet ja velvoitteet sekä mahdollisten komplikaatioiden hoito edellyttävät moniammatillista erityisosaamista ja yhteistyötä sekä potilaskohtaista harkintaa.
Luustolääkkeet
Luustoon levinneessä syövässä käytetään tukihoitona bisfosfonaatteja ja denosumabia. Ne vähentävät luustokomplikaatioiden riskiä, mutta niillä ei ole vaikutusta levinneen syövän ennusteeseen (23).
Bisfosfonaatit ovat pyrofosfaatin analogeja, jotka sitoutuvat voimakkaasti luuhun, aiheuttavat osteoklastien apoptoosia ja estävät luun hajoamista. Ne vähentävät kiinteiden kasvainten luustoetäpesäkkeiden komplikaatioriskiä 30–50 % lumelääkkeeseen verrattuna (1,23,24). Bisfosfonaateista tehokkain on tsoledronihappo, jota annetaan suoneen 4 mg 1–3 kuukauden välein (23,25). Suun kautta päivittäin otettavilla ibandronaatilla (50 mg/vrk) ja klodronaatilla (1 600 mg/vrk) on käyttöaiheena vain rintasyövän luustoetäpesäkkeiden hoito.
Denosumabi on RANK‑ligandin monoklonaalinen vasta-aine. Se estää osteoklastien aktiivisuutta eikä varastoidu luuhun (23). Denosumabi annoksella 120 mg kuukauden välein vähentää kiinteiden kasvainten luustoetäpesäkkeiden komplikaatioriskiä vielä 17 % tsoledronihappoon verrattuna (26). Paremman tehon ja ihonalaisen annostelun vuoksi denosumabi on nykyään tsoledronihappoa käytetympi.
Leukaluukuolio on luustolääkkeiden pelätyin haitta. Sillä tarkoitetaan leukaluun paljastumista tai leukaluuhun johtavaa fisteliä luustolääkettä käyttäneellä potilaalla. Denosumabi aiheuttaa leukaluukuoliota useammin kuin bisfosfonaatit, ja suurin riski liittyy näiden lääkkeiden peräkkäiseen käyttöön (27).
Leukaluukuolion riskiä voi vähentää välttämällä hampaanpoistoja luustolääkkeen käytön aikana, huolehtimalla suuhygieniasta ja mahdollisesti pidentämällä luustolääkkeen annosväliä. Huonoennusteiset hampaat tulisi poistaa ja poistokuopan parantua pari kuukautta ennen luustolääkityksen aloittamista. Jos leukaluukuolio on jo kehittynyt, potilas ohjataan suu- ja leukakirurgin hoitoon (28).
Veren kalsiumpitoisuuksia seurataan luustolääkityksen yhteydessä hypokalsemian varalta. Munuaisten vajaatoiminta lisää vaikean hypokalsemian riskiä. Suun kautta otettaviin bisfosfonaatteihin liittyy ruoansulatuskanavan ärsytysoireita. Epätyypillisiä subtrokanteerisia reisiluun murtumia tavataan luustolääkkeiden harvinaisena haittana (1).
Kivun hoito
Luuston etäpesäkkeistä aiheutuvan kivun hoito noudattaa pääosin yleisiä kroonisen kivun hoidon periaatteita. Kipulääke valitaan kivun voimakkuuden mukaan (WHO:n kipuportaat). Tulehduskipulääkkeet ovat erityisen tehokkaita luustoetäpesäkkeiden aiheuttamassa kivussa, ja niiden käyttöä kannattaa yleensä jatkaa opioidin rinnalla (29,30).
Vaikeiden luustokipujen hoito on useimmiten syytä aloittaa suoraan vahvalla opioidilla (esim. morfiini tai oksikodoni) ja liittää mukaan tulehduskipulääke (tai parasetamoli), toki mahdolliset vasta-aiheet huomioiden. Heikompia opioideja (tramadoli, kodeiini) voidaan harkita vain lievään tai korkeintaan kohtalaiseen kipuun (30).
Edenneessä syövässä 30–40 %:lla potilaista kivussa on mukana neuropaattinen komponentti. Opioidihoitoon yhdistetyt neuropaattisen kivun hoidossa käytettävät lääkkeet, kuten gabapentinoidit (gabapentiini, pregabaliini), trisykliset masennuslääkkeet, duloksetiini ja venlafaksiini, tehostavat kivun hoitoa (29,30).
Kivun säännöllinen arviointi ja kirjaaminen on hyvän hoidon perusedellytys. Kivun voimakkuus voidaan kirjata joko VAS-kipujanaa tai numeerista arviointiasteikkoa käyttäen. Lääkehoidon rinnalla käytetään myös lääkkeettömiä kivunhallintakeinoja, kuten asento- ja liikehoitoja sekä rentoutusta (30).
Lopuksi
Tässä kuvattujen menetelmien lisäksi syövän etenemistä jarruttavat hoidot, kuten hormonaalinen ja solunsalpaajahoito, vähentävät luustoetäpesäkkeiden komplikaatioriskiä. Hoidossa tulee aina huomioida riittävä kivunlievitys. Luustoetäpesäkkeiden aiheuttaman kivun hoitoa pyritään kehittämään uusilla hoitomuodoilla, kuten magneettikuvausohjauksessa kohdennetulla suurienergiaisella ultraäänikuumennushoidolla (HIFU). Sitä voidaan antaa kallon ja rangan ulkopuolisiin luustoetäpesäkkeisiin, jos uusintasädehoito ei ole enää mahdollinen tai potilas ei ole hyötynyt palliatiivisesta sädehoidosta (31).
Anu Anttonen: Ei sidonnaisuuksia.
Leena Vehmanen: Luentopalkkio (Amgen), kongressiin osallistuminen (Pfizer).
Veera Ahtiainen: Apurahat (Suomen Onkologiayhdistys, Helsingin yliopisto, Hus Syöpäkeskus), kliininen lääketutkimus (Bayer, MSD).
- 1
- Coleman R, Hadji P, Body J ym. Bone health in cancer: ESMO Clinical Practice Guidelines. Ann Oncol 2020;31:1650–63. doi: 10.1016/j.annonc.2020.07.019
- 2
- Ryan C, Stoltzfus KC, Horn S ym. Epidemiology of bone metastases. Bone 2022;158:115783. doi: 10.1016/j.bone.2020.115783
- 3
- Murtola T, Seikkula H, Vehmanen L ym. Eturauhassyövän kastraatiohoidon haittavaikutukset. Suom Lääkäril 2021;76(45):2647–51.
- 4
- Vehmanen L, Matikainen N. Luustolääkkeet estävät varhaisvaiheen rintasyöpää sairastavien murtumia ja parantavat taudin ennustetta. Duodecim 2019;135:2283–90.
- 5
- Kimura T. Multidisciplinary approach for bone metastasis: a review. Cancers 2018;10:156. doi: 10.3390/cancers10060156.
- 6
- Kankare J, Anttonen A. Selkärangan etäpesäkkeiden hoito. Suom Lääkäril 2017;72:1219–24.
- 7
- Hu M. Hypercalcemia of malignancy. Endocrinol Metab Clin North Am 2021;50:721–8.
- 8
- Mottet. N, Bellmunt J, Bolla M ym. EAU-ESTRO-SIOG guidelines on prostate cancer. Part 1: screening, diagnosis, and local treatment with curative intent Eur Urol 2017;71:618–29.
- 9
- Senku E, Kyriakides S, Ohno S ym. Primary breast cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol 2015;26:v8-v30.
- 10
- Prasad D, Schiff D. Malignant spinal-cord compression. Lancet Oncol 2005;6:15–24.
- 11
- Oldenburger E, Brown S, Willmann J ym. ESTRO ACROP guidelines for external beam radiotherapy of patients with complicated bone metastases. Radiother Oncol 2022;173:240–53. doi: 10.1016/j.radonc.2022.06002
- 12
- Rich S, Chow R, Raman S ym. Update of the systematic review of palliative radiation therapy fractionation for bone metastases. Radiother Oncol 2018;126:547–557. doi: 10.1016/j.radonc.2018.01.003
- 13
- Lutz S, Balboni T Jones J, ym. Palliative radiation therapy for bone metastases: update of an ASTRO evidence-based guideline. Pract Radiat Oncol 2017;7:4–12. doi: 10.1016/j.prro.2016.08.001
- 14
- van der Velden J, Willmann J, Spalek M ym. ESTRO ACROP guidelines for external beam radiotherapy of patients with uncomplicated bone metastases. Radiother Oncol 2022;173:197–206.
- 15
- Zhang B, Leech M. A review of stereotactic body radiation therapy in the management of oligometastatic prostate cancer. Anticancer Res 2020;40:2419–28.
- 16
- Parker C, Nilsson S, Heindrich D ym. Alpha emitter radium-223 and survival in metastatic prostate cancer. N Engl J Med 2013;369:213–23. doi: 10.1056/NEJMoa1213755
- 17
- Murray I, Dy Y. Systemic radiotherapy of bone metastases with radionuclides. Clin Oncol 2021;33:98–105. doi: 10.1016/j.clon.2020.11.028
- 18
- Manafi-Farid R, Masoumi F, Divband G ym. Targeted palliative radionuclide therapy for metastatic bone pain. J Clin Med 2020;9:1–24. doi: 10.3390/jcm9082622
- 19
- Bodei L, Lam M, Chiesa C ym. EANM procedure guideline for treatment of refractory metastatic bone pain. Eur J Nucl Med Mol Imaging 2008;35:1934–40. doi: 10.1007/s00259-008-0841-y
- 20
- Sartor O, de Bono J, Chi K ym. Lutetium-177-PSMA-617 for metastatic castration-resistant prostate cancer. N Engl J Med 2021;385:1091–103. doi: 10.1056/NEJMoa2107322
- 21
- Denis-Bacelar A, Chittenden S, McCready R ym. Bone lesion absorbed dose profiles in patients with metastatic prostate cancer treated with molecular radiotherapy. Br J Radiol 2018;91:20170795. doi: 10.1259/bjr.20170795
- 22
- Marshall C. fu W, Wang H ym. Randomized phase II trial of sipuleucel-T with or without radium-223 in men with bone-metastatic castration-resistant prostate cancer. Clin Cancer Res 2021;27:1623–30. doi: 10.1158/1078-0432.CCR-20-4476
- 23
- D'Oronzo S, Coleman R, Brown J, Silvestris F. Metastatic bone disease: Pathogenesis and therapeutic options: Up-date on bone metastasis management. J Bone Oncol 2018;15:004–4. doi: 10.1016/j.jbo.2018.10.004
- 24
- Palmieri C, Fullarton J ja Brown J. Comparative efficacy of bisphosphonates in metastatic breast and prostate cancer and multiple myeloma: a mixed-treatment meta-analysis. Clin Cancer Res 2013;19:6863–72. doi: 10.1158/1078–0432. CCR-13-2275
- 25
- Himelstein AL, Foster J, Khatcheressian J ym. Effect of longer-interval vs standard dosing of zoledronic acid on skeletal events in patients with bone metastases. A randomized clinical trial. JAMA 2017;317:48–58. doi: 10.1001/jama.2016.19425
- 26
- Lipton A, Fizazi K, Stopeck A ym. Superiority of denosumab to zoledronic acid for prevention of skeletal-related events: a combined analysis of 3 pivotal, randomised, phase 3 trials. Eur J Cancer 2012;48:3082. doi: 10.1016/j.ejca.2012.08.002
- 27
- Loyson T, Van Cann T, Schöffski P ym. Incidence of osteonecrosis of the jaw in patients with bone metastases treated sequentially with bisphosphonates and denosumab. Acta Clin Belg 2018;73:100–109. doi: 10.1080/17843286.2017.1348001
- 28
- Antiresorptiivista lääkitystä saavien potilaiden hammashoito. Hoitoketjut. HUS-HYKS Suu- ja leukasairauksien linja. Helsinki: Suomalainen Lääkäriseura Duodecim 2020
- 29
- Kalso E. Syöpäkivun lääkehoito. Duodecim 2016;132: 2125–8.
- 30
- Suomalaisen Lääkäriseuran Duodecimin ja Suomen Palliatiivisen Lääketieteen yhdistyksen asettama työryhmä. Palliatiivinen hoito ja saattohoito. Käypä hoito -suositus 4.10.2019. www.kaypahoito.fi
- 31
- Slotman DJ, Bartels MMTJ, Ferrer CJ ym. Focused Ultrasound and RadioTHERapy for non-invasive palliative pain treatment in patients with bone metastasis: a study protocol for the three-armed randomized controlled FURTHER trial. Trials 2022;23:1061.
Treatment of skeletal metastases
In the treatment of skeletal metastases, the goal is to alleviate symptoms that impair the quality of life. The skeletal metastasis is commonly associated with pain and the risk of pathological fracture. There are number of active symptomatic treatments, from appropriate pain medication to surgery and targeted treatments.
The choice of treatment is guided by the clinical and radiological characteristics of the bone lesions in relation to the patients` overall benefit and potential disadvantages of the treatment measures.
Anu Anttonen, Leena Vehmanen, Veera Ahtiainen