Uusi suomalainen klamydiavariantti – haaste molekyylidiagnostiikalle
• Alkuvuodesta 2019 TYKS:n mikrobiologian laboratoriossa havaittiin ristiriitaisia klamydiatestituloksia. Niiden selvittelyn tuloksena löydettiin suomalainen Chlamydia trachomatis -variantti, joka ei näkynyt laajasti käytössä olleessa klamydian ja tippurin seulontatestissä.
• Variantin 23S rRNA -geenin alueella todettiin yhden emäksen mutaatio. Sen vaikutusta bakteerin ominaisuuksiin tai kliinistä merkitystä ei vielä pystytä arvioimaan.
• Arviolta 6–10 % klamydiatapauksista on mutaation vuoksi jäänyt löytymättä Etelä- ja Länsi-Suomessa viime vuosina. Tosin näytteenoton puutteiden takia tapauksia saattaa jäädä toteamatta sitäkin enemmän.

TYKS:n kliinisen mikrobiologian laboratoriossa todettiin kevättalvella 2019 ristiriita kahden eri klamydiatestin antamien tulosten välillä. 32-vuotiaan oireisen miehen virtsanäyte oli C. trachomatis -positiivinen laajassa seksitautien seulontatutkimuksessa, vaikka potilaalla oli usea negatiivinen testitulos varsinaisessa klamydian ja tippurin tutkimuksessa (Aptima Combo 2). Hänen partnerinsa oli todettu C. trachomatis -positiiviseksi Tampereella.
Löydösten perusteella alettiin epäillä TYKS:n käyttämässä testissä "näkymätöntä" klamydiaa. Useiden ristiriitaisia tuloksia antaneiden tapausten ilmaantuminen johti selvittelyihin ja lopulta uuden suomalaisen klamydiavariantin (FI-nvCT) löytymiseen (1,2,3).
Tausta
Chlamydia trachomatiksen aiheuttama klamydia on yleisin seksiteitse tarttuva bakteeri-infektio. Suomessa kliinisen mikrobiologian laboratoriot ilmoittavat Terveyden ja hyvinvoinnin laitoksen (THL) ylläpitämään tartuntatautirekisteriin vuosittain lähes 15 000 klamydiatapausta (https://thl.fi/fi/web/infektiotaudit/seuranta-ja-epidemiat/tartuntatautirekisteri).
C. trachomatis aiheuttaa naisille mm. kohdunkaulan tulehduksia, virtsaputkitulehduksia sekä infektion pitkittyessä myös sisäsynnytintulehduksia (pelvic inflammatory disease, PID) ja munanjohdinperäistä hedelmättömyyttä. Klamydiainfektio on myös liitetty raskausajan ongelmiin, ja vastasyntyneellä voi äidiltä saadun tartunnan seurauksena ilmetä sidekalvon tulehdusta ja hengitystieinfektioita. Miehillä voi esiintyä virtsaputkitulehduksia ja lisäkivestulehduksia (4). Valtaosa sekä miesten että naisten tartunnoista on kuitenkin oireettomia, ja riskiryhmien säännöllinen testaaminen on epidemian hallinnan kulmakiviä (4,5).
Klamydian ja tippurin seulontaan on saatavissa useita herkkiä ja tarkkoja bakteerien nukleiinihappojen monistamiseen perustuvia testejä ja automatisoituja laitteistoja (3). Testeillä voidaan tutkia ensivirtsanäytteiden lisäksi emättimestä, kohdunkaulakanavasta, virtsaputkesta ja peräsuolesta sekä nielusta ja silmästä otettavia tikkunäytteitä (6).
Ruotsissa todettiin vuonna 2006 muuntunut C. trachomatis -kanta (nv-CT), jonka plasmidista puuttui 377 emäsparin pituinen geenijakso juuri kahden yleisesti käytetyn kaupallisen testin kohdealueelta (7). Variantti jäi näillä testeillä löytymättä, ja sen jäljille päästiin vasta, kun Hallandin alueella Länsi-Ruotsissa alettiin selvittää klamydiatapausten odottamatonta 25 %:n vähenemistä vuodesta 2005 vuoteen 2006. Diagnostiikan epäonnistuminen tarjosi variantille huomattavan valintaedun, ja vuonna 2007 sen osuus klamydiainfektioista siihen osumattomia testejä käyttäneillä alueilla oli jopa yli puolet (8).
Uusi suomalainen klamydiavariantti
Heti ristiriitaisten testitulosten ilmettyä kevättalvella 2019 TYKS:sta otettiin yhteyttä Aptima Combo 2 -yhdistelmätestin (AC2, C. trachomatiksen kohdegeeni 23S rRNA) valmistajaan, ja käyttöön saatiin saman valmistajan toinen testi (ACT, C. trachomatiksen kohdegeeni 16S rRNA). Aiemmat ristiriitaisen tuloksen antaneet näytteet olivat ACT-testillä positiivisia, mikä vahvisti epäilyn, että C. trachomatiksen osoitus AC2-testillä oli epäonnistunut osassa tutkituista näytteistä. Vaikka laitteiston ohjelmisto tulkitsi ristiriitaisia tuloksia antaneet näytteet AC2-testillä negatiivisiksi, sellaisissa näytteissä, joissa muiden testien perusteella esiintyi klamydiaa, laitteen ilmoittama signaali huomattiin hiukan korkeammaksi kuin täysin negatiivisissa näytteissä.
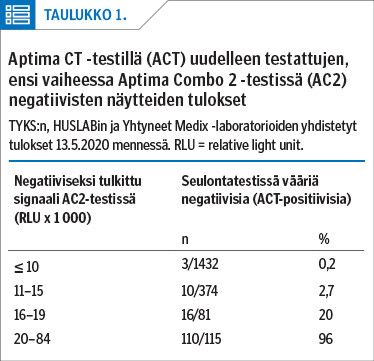
TYKS:n lisäksi AC2-testiä käyttävät Suomessa HUSLAB, Yhtyneet Medix Laboratoriot (YML), Satadiag ja Päijät-Hämeen hyvinvointikuntayhtymän laboratorio (nykyään osa Fimlabia). Näissä laboratorioissa toukokuun 2019 puoleenväliin mennessä negatiivisiksi tulkituille näytteille tehdyissä varmistustesteissä huomattava osa kohonneen signaalin antaneista näytteistä osoittautui positiivisiksi (taulukko 1). Löydöksiä oli melko tasaisesti miesten ja naisten näytteissä.
Ristiriitaisen tuloksen antaneita näytteitä tutkittiin Helsingin yliopiston lääketieteellisen tiedekunnan virologian osastolla. Sekvensoimalla todettiin niiden sisältämän C. trachomatiksen 23S ribosomaalista RNA:ta koodittavassa geenissä (AC2-testin kohde) yhden emäksen muutos ja bakteeri nimettiin suomalaiseksi klamydiavariantiksi (FI-nvCT). Tätä muutosta ei ole osoitettu Suomessa tai muualla aikaisemmin sekvensoiduissa C. trachomatis -kannoissa (1,3).
Koska makrolidien sitoutumiskohta on toisaalla ribosomissa, mutaatio ei todennäköisesti heikennä kannan herkkyyttä makrolideille, joita käytetään yleisesti infektion hoidossa (3). Vasta bakteerin koko genomin sekvensointi kuitenkin varmistaa, esiintyykö variantilla muita mutaatioita, joilla voisi olla vaikutuksia bakteerin tarttuvuuteen, virulenssiin, mikrobilääkeherkkyyteen tai yleiseen kilpailukykyyn (fitness).
Kesällä 2019 testivalmistaja vahvisti, että C. trachomatiksen 23S rRNA:ssa toteamamme mutaatio on väärien negatiivisten tulosten juurisyy (2), ja kehotti kaikkia eurooppalaisia AC2-testin käyttäjiä aloittamaan negatiivisiksi tulkittujen, mutta taustatasoa hieman korkeampaa signaalia (RLU ≥ 15 000) antavien näytteiden testaamisen ACT:llä, kuten suomalaiset käyttäjät olivat alkaneet tehdä jo keväällä (Hologic Field Safety Notice 7.6.2019).
Helsingin ja Uudenmaan sairaanhoitopiirissä sekä Kymenlaaksossa, Varsinais-Suomessa, Satakunnassa ja Päijät-Hämeessä klamydiadiagnostiikassa on käytetty AC2-testiä lähes koko kuluvan vuosikymmenen ajan. Yksittäisiä mahdollisia FI-nvCT-havaintoja on myös Pohjois-Pohjanmaan, Vaasan, Etelä-Pohjanmaan, Pirkanmaan ja Kanta-Hämeen sairaanhoitopiirien alueilla otetuista näytteistä (Sakari Jokiranta, julkaisemattomia havaintoja).
Mahdollisesti FI-nvCT:n aiheuttamien tartuntojen määrä Suomessa oli huhtikuun 2019 lopussa noin 170 (1). TYKS:ssa tutkitun valikoimattoman aineiston perusteella arvioimme, että FI-nvCT:n osuus klamydialöydöksistä on 6–10 %. Suhteutettuna AC2-testiä käyttäneistä sairaanhoitopiireistä vuonna 2018 Tartuntatautirekisteriin ilmoitettuihin klamydialukuihin (8 659 tapausta) tämä tarkoittaisi, että vuonna 2019 olisi jäänyt löytymättä 520–866 variantin aiheuttamaa tapausta.
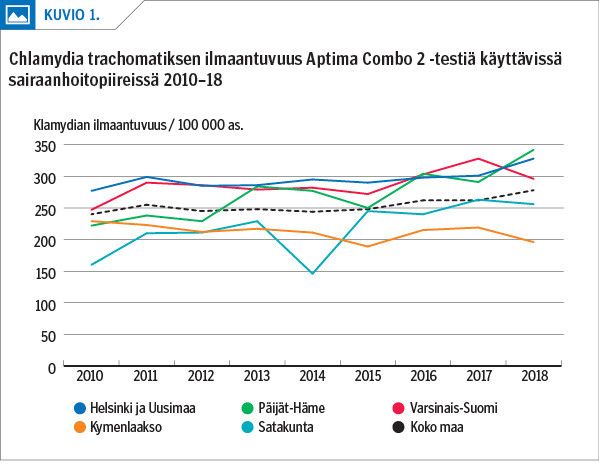
Tartuntatautirekisteriin kootuista tiedoista ilmenee myös, että klamydian ilmaantuvuudessa tapahtui Varsinais-Suomessa noin 10 %:n lasku vuodesta 2017 vuoteen 2018. Ilmaantuvuus pieneni myös Kymenlaaksossa, kun taas HUS-piirin alueella ja Päijät-Hämeessä se jatkoi nousuaan (kuvio 1). Varsinais-Suomessa klamydian insidenssi nousi vuonna 2019 takaisin vuoden 2017 tasolle ja kääntyi selvään nousuun Kymenlaaksossa ja Satakunnassa.
Laboratoriodataa tutkimalla on selvinnyt, että negatiivisiksi tulkittujen, mutta hieman kohonneen signaalin (RLU 20 000–84 000) antaneiden näytteiden osuus lisääntyi HUSLABissa ja YML:ssä vuonna 2017 ja TYKS:ssa vuonna 2018, mikä saattaa kuvastaa variantin ilmaantumista ja yleistymistä. Suurimmillaan näiden näytteiden osuus oli 0,5–1 % (3). Varhaisin näyte, josta varianttikanta on voitu molekyylibiologisesti todeta, on otettu Turussa kesäkuun lopussa vuonna 2018 (1).
Euroopan tautivirasto ECDC teki tilanteesta nopean riskinarvion kesäkuussa (11). FI-nvCT:n levinneisyyttä Euroopassa on tarkoitus selvittää kohonneen, mutta negatiiviseksi tulkitun signaalin antaneiden näytteiden uusintatestauksin sekä spesifisen FI-nvCT-testin avulla. Toistaiseksi Suomen lisäksi FI-nvCT-tartuntoja on löydetty runsaasti Norjasta (12) ja muutamia Keski-Ruotsista Örebron alueelta, jossa toimivassa WHO:n yhteistyölaboratoriossa testaus aloitettiin jo maaliskuun lopulla 2019 (13). Sen sijaan Britanniassa tehdyssä laajassa seulonnassa tutkittiin noin 250 000 näytettä löytämättä yhtään FI-nvCT-bakteeria (14).
Jatkossa selvinnee, onko FI-nvCT oikeasti suomalainen erikoisuus vai jo aiemmin laajalle levinnyt, mutta harvinainen muunnos, joka on yleistynyt todettavalle tasolle vasta nyt Suomessa sille otollisten olosuhteiden vuoksi. Testivalmistajan nopean reagoinnin ansiosta nyt on käytössä uusi testiversio, joka löytää myös nykyisin tunnetut mutatoituneet bakteerit.
Kliininen merkitys
Klamydian kantajat voivat levittää tartuntaa ja hoitamattomaan infektioon liittyy pitkäaikaiskomplikaatioiden mahdollisuus. Koska laboratoriodatasta todennäköiset väärät negatiiviset tulokset oli mahdollista erottaa oikeista negatiivisista kohtalaisella tarkkuudella, useimmat laboratoriot päätyivät kutsumaan uuteen tutkimukseen potilaat, joiden näytteestä oli saatu epäilyttävä tulos (hieman kohonnut signaali, RLU ≥ 20 000 mutta tulkinta negatiivinen tai raja-arvoinen) vuoden 2018 alun jälkeen eli puoli vuotta ennen ensimmäistä varmistettua tapausta.
TYKS:ssa oli lokakuun 2019 loppuun mennessä todettu 72 mutaation osalta varmistettua tai testitulosten perusteella todennäköistä FI-nvCT-tartuntaa, mikä oli 8 % kaikista klamydialöydöksistä. Kaikkiaan 21 (29 %) varianttilöydöksistä tehtiin uusintanäytteeseen kutsuttujen potilaiden näytteistä. Potilaiden keski-ikä on 26,9 vuotta (vaihteluväli 17–48 v). Vaikka huhtikuun 2019 loppuun mennessä todetuissa tapauksissa miesten ja naisten osuudet olivat lähes yhtä suuret, nyt naisten osuus oli 64 %. Ero selittynee sillä, että naiset ovat noudattaneet uusintakutsua useammin kuin miehet. Yhdistämällä uusintanäytteessä käyneiden potilaiden laboratoriodataa ja kliinisiä tietoja voidaan saada mielenkiintoista tietoa pitkittyneestä klamydiainfektiosta yleensä ja varianttikannasta erityisesti, mutta toistaiseksi luvut ovat liian pieniä mielekkäiden päätelmien tekemiseksi.
Ruotsissa sikäläinen varianttikanta todettiin vuonna 2006. Taalainmaalla ja Örebron alueella, joissa se oli jäänyt toteamatta ja saanut levitä, kannan osuus klamydiatapauksista oli 56 %, kun taas Upsalan ja Norrbottenin alueilla, joissa käytössä ollut testi tunnisti variantin, osuus oli 19 %. Kun Taalainmaalla ja Örebrossakin saatiin käyttöön uudet, myös varianttikannan tunnistavat testiversiot, alueiden väliset erot alkoivat tasaantua, ja vuonna 2015 ruotsalaisen varianttikannan osuus oli selvästi alle 10 % riippumatta siitä, mitä testiä alueella käytettiin 10 vuotta aikaisemmin (15). Huolimatta siitä, että arviot väärän negatiivisen tuloksen saaneiden testien kokonaismääristä Ruotsissa vaihtelivat 8 000:n ja 15 000:n välillä, klamydiaan liittyvien komplikaatioiden esiintyvyys vuoteen 2015 ulottuneessa seurannassa oli vain vähän suurempi sellaisilla alueilla, joissa varianttikanta jäi toteamatta.
Koska Suomessa variantti havaittiin varhain, löytymättä jääneiden klamydiatartuntojen määrä jäänee selvästi pienemmäksi kuin aikanaan samankaltaisessa tilanteessa Ruotsissa. Emme vielä tiedä riittävästi suomalaisesta variantista, jotta pystyisimme arvioimaan sen kliinistä merkitystä. Ei ole syytä olettaa, että variantti poikkeaisi olennaisesti muista klamydioista tarttumis- tai taudinaiheuttamiskyvyltään tai hoitovasteeltaan, mutta asiaa selvitetään parhaillaan.
On myös muistettava, että näytteenottoon liittyvät tekijät voivat johtaa vääriin negatiivisiin klamydiatuloksiin. Miehiltä suositellaan tutkittavaksi asianmukaisesti otettu ensivirtsanäyte, mutta naisilta emättimen limakalvon tikkunäyte on suositeltavampi, koska sen avulla todetaan klamydian aiheuttama kohdunkaulan tulehdus varmemmin kuin ensivirtsanäytteestä. Ensivirtsanäytteistä ei myöskään voida todeta nielussa tai peräsuolessa olevaa tartuntaa, vaan näytteenotto tulee kohdentaa tartunnalle altistuneille alueille (6,16).
Lopuksi
Bakteerien ribosomaalista RNA:ta pidetään hyvin stabiilina, ja tästä syystä se lienee valikoitunut diagnostisen testin kohteeksi. FI-nvCT-bakteerin löytyminen kuitenkin osoittaa, että mikrobien evoluutio jatkuu ja vastaa ympäristön haasteisiin; tässä tapauksessa laajasti ja pitkään käytetyn diagnostisen testin aiheuttama selektiopaine saattoi johtaa variantin ilmaantumiseen.
Vaikka klamydia yleisyytensä ja ominaispiirteidensä, mm. oireettomien tartuntojen suuren osuuden vuoksi lienee yksi diagnostiikan haastavimmista infektioista, nyt todetun ilmiön opetukset ovat yleistettävissä muidenkin infektioiden molekyylidiagnostiikkaan. Varsinkin suuria näytemääriä tutkivat täysautomaattiset systeemit, joissa tulokset siirtyvät suoraan laboratoriotietojärjestelmään, vaativat huolellista ja mieluiten automatisoitua trendiseurantaa varianttien ja muiden testiympäristössä tapahtuvien muutosten toteamiseksi.
Tässä tapauksessa oireisille potilaille tarkoitettu laaja seksitautien seulontatesti (johon klamydian ja tippurin aiheuttajat olivat tulleet mukaan vasta hiljakkoin), sen tulosten huolellinen tarkastelu, diagnostiikan sudenkuoppien tuntemus sekä sukupuolitautipoliklinikan ja laboratorion ennestään tiivis yhteydenpito johtivat varsin nopeasti variantin jäljille. Näiden tekijöiden – erityisesti kliinikon ja laboratorion yhteistyön – merkitystä ei pidä väheksyä entisestään keskittyvässä ja automatisoituvassa kliinisessä laboratoriotoiminnassa.
Kaisu Rantakokko-Jalava: Luentopalkkio ja matkakorvaus (Hologic). Konsultointipalkkiot (Labquality), luentopalkkiot (Professio, Labquality, alan yhdistykset), tekijänpalkkiot (Duodecim).
Mirja Puolakkainen: Apurahat laitokselle (Suomen Akatemia, HUS EVO, matkakorvaus (Hologic).
- 1
- Rantakokko-Jalava K, Hokynar K, Hieta N ym. Chlamydia trachomatis samples testing falsely negative in the Aptima Combo 2 test in Finland, 2019. Euro Surveill 2019;24(22):1900298. doi: 10.2807/1560-7917.ES.2019.24.22.1900298
- 2
- Unemo M, Getman D, Hadad R ym. Letter to the editor: Chlamydia trachomatis samples testing falsely negative in the Aptima Combo 2 test in Finland, 2019. Euro Surveill 2019;24(24):1900354. doi: 10.2807/1560-7917.ES.2019.24.24.1900354
- 3
- Hokynar K, Rantakokko-Jalava K, Hakanen A. The Finnish new variant of Chlamydia trachomatis with a single nucleotide polymorphism in the 23S rRNA target escapes detection by the Aptima Combo 2 test. Microorganisms 2019;7:227.
- 4
- Paavonen J. Klamydiakantaja – oireeton vai uskoton? Duodecim 2012;128:1351–6.
- 5
- European Centre for Disease Prevention and Control. Guidance on chlamydia control in Europe– 2015. Stockholm: ECDC; 2016.
- 6
- Hiltunen-Back E, Puolakkainen M. Oireettomuus yleistä tippurissa ja klamydiassa. Suom Lääkäril 2018;73:1590–2.
- 7
- Ripa T, Nilsson PA. A variant of Chlamydia trachomatis with deletion in cryptic plasmid: implications for use of PCR diagnostic tests. Euro Surveill 2006;11:E061109.1.
- 8
- Herrmann B, Törner A, Low N ym. Emergence and spread of Chlamydia trachomatis variant, Sweden. Emerg Infect Dis 2008;14:1462–5.
- 9
- Korhonen S, Hiltunen-Back E, Puolakkainen M. Genotyping of Chlamydia trachomatis in rectal and pharyngeal specimens: identification of LGV genotypes in Finland. Sex Transm Infect 2012;88:465–9.
- 10
- Hadfield J, Harris SR, Seth-Smith HMB ym. Comprehensive global genome dynamics of Chlamydia trachomatis show ancient diversification followed by contemporary mixing and recent lineage expansion. Genome Res 2017;27:1220–9.
- 11
- European Centre for Disease Prevention and Control. Rapid risk assessment: Chlamydia trachomatis false-negative test results by Aptima Combo 2 CT/NG assay in the EU/EEA, 2019 – 17 June 2019. Stockholm: ECDC; 2019.
- 12
- Johansen TB, Kløvstad H, Rykkvin R ym. The ‘Finnish new variant of Chlamydia trachomatis’ escaping detection in the Aptima Combo 2 assay is widespread across Norway, June to August 2019. Euro Surveill 2019;24(42):1900592. doi: 10.2807/1560-7917.ES.2019.24.42.1900592
- 13
- Unemo M, Hansen M, Hadad R ym. Finnish new variant of Chlamydia trachomatis escaping detection in the Aptima Combo 2 assay also present in Orebro County, Sweden, May 2019. Euro Surveill 2019;24(26):1900370. doi: 10.2807/1560-7917.ES.2019.24.26.1900370
- 14
- Roberts DJ, Davis GS, Cole MJ ym. Prevalence of new variants of Chlamydia trachomatis escaping detection by the Aptima Combo 2 assay, England, June to August 2019. Euro Surveill 2019;24(38):1900557. doi: 10.2807/1560-7917.ES.2019.24.38.1900557
- 15
- Dahlberg J, Hadad R, Elfving K ym. Ten years transmission of the new variant of Chlamydia trachomatis in Sweden: prevalence of infections and associated complications Sex Transm Infect 2018;94:100–4.
- 16
- Papp JR, Schachter J, Gaydos CA ym. Recommendations for the laboratory-based detection of Chlamydia trachomatis and Neisseria gonorrhoeae - 2014. MMWR Recomm Rep 2014;63:1–19.
A new Finnish chlamydial variant –a challenge to molecular diagnostics
In early 2019, a discrepancy was noticed in test results for chlamydia in the Clinical Microbiology Laboratory of Turku University Hospital (Tyks). A first-void urine sample from a 32-year-old symptomatic male had been referred for analysis with a multiplex sexually transmitted infection assay and was clearly positive for Chlamydia trachomatis, although the patient had had several negative test results in the commonly used chlamydia and gonorrhoea test (Aptima Combo 2). His partner was found to be C. trachomatis positive in Tampere. Based on the findings, ‘invisible’ chlamydia was suspected in the test used by Tyks. The emergence of several cases with conflicting results led to further investigations and eventually to the discovery of a new Finnish chlamydial variant (FI-nvCT) (11 Rantakokko-Jalava K, Hokynar K, Hieta N ym. Chlamydia trachomatis samples testing falsely negative in the Aptima Combo 2 test in Finland, 2019. Euro Surveill 2019;24(22):1900298. doi: 10.2807/1560-7917.ES.2019.24.22.1900298,22 Unemo M, Getman D, Hadad R ym. Letter to the editor: Chlamydia trachomatis samples testing falsely negative in the Aptima Combo 2 test in Finland, 2019. Euro Surveill 2019;24(24):1900354. doi: 10.2807/1560-7917.ES.2019.24.24.1900354,33 Hokynar K, Rantakokko-Jalava K, Hakanen A. The Finnish new variant of Chlamydia trachomatis with a single nucleotide polymorphism in the 23S rRNA target escapes detection by the Aptima Combo 2 test. Microorganisms 2019;7:227.).