Antibioottikuurien pituus – aika päivittää hoitosuosituksia?
Lyhytkin antibioottihoito muokkaa suolen hyödyllistä mikrobistoa kuukausiksi tai vuosiksi.
Antibioottihoitoihin liittyy bakteeriresistenssin lisääntyminen ja tulevien infektioiden muuttuminen siten vaikeammin hoidettaviksi.
Mikrobiston muutos voi myös suurentaa riskiä sairastua kroonisiin tauteihin.
Etenkin toistuvien ja pitkien antibioottihoitojen suosituksia tulisi päivittää muuttuvan tiedon perusteella.
Ihminen syntyy lähes steriilinä mutta kolonisoituu bakteereilla jo synnytyskanavassa. Bakteeristo kehittyy vuorovaikutuksessa ympäristön kanssa. Se on yksilöllinen ja säilyy varsin muuttumattomana läpi elämän, jos sitä ei häiritä.
Kolmasosa suoliston bakteereista on herkkiä yleisesti käytetyille antibiooteille (1). Lyhytkin antibioottikuuri aiheuttaa dysbioosin: tilan, jossa muun muassa suoliston bakteeriston monimuotoisuus on vähentynyt. Muutos palautuu osittain jo parissa viikossa antibioottikuurin jälkeen, mutta täysin ennalleen se ei välttämättä palaa (2,3).
Kuurien määrä ja pituus vaikuttavat terveysriskeihin
Viikon mittainen makrolidikuuri kaksinkertaistaa yli vuodeksi resistenttien Haemophilusten ja streptokokkien kantajien osuuden hoitamattomiin verrattuna (4). Amoksisilliini saa aikaan saman, mutta vaikutuksen kesto lienee lyhyempi (5). Yli viikon mittainen amoksisilliini- tai trimetopriimisulfakuuri kaksinkertaistaa resistentit kannat lyhyempään kuuriin verrattuna, ja kolme kuuria vuoden aikana kolminkertaistaa kannat yhteen kuuriin verrattuna (6).
Kun resistenssi on saatu aikaan, sen hallinta on hankalaa. Resistenssigeenit voivat siirtyä bakteerista ja bakteerilajista toiseen ja aiheuttaa "geeniepidemioita" suolikanavassa (7). Väestötasolla resistenssitilanne ei välttämättä enää korjaudu, vaikka valintapainetta pienennettäisiin antibioottien käyttöä vähentämällä (8).
Antibioottihoidon seurauksena ilmaantuu vaikeammin hoidettavia resistenttien bakteerien aiheuttamia infektioita, superinfektioita sekä elimistön immunologisten ja metabolisten toimintojen muutoksia. Sairaaloissa yli kahden päivän profylaksin on todettu lisäävän potilaiden kolonisoitumista resistenteillä mikrobeilla (9) ja on myös viitteitä siitä, että kirurgiaan liittyvien infektioiden riski kasvaa (10,11). Avohoidossa yli viikon mittainen kefalosporiini- tai fluorokinolonihoito voi viisinkertaistaa Clostridium difficile -infektioiden riskin lyhyempään hoitoon verrattuna (12) ja tiheät tai pitkät antibioottikuurit voivat lisätä välikorvatulehduksen ja säärihaavojen uusimisriskiä (13).
Varhaislapsuuden antibioottikuurien on raportoitu lisäävän lapsen riskiä sairastua lihavuuteen (14) tai atopiaan (2), ja riski suurenee saatujen antibioottien määrän kasvaessa. Dysbioosin on väitetty myös olevan yhteydessä autoimmuunisairauksia ja valtimotautia suosiviin muutoksiin elimistössä (1,2,15), mutta selvän kausaliteetin osoittaminen vaatisi aikuisikään ulottuvan seurantatutkimuksen.
Lyhyempikin kuuri voi riittää
Huoli antibioottihoitojen haitoista on katalysoinut tutkimuksia, joissa on pyritty kartoittamaan totuttua lyhyempien antibioottikuurien hyötyjä ja haittoja infektioiden hoidossa. Hengitystieinfektioissa lyhyempien kuurien havaittiin odotetusti johtavan antibioottien käytön vähentymiseen ilman esiin tulleita haittoja (16). Välikorvatulehduksen (17), virtsatietulehduksen (18) ja ihoinfektioiden hoidossa (19) on lisäksi tutkittu hoitolinjausta, jossa on tukeuduttu antibioottihoitoon vasta oireenmukaisen hoidon jälkeen vaikeutuvissa tai pitkittyvissä infektioissa. Tämäkin hoitolinjaus vähensi antibioottien käyttöä ilman havaittuja riskejä.
Teho-osastojen infektioissa hoitoja on onnistuttu laboratorioseurannan avulla yksilöllisesti lyhentämään (20). Sen sijaan avohoidon infektioita hoidettaessa on vaikeaa arvioida sopivaa hetkeä lopettaa antibioottikuuri. Laboratoriotutkimuksista tai kuvantamisista ei avohoidossa ole tässä juuri hyötyä. Päivitetyt ja ajantasaiset hoitosuositukset ovat tällöin avainasemassa hoidon ohjauksessa.
Paineita suositusten laatijoilla ja päivittäjillä
Kansallisia, tutkimusnäyttöön perustuvia Käypä hoito -suosituksia on laadittu jo kahden vuosikymmenen ajan. Suosituksia laaditaan terveydenhuollon ammattilaisista koostuvin vapaaehtoisvoimin, ja niistä on tullut tärkeä potilaita hoitavan työkalu. Yksi ajantasaisten suositusten laatimisen haasteista kuitenkin on, että tutkimustieto lisääntyy jatkuvasti mutta suosituksia päivitetään vuosien välein.
On painetta reagoida entistä enemmän lisääntyvään mikrobien resistenssiin sekä uusiin todettuihin ja epäiltyihin antibioottien tuomiin yleisen terveyden uhkiin. Mikrobien antibioottiherkyys on luokiteltu "luonnonvaraksi", johon tulevilla sukupolvilla on yhtäläinen nautintaoikeus nykyisten kanssa (ns. Locken provisio vuodelta 1672) (21). Useassa antibioottien käyttöaiheessa ollaankin parhaillaan tutkimuksin hakemassa lyhintä tehokasta hoitoaikaa tai hoidon aloituksissa entistä suurempaa pidättyvyyttä.
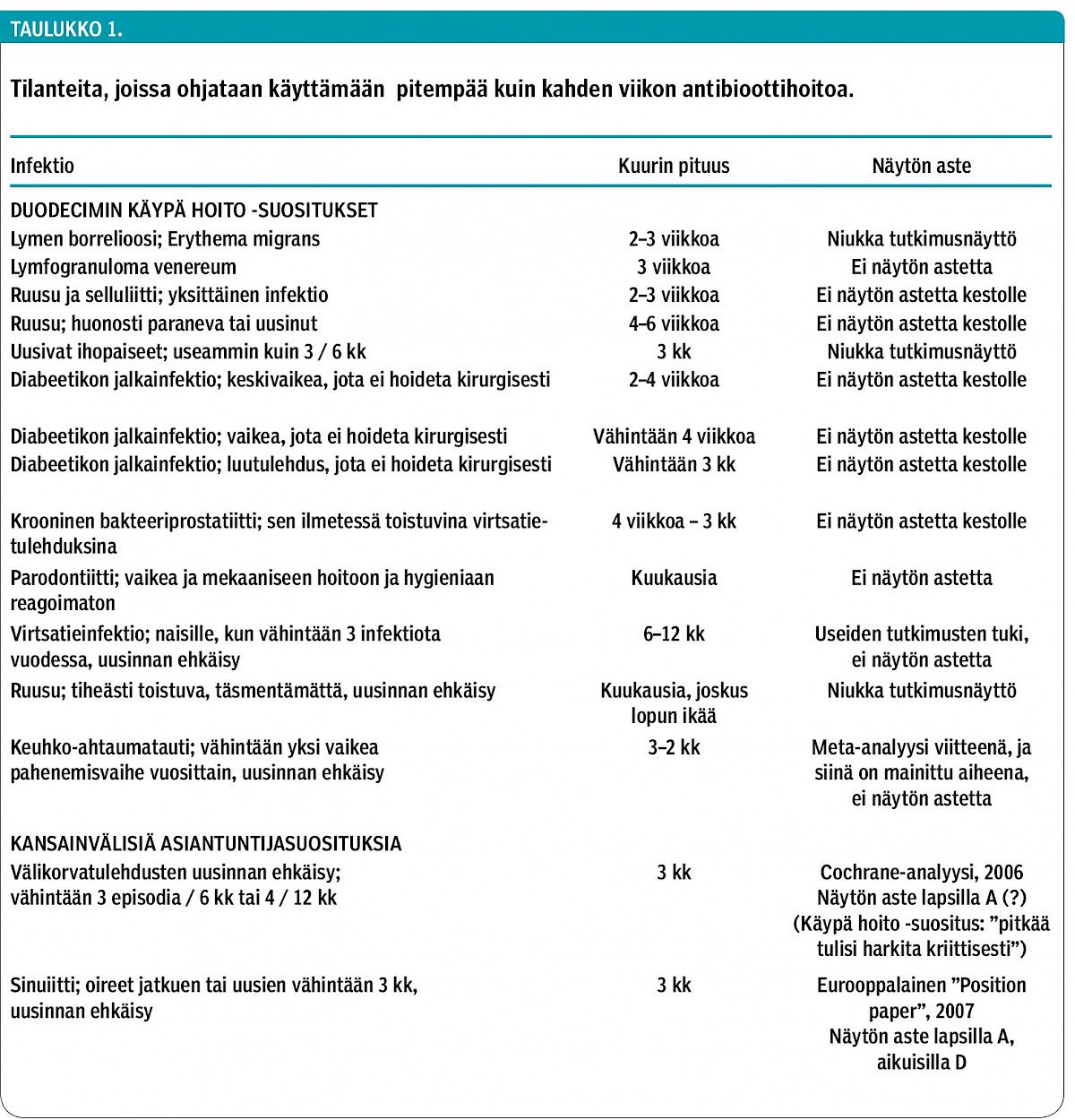
Tulevaisuuden resistenssiuhka on jo huomioitu useassa hoitosuosituksessa. Joihinkin infektioihin suositetaan kuitenkin yhä viikkojen hoitokuureja, mutta niitä puoltava tutkimusnäyttö on rajallista (taulukko 1). Joidenkin indikaatioiden, kuten keuhkoahtaumataudin pahenemisvaiheiden ehkäisyn (22) ja diabeetikkojen jalkainfektioiden (23), yhteydessä uusi tutkimustieto ja siihen perustuvat kansainväliset suositukset tukevat jo entistä pidättyvämpää antibioottien käyttöä tai lyhyempiä hoitoja.
Lopuksi
Antibiootit ovat kuuluneet ja kuuluvat yhä eniten terveyttä tuoneisiin ja ihmishenkiä säästäneisiin lääkkeisiin (24). Kansainväliset hoitosuositukset ovat parhaillaan päivittymässä, ja yleistrendinä on pitkien antibioottihoitojen lyhentyminen.
Siihen asti että kansalliset hoitosuosituksemme pitkien antibioottihoitojen suhteen päivittyvät, on yksittäisen suomalaisen lääkärin kuitenkin edelleen hyvä noudattaa kansallisia hoitosuosituksiamme tai tarvittaessa neuvotella kuurin sopivasta pituudesta infektiolääkärin kanssa. Tärkeintä silti on, ettei antibioottihoitoa lainkaan aloiteta, jos ei ole perusteltua odottaa sen hyödyttävän potilasta (25).
Ei sidonnaisuuksia.
- 1
- Francino MP. Antibiotics and the human gut microbiome: dysbioses and accumulation of resistances. Front Microbiol 2016;6:1543. doi: 10.3389/fmicb.2015.01543.
- 2
- Korpela K, Salonen A, Virta LJ ym. Intestinal microbiome is related to lifetime antibiotic use in Finnish pre-school children. Nat Commun 2016;7:10410. doi: 10.1038/ncomms10410.
- 3
- Dethlefsen L, Relman DA. Incomplete recovery and individualized responses of the human distal gut microbiota to repeated antibiotic perturbation. Proc Natl Acad Sci U S A 2011;108 (Suppl 1):4554–61.
- 4
- Chung A, Perera R, Brueggemann AB ym. Effect of antibiotic prescribing on antibiotic resistance in individual children in primary care: prospective cohort study. BMJ 2007;335:429 doi:10.1136/bmj.39274.64/465.BE.
- 5
- Malhotra-Kumar S, Lammens C, Coenen S, Van Herck K, Goossens H. Effect of azithromycin and clarithromycin therapy on pharyngeal carriage of macrolide-resistant streptococci in healthy volunteers: a randomised, double-blind, placebo-controlled study. Lancet 2007;369:482–90.
- 6
- Costelloe C, Metcalfe C, Lovering A, Mant D, Hay AD. Effect of antibiotic prescribing in primary care on antimicrobial resistance in individual patients: systematic review and meta-analysis. BMJ 2010;340:c2096. doi: 10.1136/bmj.c2096.
- 7
- van Schaik W. The human gut resistome. Philos Trans R Soc Lond B Biol Sci 5;370:20140087. doi: 10.1098/rstb.2014.0087.
- 8
- MacLean RC, Vogwill T. Limits to compensatory adaptation and the persistence of antibiotic resistance in pathogenic bacteria. Evol Med Public Health 2015;(1):4-12.
- 9
- Harbarth S, Samore MH, Lichtenberg D, Carmeli Y. Prolonged antibiotic prophylaxis after cardiovascular surgery and its effect on surgical site infections and antimicrobial resistance. Circulation 2000;101:2916–21.
- 10
- Namias N, Harvill S, Ball S, McKenney MG, Salomone JP, Civetta JM. Cost and morbidity associated with antibiotic prophylaxis in the ICU. J Am Coll Surg 1999;188:225–30.
- 11
- Zhow L, Ma J, Gao J, Chen S, Bao J. Optimizing prophylactic antibiotic practice for cardiothoracic surgery by pharmacists’ effects. Medicine 2016;95(9):e2753. doi: 10.1097/MD.0000000000002753
- 12
- Dubberke ER, Reske KA, Yan Y, Olsen MA, McDonald LC, Fraser VJ. Clostridium difficile--associated disease in a setting of endemicity: identification of novel risk factors. Clin Infect Dis 2007;45:1543–9.
- 13
- O’Meara S, Al-Kurdi D, Ologun Y, Ovington LG, Martyn-St James M, Richardson R. Antibiotics and antiseptics for venous leg ulcers. Cochrane Database Syst Rev 2014;1:CD003557. doi: 10.1002/14651858.CD003557.
- 14
- Saari A, Virta LJ, Sankilampi U, Dunkel L, Saxen H. Antibiotic exposure in infancy and risk of being overweight in the first 24 months of life. Pediatrics 2015;135:617–26.
- 15
- Marchesi JR, Adams DH, Fava F, ym. The gut microbiota and host health: a new clinical frontier. Gut 2016;65:330-9.
- 16
- Greenberg D, Givon-Lavi N, Sadaka Y, Ben-Shimol S, Bar-Ziv J, Dagan R. Short-course antibiotic treatment for community-acquired alveolar pneumonia in ambulatory children: a double-blind, randomized, placebo-controlled trial. Pediatr Infect Dis J 2014;33:136–42.
- 17
- Tapiainen T, Kujala T, Renko M ym. Effect of antimicrobial treatment of acute otitis media on the daily disappearance of middle ear effusion: a placebo-controlled trial. JAMA Pediatr 2014;168:635–41.
- 18
- Gágyor I, Bleidorn J, Kochen MM, Schmiemann G, Wegscheider K, Hummers-Pradier E. Ibuprofen versus fosfomycin for uncomplicated urinary tract infection in women: randomised controlled trial. BMJ 2015;351:h6544. doi: 10.1136/bmj.h6544.
- 19
- Talan DA, Mower WR, Krishnadasan A ym. Trimethoprim-sulfamethoxazole versus placebo for uncomplicated skin abscess. N Engl J Med 2016;374:823–32.
- 20
- Maseda E, Suarez-de-la-Rica A, Anillo V ym. Procalcitonin-guided therapy may reduce length of antibiotic treatment in intensive care unit patients with secondary peritonitis: A multicenter retrospective study. J Crit Care 2015;30:537–42.
- 21
- Leibovici L, Paul M, Ezra O. Ethical dilemmas in antibiotic treatment. J Antimicrob Chemother 2012;67:12-6.
- 22
- Taylor SP, Sellers E, Taylor BT. Azithromycin for the prevention of COPD exacerbations: the good, bad, and ugly. Am J Med 2015;128:1362.e 1–6.
- 23
- Lipsky BA, Aragón-Sánchez J, Diggle M ym. IWGDF guidance on the diagnosis and management of foot infections in persons with diabetes. Diabetes Metab Res Rev 2016;32(Suppl. 1):45–74.
- 24
- Owens RC Jr. Antimicrobial stewardship: concepts and strategies in the 21st century. Diagn Microbiol Infect Dis 2008;61:110–28.
- 25
- Huttunen R, Syrjänen J, Vuento R. Milloin antibioottihoito ei ole tarpeen? Suom Lääkäril 2015;70:2065–72.