Käden digitaalinen radiogrammetria murtumapotilaan osteoporoosiriskin arvioinnissa
LÄHTÖKOHDAT Osteoporoosin seulonnan murtumapotilailta tulisi olla tehokasta ja nopeaa. Digitaalisella radiogrammetrialla (DXR) voidaan määrittää tavallisesta röntgenkuvasta kämmenluiden mineraalitiheys.
MENETELMÄT 160 naispuoliselle murtumapotilaalle (ikä 50–74 vuotta) tehtiin DXR ja laskettiin murtumariskin FRAX-arvo. Potilaille (n = 116), joilla todettiin DXR-tutkimuksessa osteopenia tai osteoporoosi, tehtiin myös sentraalinen DXA (kaksienergiainen röntgenabsorptiometria).
TULOKSET DXR-tutkimuksen tulos ja murtumariskin FRAX-arvo korreloivat kohtalaisesti (r = 0,47; p < 0,001). DXR-tuloksen raja-arvo T = –1 SD tunnisti suurentuneen FRAX-arvon (≥ 10 %) 91 %:n sensitiivisyydellä ja 52 %:n spesifisyydellä. FRAX-seulonnalla ilman DXR-tutkimusta luuntiheyden varmistus DXA:lla olisi tarvittu 110 potilaalle 160:stä. Jos DXA tehtäisiin vain niille, joilla oli DXR:n perusteella osteopenia ja joilla FRAX-arvo oli 10–19 %, DXA olisi tarpeellinen enää 38 potilaalle.
PÄÄTELMÄT Pelkkään FRAX-seulontaan verrattuna DXR-tutkimus ja sen perusteella osteopeenisille tehty FRAX-arvon laskenta vähentävät tehokkaasti tarvetta DXA:lle, joka on raskaampi ja kalliimpi tutkimus.

Määritelmän mukaan osteoporoosissa kaksienergiaisella röntgenabsorptiometrialla (DXA) mitattu reisiluun yläosan tai lannerangan mineraalitiheys on pienentynyt vähintään 2,5 keskihajonnan (SD) verran vertailuaineistoon nähden (DXA T-arvo ≤ –2,5 SD). Osteoporoosin primaariseulontaan tarvitaan kuitenkin DXA-tutkimusta keveämpiä menetelmiä.
Esimerkiksi kliinisiä riski-indeksejä voidaan käyttää apuna murtumariskin ja DXA-jatkotutkimusten tarpeen arvioimisessa. Suomessa on käytetty Mikkelin osteoporoosi-indeksiä (MOI), ja nykyään käytetään etenkin kansainvälistä FRAX-riskilaskuria (1). Yksinkertaisempi MOI oli käytössä Mikkelin keskussairaalassa murtumapotilaiden primaariseulana vuosina 2004–2014 ja FRAX on ollut käytössä vuodesta 2014. FRAX-tietojen kirjaus on kuitenkin ollut epäluotettavaa vuodeosaston ja ensiavun kiireessä (2).
Osteoporoosin seulonnassa voidaan käyttää myös perifeerisiä luuntiheysmittauksia, kuten perifeerisiä DXA- ja kaikututkimuksia (3,4). Jos sentraalista DXA-tutkimusta ei ole saatavilla, hoito voidaan aloittaa esimerkiksi ranteen DXA:n ja kliinisen riskiarvion perusteella (4). Perifeeristen tiheysmittausten sensitiivisyys tunnistaa osteoporoosi vaihtelee eri menetelmien välillä (5).
Digitaalinen radiogrammetria (DXR) on perifeerinen luuntiheysmittaus, joka toteutuu joustavasti murtuman röntgenkuvauksen yhteydessä. Siinä määritetään kämmenluiden (MC II–IV) mineraalitiheys luun leveyden ja kuoriluun paksuuden ja huokoisuuden perusteella käden tavallisesta digitaalisesta röntgenkuvasta (6).
Menetelmällä määritetty kämmenluiden mineraalitiheys korreloi hyvin DXA:lla mitatun värttinäluun mineraalitiheyden kanssa (r = 0,82–0,86) (6,7). Reisiluun kaulan mineraalitiheyden kanssa se korreloi kohtalaisesti (r = 0,65) (8). DXR-tutkimuksen toistettavuus on parempi (vaihtelu 0,14–0,44 %) kuin lonkan tai selän DXA-tutkimusten (vaihtelu 1,6–1,9 %) (9,10,11). DXR tunnistaa reisiluun kaulan osteoporoosin paremmin kuin FRAX ja lisäksi se ennustaa sekä lonkka- että muita osteoporoosimurtumia yhtä hyvin kuin FRAX (12).
DXR-tutkimus otettiin Mikkelin keskussairaalassa käyttöön murtumapotilaiden primaariseulana 1.11.2016. Tässä tutkimuksessa verrattiin DXR-seulontatutkimuksen tuloksia ensimmäisen kuuden kuukauden ajalta FRAX-seulonnan tuloksiin pienienergiaisen murtuman saaneilla naisilla. Tavoitteena oli verrata näiden kahden seulontamenetelmän kykyä luokitella potilaat riskiryhmiin sekä selvittää, vähentääkö DXR:n käyttö DXA-jatkotutkimusten tarvetta.
Aineisto ja menetelmät
Tutkimukseen otettiin mukaan 50–74-vuotiaat naiset, joita hoidettiin Mikkelin keskussairaalassa pienienergiaisen murtuman takia talvikaudella 1.11.2016–30.4.2017. Murtuman kokeneilla yli 75-vuotiailla naisilla hoito voidaan aloittaa ilman luuntiheysmittausta suuren FRAX-lonkkamurtumariskiarvon perusteella (1), joten heidät suljettiin pois tutkimuksesta. Tutkimuksella on Etelä-Savon sairaanhoitopiirin tutkimuslupa, ja potilaat antoivat siihen kirjallisen suostumuksensa.
Kun potilas tuli murtuman vuoksi röntgentutkimukseen, häneltä otettiin samalla käden PA-suuntainen röntgenkuva DXR-tutkimusta varten (kuvausetäisyys 115 cm, putkijännite 52 kV, sähkömäärä 1,2 mAs, efektiivinen sädeannos < 0,001 mSv). Kuva otettiin pääsääntöisesti vasemmasta, ei-dominantista kädestä. Jos vasemman yläraajan murtuma esti DXR-tutkimuksen tai murtuman kuvaus viivästyi yli 2 viikkoa, kuva otettiin oikeasta kädestä, jotta mahdollinen immobilisaatio-osteoporoosi ei vääristäisi tulosta.
Kuva lähetettiin pilvipalvelun kautta ilman potilastietoja Ruotsiin analysoitavaksi DXR-analyysiohjelmalla (OneScreen Osteoporosis Package, Sectra AB, Linköping, Ruotsi). Analyysin tarkisti sikäläinen sairaalafyysikko, ja vastaus saatiin 1–3 päivän kuluessa. Lisäksi kaikille potilaille tehtiin painoindeksin huomioiva FRAX-riskilaskenta (FRAX-BMI). DXA-tutkimus (Lunar Prodigy, GE Healthcare / Terveystalo, Mikkeli) tehtiin vain potilaille, joilla oli DXR-tutkimuksen perusteella osteopenia tai osteoporoosi (T-arvo oli < –1 SD) (kuvio 1).
Receiver operating characteristic -analyysillä (ROC) tutkittiin sekä DXR:n että FRAX:n kykyä tunnistaa reisiluun kaulan osteoporoosi. Lisäksi tutkittiin murtumariskin FRAX-arvon ja DXR T -arvon välistä suhdetta (Pearsonin korrelaatio ja ROC-analyysi) sekä arvioitiin DXR:n tuomia laskennallisia säästöjä DXA-jatkotutkimuksissa. Tilastoanalyysit tehtiin SPSS-ohjelmistolla.
Tulokset
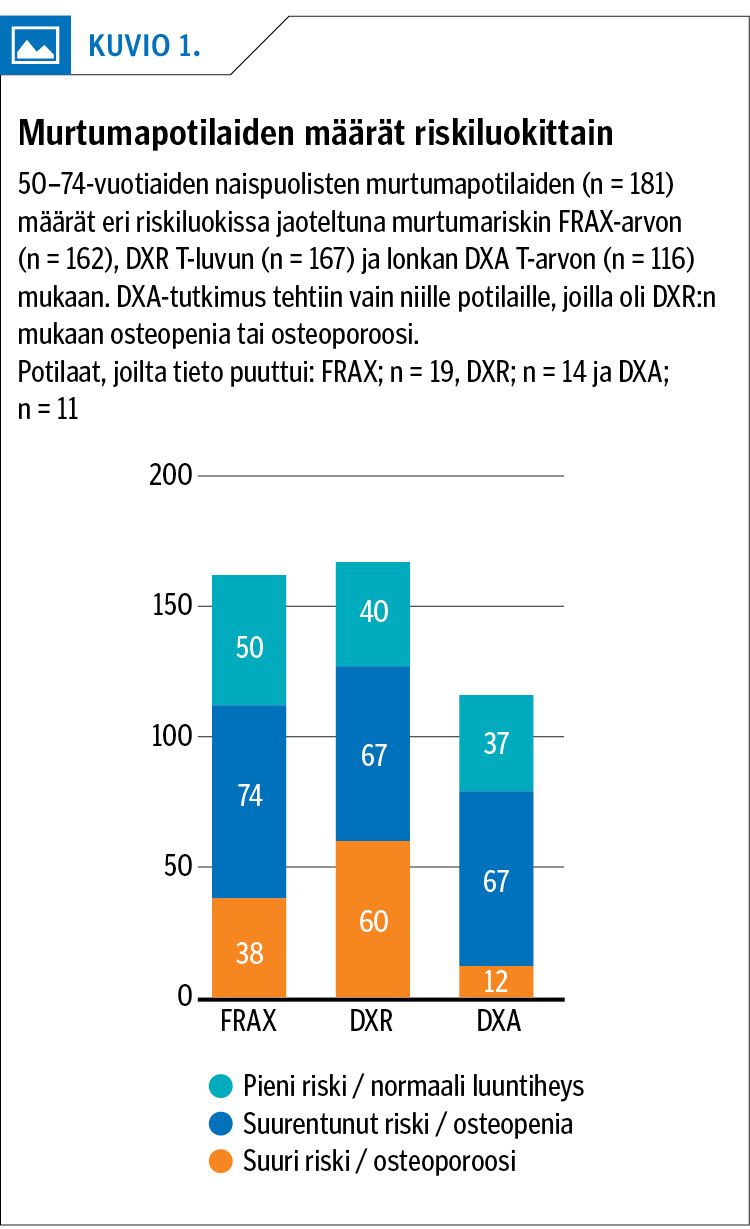
181 murtumapotilaasta DXR-tutkimus toteutui 167:llä, FRAX-laskenta 162:lla, molemmat 160:llä ja DXA-tutkimus 116:lla. Vastaavasti tutkimus jäi puuttumaan 14, 19 ja 11 potilaalta (kuvio 1). Keskimääräisissä riskiluokkajakaumissa ei ollut eroa tutkittujen ja pudokkaiden välillä. Murtumista 87 oli ranne-, 37 olka-, 26 nilkka-, 6 lonkka- ja 25 muita murtumia.
167 DXR-kuvauksesta 128 tehtiin ensimmäisen 2 viikon kuluessa murtumasta, 36 tehtiin viikoilla 3–12 ja 3 tehtiin myöhemmin kuin 12 viikon kuluttua. Tyypillisesti DXR-tutkimus tehtiin murtumakuvauksen yhteydessä, ja vain neljä potilasta kutsuttiin erilliselle kuvauskäynnille. Kuvauksista 114 tehtiin vasemmasta ja 53 oikeasta kädestä.
DXR-tutkimuksella osteoporoosi todettiin 36 %:lla potilaista ja osteopenia 40 %:lla potilaista. Vastaavasti suuri murtumariskin FRAX-arvo (FRAX-BMI ≥ 20 %) (13) todettiin 23 %:lla ja suurentunut FRAX-arvo (FRAX-BMI 10–19 %) 46 %:lla potilaista. DXA:lla tutkituista osteoporoosi todettiin 10 %:lla ja osteopenia 58 %:lla (kuvio 1).
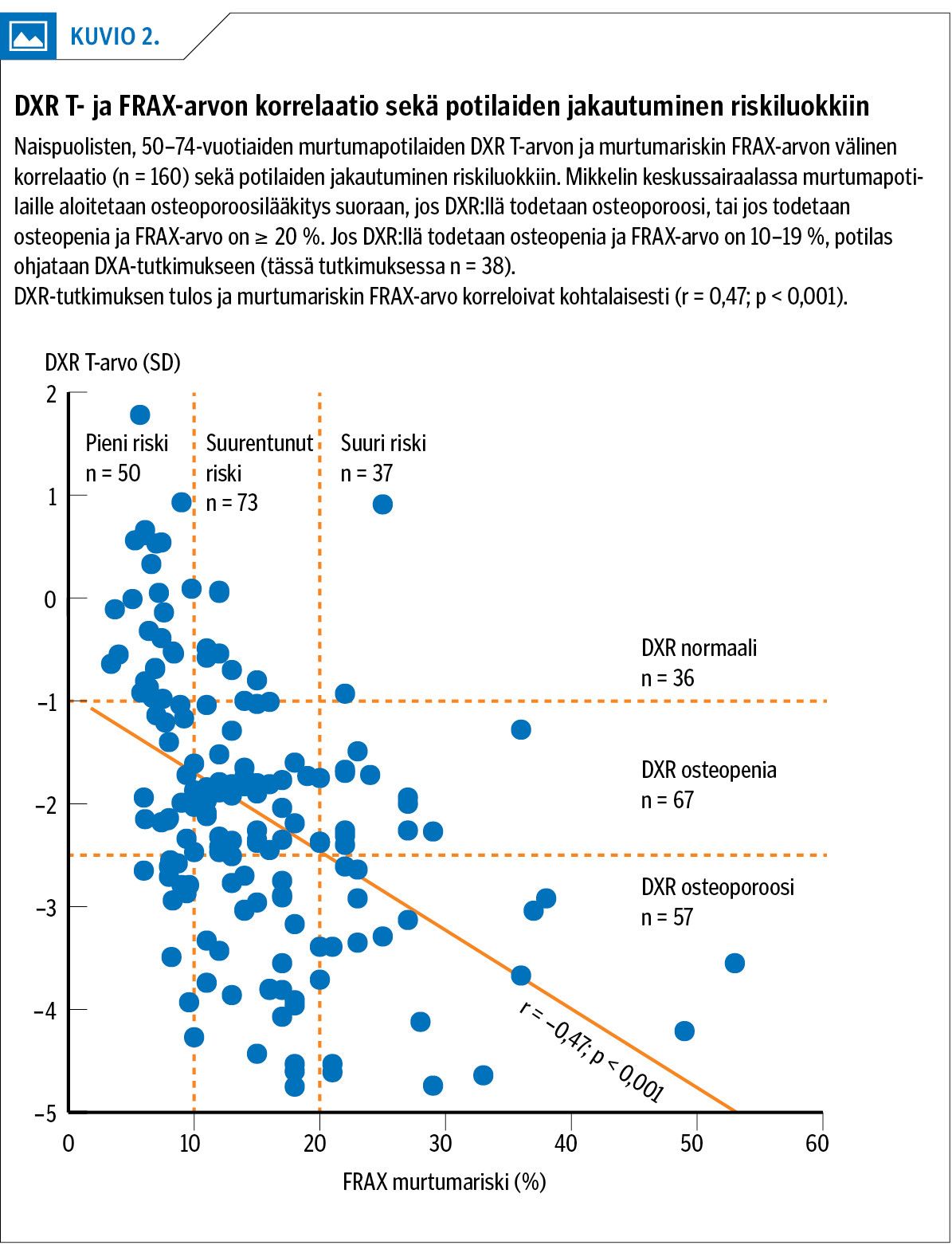
Seulontaryhmittely DXR T-arvojen ja murtumariskin FRAX-arvon mukaan on esitetty kuviossa 2. Sen pohjalta arvioitiin DXA-jatkotutkimusten määrällinen tarve eri seulontamenetelmiä käytettäessä. Jos primaariseulana olisi FRAX, luuntiheyden varmistus DXA:lla tarvittaisiin 160 potilaasta niille 110:lle, joilla on suurentunut (n = 73) tai suuri (n = 37) FRAX-riskiarvo.
Jos seulonta aloitettaisiin DXR:llä ja FRAX-laskenta kohdistettaisiin niille, jotka ovat DXR:n mukaan osteopeenisia, FRAX-laskenta olisi tarpeen vain 67:lle 160 potilaasta. Jos sen jälkeen DXA kohdistettaisiin vain niille potilaille, jotka ovat DXR:n mukaan osteopeenisia ja joilla FRAX-arvo on 10–19 %, DXA-tutkimusta tarvittaisiin vain 38 potilaalle 160:stä (24 %).
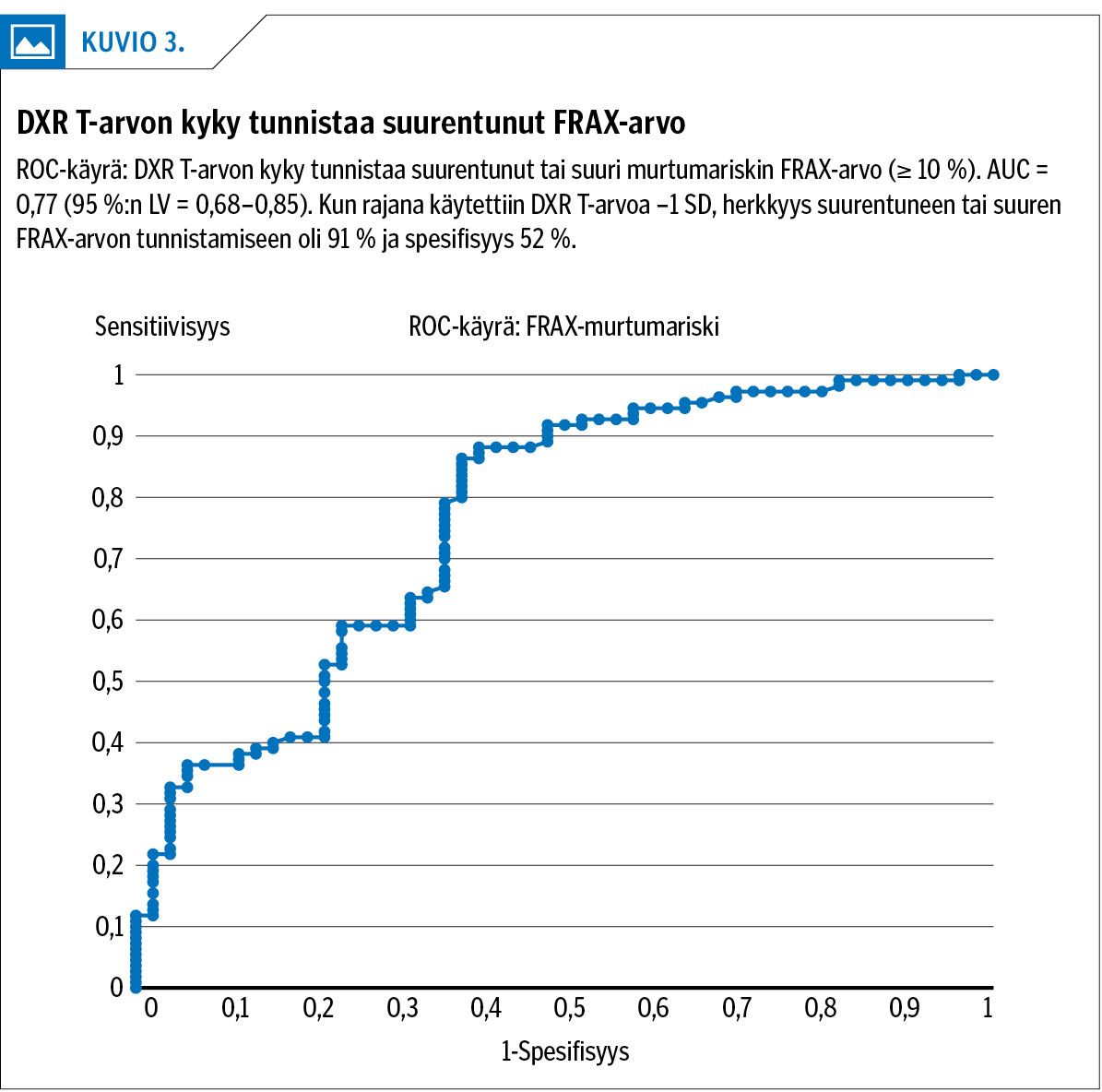
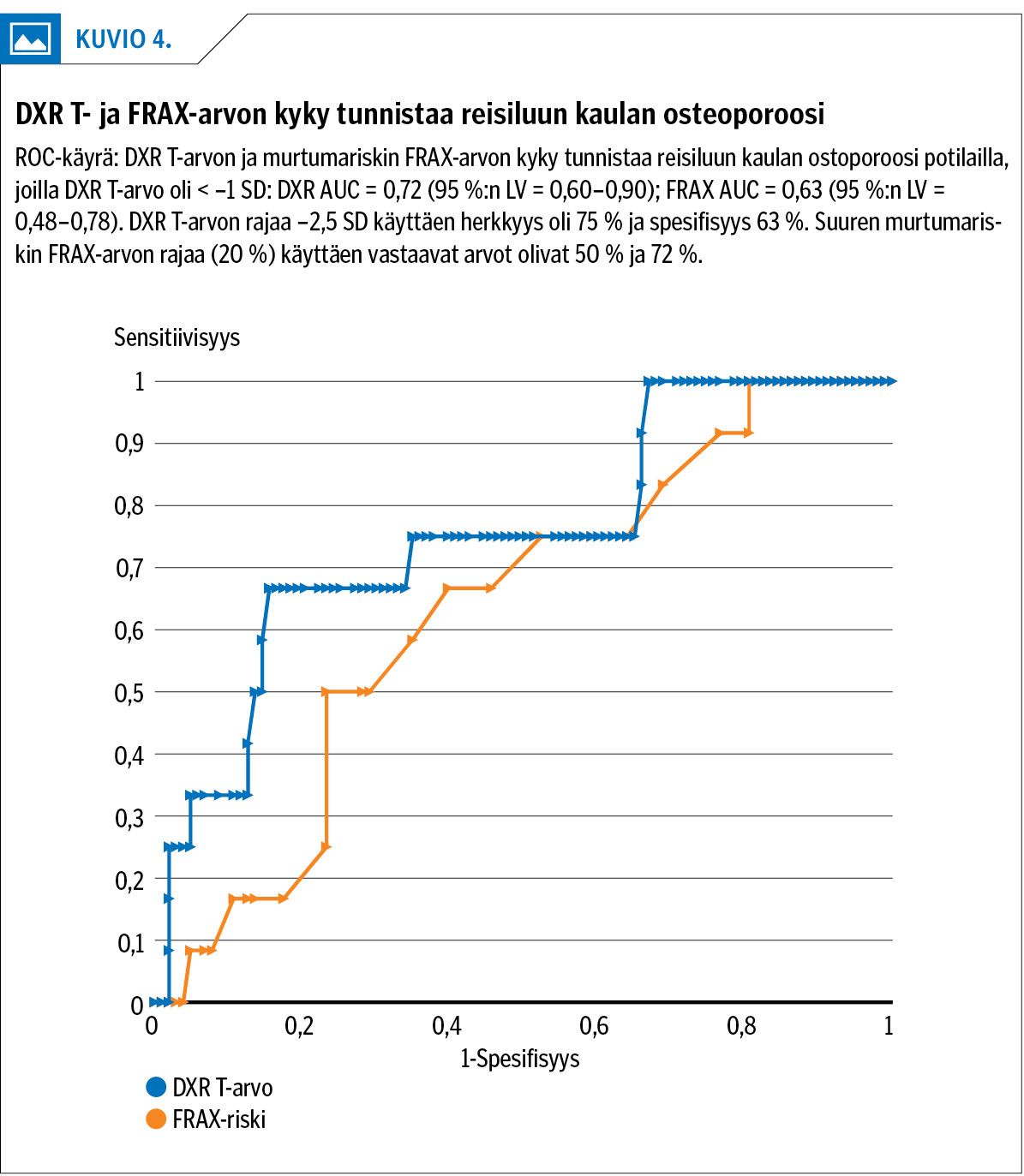
ROC-analyysin perusteella suurentunut FRAX-arvo (≥ 10 %) tunnistettiin DXR:ssä osteopenian raja-arvoa (T-arvo = –1 SD) käyttäen 91 %:n sensitiivisyydellä (spesifisyys 52 %; AUC 0,77; 95 %:n LV = 0,68–0,85) (kuvio 3). Potilailla, joilla DXR-arvo oli alle –1 SD, DXR tunnisti osteoporoosin FRAX-laskentaa paremmin (DXR AUC = 0,75 ja FRAX AUC = 0,63) (kuvio 4).
Päätelmät
Yhdysvaltojen kansallinen osteoporoosityöryhmä (NBHA) on ehdottanut, että osteoporoosin diagnoosi voidaan hyväksyä seuraavissa tilanteissa: 1) lonkan tai lannerangan DXA T-arvo ≤ –2,5 SD, 2) lonkan murtuma ilman DXA-tutkimusta, 3) selän, lantion ja olkaluun yläosan murtumat sekä osin myös rannemurtumat, kun potilaalla on osteopenia, 4) FRAX-arvo ≥ 20 % (13).
Mikkelin keskussairaala soveltaa tätä suositusta: kun perifeerisen murtuman saaneella potilaalla on osteopenia DXR:n perusteella ja suurentunut FRAX-arvo (10–19 %), diagnoosi varmistetaan sentraalisella DXA:lla. Murtumapotilaan hoito aloitetaan ilman DXA-tutkimusta, jos hänellä todetaan DXR-tutkimuksessa osteoporoosi, tai jos todetaan osteopenia yhdessä suuren FRAX-arvon (≥ 20 %) kanssa.
Ruotsalaisessa murtumapotilaiden seurantatutkimuksessa lonkkamurtumien esiintyvyys oli kaksinkertainen niillä naisilla, joilla oli jo DXR:n perusteella osteopenia verrattuna naisiin, joilla DXR oli normaali. Lonkkamurtumien esiintyvyys oli suuri niillä 55–85-vuotiailla, joilla oli DXR:n perusteella osteoporoosi (1,6 % /vuosi) (14).
Sentraalisessa DXA-tutkimuksessa määritetään reisiluun kaulan ja trokanter-alueen tai lannerangan mineraalitiheys. DXR-tutkimus taas määrittelee kämmenluiden mineraalitiheyden digitaalisesta röntgenkuvasta. FRAX-laskurilla puolestaan arvioidaan murtumariskiä eikä luun mineraalitiheyttä. Mittareilla ei täten välttämättä ole suoraa korrelaatiota, mutta sekä DXR-tutkimusta että FRAX-riskiarviointia voidaan käyttää määritettäessä DXA-jatkotutkimuksen tarvetta. Alle 65-vuotiailla FRAX-laskurin kyky tunnistaa reisiluun kaulan osteoporoosi on huonohko (AUC-arvo noin 0,6) (15). Heillä DXA-tutkimuksen tarve voidaan tunnistaa myös yksinkertaisemmilla kliinisillä indekseillä tai perifeerisellä luuntiheysmittauksella (3,4,16).
FRAX-riskilaskenta on tärkeä määritettäessä osteoporoosin hoitokynnystä, sillä kliinisten riskitekijöiden huomioiminen lisää tunnistuksen herkkyyttä (hoidosta hyötyvien potilaiden määrää) vähentämättä spesifisyyttä (lisäämättä tarpeettomia hoitoja) (17).
Norjalaisessa potilasaineistossa DXR T-arvo –1,2 SD tunnisti reisiluun kaulan osteoporoosin 90 %:n herkkyydellä sekä murtumapotilailla että väestöverrokeilla (8). Tämän vuoksi suljimme pois DXA-tutkimuksesta potilaat, joilla DXR T-arvo oli suurempi kuin –1 SD.
Tässä tutkimuksessa DXR-tulos korreloi kohtalaisesti murtumariskin FRAX-arvon kanssa ja tunnisti hyvin suurentuneen FRAX-arvon (≥ 10 %). Niillä potilailla, joille DXA-tutkimus tehtiin, DXR tunnisti reisiluun kaulan osteoporoosin paremmin kuin FRAX. Koska DXR:ssä normaalin tuloksen saaneille potilaille ei tehty DXA-tutkimusta, heidän osuutensa ei näy tutkimuksessa tehdyissä tilastollisissa analyyseissä. Näistä potilaista vain kahdella todettiin suuri ja kahdeksalla suurentunut murtumariski FRAX-laskennalla (kuvio 2).
Pelkkään FRAX-seulontaan verrattuna ensin DXR:llä ja sitten FRAX:lla tehty seulonta voisi vähentää tehokkaasti raskaamman ja kalliimman DXA-tutkimuksen tarvetta. DXR:n käyttäminen primaariseulana pienentää myös osteoporoosihoitajan työtaakkaa: FRAX-seulontojen (á 10–15 min) määrä käytännössä puolittuu, ja säästyneen työajan voi käyttää potilasvirtojen hallinnan tehostamiseen. Murtuman röntgenkuvauksen yhteydessä tehty käden DXR-tutkimus vie aikaa vain 1–2 minuuttia. Kuvaus on helposti saatavilla eikä vaadi röntgenhoitajalta pitkää perehdytystä. Haittapuolena on ionisoivan säteilyn käyttö, mutta potilaan saama efektiivinen sädeannos on hyvin pieni.
Murtuman hoidosta vastaava lääkäri saa DXR-tutkimuksella valtaosalla potilaista tiedon luuntiheydestä jo murtuman hoidon ensi viikkoina, ja voi tarvittaessa aloittaa luustolääkityksen. Tämä on parantanut myös koulutettavien murtumakirurgien tietoa osteoporoosista ja saanut heidät ottamaan lisää vastuuta hoidosta.
Toivomme myös potilaiden sitoutuvan paremmin hoitamaan osteoporoosiaan, kun he saavat tiedon luuntiheydestään jo murtuman yhteydessä. Nyt, kaksi vuotta menetelmää käytettyämme osteoporoosihoitajamme (AK) onkin todennut:
"DXR on mullistanut osteoporoosiseulamme. Olen kuin lennonjohtaja, joka monitorista valvoo ohjelmoitua lentoon nousua (prosessin etenemistä potilastietojärjestelmässä ja PACS:ssa) ja turvallista laskeutumista (hoidon toteutumista)."
Pekka Waris, Pia Linder, Arja Kuukka, Petteri Saarinen, ja Ville Waris: Ei sidonnaisuuksia.
Joonas Sirola: Käypä hoito (Osteoporoosi) -työryhmän jäsen, Luustoliiton hallituksen jäsen.
Tämä tiedettiin
Murtumapotilaiden osteoporoosin ja murtumariskin arviointi toteutuu maassamme edelleen huonosti.
Arviontiin voidaan käyttää perifeerisiä luuntiheysmittauksia ja murtumariskin laskentaa. Niitä käyttämällä raskaamman ja kalliimman DXA-tutkimuksen tarve puolittuu.
tutkimus opetti
Käden luuntiheyden DXR-tutkimuksessa osteopenian raja-arvo T = –1 SD tunnisti suurentuneen FRAX-riskiarvon (≥ 10 %) 91 %:n sensitiivisyydellä ja 52 %:n spesifisyydellä.
Niillä potilailla, joilla oli DXR:n perusteella pienentynyt luuntiheys, DXR tunnisti reisiluun kaulan osteoporoosin paremmin kuin kansainvälinen FRAX-riskilaskuri.
Murtumapotilaiden DXA-tutkimuksen tarve väheni neljäsosaan, kun alkuseulonta tehtiin DXR:llä, jatkoseulonta osteopeenisille FRAX:lla ja DXA-tutkimus ainoastaan niille, joilla FRAX-riskiarvo oli suurentunut (10–19 %).
- 1
- Suomalaisen Lääkäriseuran Duodecimin ja Suomen Ortopediyhdistyksen asettama työryhmä. Lonkkamurtuma. Käypä hoito -suositus 27.5.2018. www.kaypahoito.fi
- 2
- Waris V, Aarnio J, Saarinen P, Sirola J, Waris P, Käden digitaalinen luuntiheysmittaus (DXR-BMD) murtumapotilaan FRAX-riskin arvioinnissa ja hoidossa Mikkelin keskussairaalassa. Suom Ortop ja Traumatol 2017;40:160–3.
- 3
- Karjalainen JP, Riekkinen O, Kröger H. Pulse-echo ultrasound method for detection of post-menopausal women with osteoporotic BMD. Osteoporos Int 2018;29:1193–9.
- 4
- Hans DB, Shepherd JA, Schwartz EN ym. Peripheral dual-energy X-ray absorptiometry in the management of osteoporosis: the 2007 ISCD Official Positions. J Clin Densitom 2008;11:188–206.
- 5
- Boonen S, Nijs J, Borghs H, Peeters H, Vanderschueren D, Luyten FP. Identifying postmenopausal women with osteoporosis by calcaneal ultrasound, metacarpal digital X-ray radiogrammetry and phalangeal radiographic absorptiometry: A comparative study. Osteoporos Int 2005;16:93–100.
- 6
- Rosholm A, Hyldstrup L, Backsgaard L, Grunkin M, Thodberg HH. Estimation of bone mineral density by digital X-ray radiogrammetry: theoretical background and clinical testing. Osteoporos Int 2001;12:961–9.
- 7
- Forsblad D, Elia H, Carlsten H. Bone mineral density by digital X-ray radiogrammetry is strongly decreased and associated with joint destruction in long-standing Rheumatoid Arthritis: A cross-sectional study. BMC Musculoskelet Disord 2011;12:242. doi: 10.1186/1471-2474-12-242.
- 8
- Dhainaut A, Rohde GE, Syversen U, Johnsen V, Haugeberg G. The ability of hand digital X-ray radiogrammetry to identify middle-aged and elderly women with reduced bone density, as assessed by femoral neck dual-energy X-ray absorptiometry. J Clin Densitom 2010;13:418–425.
- 9
- Hoff M, Dhainaut A, Kvien TK, Forslind K, Kälvesten J, Haugeberg G. Short-time in vitro and in vivo precision of direct digital X-ray radiogrammetry. J Clin Densitom 2009;12:17–21.
- 10
- Dhainaut A, Hoff M, Kälvesten J, Lydersen S, Forslind K, Haugeberg G. Long-term in-vitro precision of direct digital X-ray radiogrammetry. Skeletal Radiol 2011;40:1575–9.
- 11
- Lodder MC, Lems WF, Ader HJ ym. Reproducibility of bone mineral density measurement in daily practice. Ann Rheum Dis 2004;63:285–289.
- 12
- Kälvesten J, Lui L-Y, Brismar T, Cummings S. Digital X-ray radiogrammetry in the study of osteoporotic fractures: Comparison to dual energy X-ray absorptiometry and FRAX. Bone 2016;86:30–5.
- 13
- Siris ES, Adler R, Bilezikian J ym. The clinical diagnosis of osteoporosis: A position statement from the National Bone Health Alliance Working Group. Osteoporos Int 2014;25:1439–43.
- 14
- Wilczek ML, Kälvesten J, Algulin J, Beiki O, Brismar TB. Digital X-ray radiogrammetry of hand or wrist radiographs can predict hip fracture risk - A study in 5,420 women and 2,837 men. Eur Radiol 2013;23:1383–91.
- 15
- Crandall CJ, Larson J, Gourlay ML ym. Osteoporosis screening in postmenopausal women 50–64 years old: comparison of US Preventive Services Task Force strategy and two traditional strategies in the Women’s Health Initiative. J Bone Miner Res 2014;29:1661–6.
- 16
- Rubin KH, Friis-Holmberg T, Hermann AP, Abrahamsen B, Brixen K. Risk assessment tools to identify women with increased risk of osteoporotic fracture: Complexity or simplicity? A systematic review. J Bone Miner Res 2013;28:1701–17.
- 17
- Kanis JA, Oden A, Johnell O ym. The use of clinical risk factors enhances the performance of BMD in the prediction of hip and osteoporotic fractures in men and women. Osteoporos Int 2007;18:1033–46.
Digital X-ray radiogrammetry (DXR) in patients with fractures
Background Patient screening in Fracture Liaison Services to prevent secondary fractures should be effective, fast and easily accessible. Tools such as FRAX can be used for fracture risk assessment, but collection of the required information is often challenging in busy accident and emergency wards. Digital x-ray radiogrammetry (DXR) measures bone mineral density of metacarpal bones from a normal hand x-ray image.
Methods DXR and FRAX assessments were performed in 160 female low energy fracture patients (aged 50–74 years) treated at the accident and emergency ward of Mikkeli Central Hospital, Finland, during winter 2016–2017. Additional DXA (dual-energy X-ray absorptiometry) measurements were performed in patients whose DXR T-score was below -1 SD (n = 116).
Results DXR and FRAX results showed moderate correlation (r = 0.47; p < 0.001). At a T-value threshold of -1 SD, DXR recognized elevated FRAX-risk with a sensitivity of 91% and specificity of 52%. According to the FRAX assessment alone, further DXA measurement would have been needed for 110 patients, i.e. those with an elevated or high FRAX-risk. By targeting the DXA assessment only to those with DXR osteopenia and FRAX-risk of 10–19%, only 38 patients would have needed the DXA. In patients with DXR T < -1, DXR identified osteoporosis better than FRAX (AUC: DXR / FRAX = 0.75 / 0.63).
Conclusions We propose DXR measurements as a primary screening technique, which would allow identification of osteopenia patients for secondary FRAX screening, thereby reducing the need for the more demanding and expensive DXA measurements in fracture patients.