Kroonisten tulehduksellisten suolistosairauksien lääkehoito
• Tulehduksellisten suolistosairauksien hoito on kehittynyt merkittävästi viime vuosikymmeninä, mutta silti sairauteen ei ole parantavaa hoitoa.
• Uudet lääkevaihtoehdot ovat muuttaneet hoidon aiempaa yksilöllisemmäksi.
• Sairaanhoitopiirien laatimien hoitoketjujen mukaisesti rauhallisessa vaiheessa taudin seuranta voidaan toteuttaa perusterveydenhuollossa erikoissaanhoidosta saatujen ohjeiden mukaisesti.

Tulehduksellisten suolistosairauksien, Crohnin taudin ja haavaisen paksusuolitulehduksen eli ulseratiivisen koliitin, hoito ja hoidon tavoitteet ovat muuttuneet kunnianhimoisemmiksi 2000-luvulla, ennen kaikkea biologisten lääkkeiden tultua markkinoille. Lääkehoidon tavoitteita ovat oireettomuus, suolen limakalvon parantuminen, sairauteen liittyvien komplikaatioiden esto ja elämänlaadun parantaminen (1,2). Huolimatta kehittyneestä lääkehoidosta jopa 30 % haavaista paksusuolitulehdusta sairastavista ja merkittävä osa Crohnin tautia sairastavista joutuu leikkaushoitoon (3).
Lääkehoidon valintaan vaikuttavat suolistosairauden laajuus ja sijainti sekä erityisesti Crohnin taudissa etenemisriskiä ennustavat tekijät, kuten tupakointi, sairauden puhkeaminen alle 18 vuoden iässä, taudin laaja-alaisuus, strikturoiva tai penetroiva tautityyppi, perianaalitauti, alkuvaiheen steroiditarve ja ekstraintestinaaliset oireet (4,5).
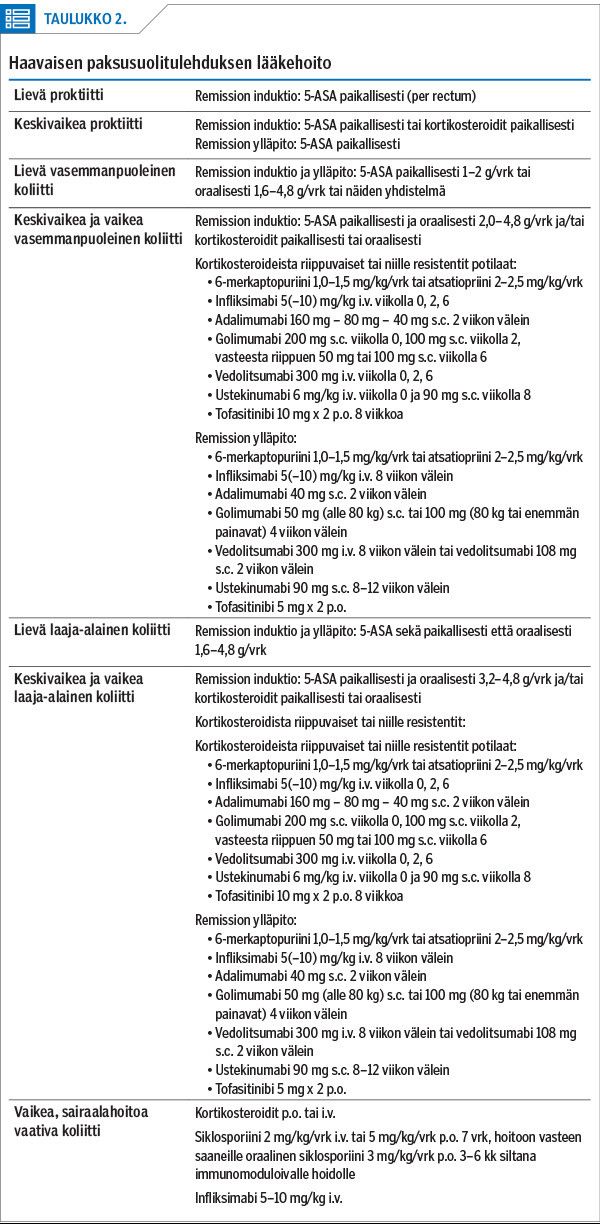
Lääkehoito jaotellaan remission (sairauden oireiden lieveneminen) induktioon ja ylläpitoon. Haavaisen paksusuolitulehduksen ja Crohnin taudin hoidon pääpiirteet on kuvattu taulukoissa (taulukko 1 ja 2).
Perusterveydenhuollossa ensisijaista on osata epäillä tulehduksellista suolistosairautta ja ohjata potilaat jatkotutkimuksiin ja hoitoon. Sairauden kroonisen luonteen ja uusiutumistaipumuksen vuoksi seuranta on tärkeää. Paikallisten hoitoketjujen mukaisesti sairauden rauhallisessa vaiheessa potilaiden seuranta voidaan toteuttaa merkittävältä osin perusterveydenhuollossa.
Glukokortikoidit remission induktiona
Kortikosteroideja käytetään remission käynnistämiseen sekä haavaisessa paksusuolitulehduksessa että Crohnin taudissa. Glukokortikoidihoito ei estä pahenemisvaiheita, eivätkä ne laajan haittavaikutusprofiilinsa vuoksi sovellu ylläpitohoitoon (Liitetaulukko 1). Tavoitteena onkin remissio ilman glukokortikoidilääkitystä (6).
Tavallisimmin remission käynnistämiseen käytetään suun kautta otettavia prednisoni- tai prednisolonivalmisteita sekä paikallisesti annosteltavia hydrokortisoni- ja budesonidivalmisteita. Oraalinen hoito aloitetaan useimmiten prednisoloniannoksella 40 mg/vrk viikon ajan, ja sen jälkeen vuorokausiannosta pienennetään 5 mg viikon välein. Hoidon pituus on tavallisesti 8 viikkoa. Kortisoniannoksen suurentamisen yli 60 mg:aan/vrk ei ole todettu parantavan hoidon tehoa, mutta sen tiedetään lisäävän hoidon haittavaikutuksia merkittävästi (7).
Oraalisen prednisolonin vaihtoehdoksi on tarjolla budesonidivalmiste, jonka haittavaikutusprofiili on suotuisampi (8). Budesonidivalmisteista enterokapselit ja depottabletit vaikuttavat ohutsuolen loppuosassa ja paksusuolen alkuosassa ja multimatriksirakenteinen valmiste (MMX) vaikuttaa pääosin vasta paksusuolessa.
Koska kortikosteroideja ei suositella pitkäaikaiseen käyttöön tai enemmän kuin kaksi kuuria vuodessa, niiden rinnalle aloitetaan yleensä jo alkuvaiheessa muu pitkäaikainen lääkitys. Peräsuolitulehduksen hoidoksi valitaan ensisijaisesti rektaalisesti annettava valmiste.
5-ASA ensilinjan hoito haavaisessa paksusuolitulehduksessa
Vanhan lääkevalmisteen sulfasalatsiinin käyttöön liittyy noin viidenneksellä potilaista haittavaikutuksia. Sen käyttö rajoittuu nykyisin lähinnä niveloireisten potilaiden hoitoon, ja 5-aminosalisylaattivalmisteet (5-ASA) ovat syrjäyttäneet sen (9).
Mesalatsiinia käytetään ensi linjan hoitona lievän ja keskivaikean haavaisen paksusuolitulehduksen remission induktiossa ja ylläpitohoidossa (5,10,11). Vasemmanpuolisessa ja laaja-alaisessa paksusuolitulehduksessa suositellaan oraalisen ja rektaalisen valmisteen samanaikaista käyttöä. Peräsuoleen rajoittuvassa taudissa hoitovaihtoehtoina ovat peräpuikot ja peräruiskeet. Ohutsuolen taudissa mesalatsiinista ei ole hyötyä, eikä eurooppalainen konsensuslausuma suosittele sen käyttöä Crohnin taudin hoidossa (4,5).
Säännöllistä turvakoeseurantaa suositellaan, erityisesti mesalatsiinihoitoon liittyvän munuaisten vajaatoiminnan riskin vuoksi. Hoidon vasta-aiheita ovat yliherkkyys sulfonamideille ja salisylaateille.
Hoidon tehostaminen ensisijaisesti immunosuppressiivisella lääkkeellä
Tiopuriineilla, atsatiopriinilla ja 6-merkaptopuriinilla (6-MP) on keskeinen asema tulehduksellisten suolistosairauksien hoidossa, vaikka niiden vaikutusmekanismia ei täysin tunneta (4,5,9,10,12).
Tiopuriinia suositellaan, jos potilaan suolistosairaus on vaatinut vähintään kaksi kortikosteroidikuuria vuodessa tai tauti aktivoituu steroidiannosta pienennettäessä. Koska tiopuriinien lääkevaikutus saavutetaan hitaasti, tavallisesti vasta 3–6 kuukauden kuluessa, ne eivät sovellu remission käynnistämiseen vaan ainoastaan sen ylläpitoon. Haavaista paksusuolitulehdusta sairastavilla potilailla mesalatsiinihoitoa jatketaan yleensä tiopuriinihoidon rinnalla.
Tiopuriinin käyttöä rajoittavat hoidon riittämätön teho (30–40 % potilaista) ja haittavaikutukset (Liitetaulukko 1), joita todetaan jopa 30 %:lla potilaista. Hoidosta saatava hyöty on kuitenkin arvioitu haittoja suuremmaksi (13,14,15).
Geneettisesti määräytyvä tiopuriinien inaktivoitumiseen osallistuvan entsyymin tiopuriinimetyylitransferaasin (TPMT) puutos altistaa tiopuriinien hematotoksisuudelle. Tavanomainen annos atsatiopriinia tai 6-merkaptopuriinia johtaa entsyymipuutoksen yhteydessä suurella todennäköisyydellä vakavaan luuydinlamaan muutamassa viikossa (16,17). Suomessa tiopuriinin käyttö aloitetaan tavallisesti annosta vähitellen suurentaen, eikä aikuispotilaiden TPMT-puutosta määritetä rutiininomaisesti.
Allopurinolin ja tiopuriinin samanaikainen käyttö suurentaa 6-merkaptopuriinin pitoisuuden moninkertaiseksi, ja sen vuoksi allopurinolin ja tiopuriinin yhteiskäytössä tulee noudattaa erityistä varovaisuutta. Tätä ominaisuutta hyödynnetään maksatoksisten haittavaikutusten estossa, mutta silloin tiopuriiniannoksen tulee olla vain murto-osa tavanomaisesta ja seuranta toteutetaan erikoissairaanhoidossa.
Tiopuriinihoito on aloitettu perinteisesti atsatiopriinilla ja vasta mahdollisten haittavaikutusten ilmaantuessa siirrytty aiemmin erityisluvalliseen 6-merkaptopuriiniin. Erityislupamenettelystä luovuttiin vuonna 2019, ja uudet hoidot aloitetaan yleensä paremmin siedetyllä 6-MP:lla. Tiopuriinia suositellaan myös TNF-alfan salpaajahoidon rinnalle estämään vasta-ainemuodostusta ja hidastamaan biologisen lääkkeen poistumista, jolloin annos voi olla tavanomaista ylläpitohoitoa merkittävästi pienempi (18).
Tiopuriinilääkitys on usein pitkäaikaista ja päätös sen purkamisesta tehdään potilaskohtaisesti. Vahvaa näyttöä oikea-aikaisesta lopettamisesta ei ole. Eurooppalaiset konsensuslausumat eivät suosittele tiopuriinihoidon lopettamista Crohnin taudin ja haavaisen paksusuolitulehduksen hoidossa, koska uusiutumisriski on merkittävä (5,10). Tuoreen englantilaisen hoitosuosituksen mukaan lopettamista voidaan harkita potilaskohtaisesti pitkäaikaisen kliinisen, endoskooppisen ja histologisen remission jälkeen potilaan toiveet huomioiden (4).
Tiopuriinilääkitys edellyttää säännöllistä verikoeseurantaa (taulukko 3). Se voidaan toteuttaa pitkäaikaisessa remissiossa oleville potilaille myös perusterveydenhuollossa.
Crohnin taudin hoidossa tiopuriini voidaan korvata foolihappoantagonisti metotreksaatilla, jonka käyttöaiheet ovat samat kuin tiopuriinien (7,10,19). Metotreksaatilla on sekä anti-inflammatorisia että antimetaboliittisia ominaisuuksia. Haavaisessa paksusuolitulehduksessa sen teho on heikko, eikä sitä voida suositella hoitovaihtoehdoksi steroidiresistentissä taudissa. Metotreksaattia voidaan kuitenkin käyttää tiopuriinin sijaan TNF-alfan salpaajahoidon rinnalla estämään vasta-ainemuodostusta ja hidastamaan biologisen lääkkeen poistumista (18). Potilaista 10–18 % joutuu keskeyttämään lääkityksen haittavaikutusten takia (Liitetaulukko 1) (20). Metotreksaattihoitoon liittyvän pahoinvoinnin estämiseksi lääkitykseen liitetään suun kautta otettava foolihappo (tavallisesti 5 mg kerta-annoksena). Myös metotreksaattilääkitys edellyttää säännöllisiä turvakokeita.
Kalsineuriinin estäjistä siklosporiinia on käytetty steroidiin reagoimattoman vaikean haavaisen paksusuolitulehduksen remission käynnistämiseen. Lääkkeen pitkäaikaista käyttöä tulee välttää haittavaikutusten, kuten munuaisten toimintahäiriöiden, takia. Crohnin taudissa siklosporiinin teho on vähäinen eikä sen käyttöä suositella (5,12).
Biologiset lääkkeet muuttivat hoidon tavoitteet
Kroonisten tulehduksellisten suolistosairauksien hoidossa ensisijainen biologinen lääke on tuumorinekroositekijä alfan (TNF-alfa) salpaaja. Suomessa niitä on käytettävissä kolme: suoneen annettava infliksimabi sekä itse pistettävät adalimumabi ja golimumabi.
Infiksimabin ja adalimumabin käyttöaiheita ovat perinteiseen hoitoon reagoimaton keskivaikea tai vaikea Crohnin tauti ja haavainen paksusuolitulehdus sekä fistuloiva Crohnin tauti (4,5,9,10,11,12). Infliksimabin etuna on sen muita biologisia lääkkeitä nopeampi teho, ja siksi sitä käytetään ensisijaisena lääkkeenä erityisesti vaikean, sairaalahoitoa vaativan haavaisen paksusuolitulehduksen hoitoon (21). Golimumabin käyttöaiheena on ainoastaan keskivaikeasti tai vaikeasti aktiivinen haavainen paksusuolitulehdus.
TNF-alfan salpaajahoitoon liittyy merkittäviä vasta-aiheita ja haittavaikutuksia. Päätös biologisten lääkehoitojen aloittamisesta kuuluukin niihin perehtyneelle erikoislääkärille paikassa, jossa potilaan ohjaaminen ja tarkka seuranta on mahdollista. Lisäksi pitkäaikaisen hoidon varsin yleisenä ongelmana on lääkevasta-aineiden muodostuminen ja tehon menetys, jonka vuoksi jopa 40 % potilasta tarvitsee joko tiheämmän annosvälin tai suuremman annoksen. Lääkehoidon optimointi pitoisuus- ja lääkevasta-ainemääritysten perusteella on suositeltavaa.
Erityisesti nuorilla potilailla atsatiopriinin ja infliksimabin yhdistelmään on liittynyt riski sairastua hyvin harvinaiseen, mutta huonoennusteiseen hepatospleeniseen T-solulymfoomaan (22). Tämä huomioon ottaen yhdistelmähoidon hyötyjä ja haittoja tulee arvioida potilaskohtaisesti.
Infliksimabin ja adalimumabin biosimilaarien tultua markkinoille biologisen lääkehoidon kustannukset ovat laskeneet merkittävästi. Tällä on iso merkitys, koska tulehduksellisissa suolistosairauksissa lääkehoitoa joudutaan usein jatkamaan vuosia.
Biologisen lääkehoidon lopettamista voidaan harkita silloin, kun sillä on saavutettu pitkäaikainen kliininen ja endoskooppisesti todettava remissio ja potilaalle on käytössä muu tehokas lääkehoito. Lopettamisen jälkeen tauti näyttää kuitenkin suurimmalla osalla potilaista lopulta taas aktivoituvan ja lääkehoito on aloitettava uudelleen (23).
TNF-alfan salpaajat eivät tehoa kaikilla potilailla, joten muilla mekanismeilla vaikuttaville biologisille lääkkeille on tarvetta. Vuonna 2014 kliiniseen käyttöön tullut suolistoselektiivinen alfa-4-beeta-7-integriinin estäjä vedolitsumabi on monoklonaalinen vasta-aine, joka estää aktivoituneiden valkosolujen kiinnittymisen suolen verisuonten endoteelin adheesiomolekyyliin (MAdCAM-1). Sen käyttöaiheita ovat sekä keskivaikea ja vaikea haavainen paksusuolitulehdus että Crohnin tauti silloin, kun vaste tavanomaiseen hoitoon tai TNF-alfan salpaajiin on ollut riittämätön tai se on hävinnyt tai kun potilas ei ole sietänyt näitä hoitoja (24,25).
Vedolitsumabi on aiemmin annettu suoneen, mutta itse pistettävä valmiste on saanut myyntiluvan ja lähitulevaisuudessa osa hoidoista voidaan toteuttaa sillä. Lääke on hyvin siedetty. Suotuisan haittavaikutusprofiilin vuoksi sitä voidaan harkita ensilinjan biologiseksi lääkehoidoksi erityisesti iäkkäille potilaille. Myös vedolitsumabihoitoa voidaan optimoida pitoisuus- ja lääkevasta-ainemäärityksin.
Interleukiini 12:n ja interleukiini 23:n yhteisen alayksikön p40:n salpaaja ustekinumabi on ollut muutaman vuoden ajan käytössä keskivaikean tai vaikean Crohnin taudin hoidossa, ja se on saanut myyntiluvan haavaisen paksusuolitulehduksen hoitoon viime vuonna (26,27). Sitä käytetään nykyisin ensisijaisesti toisen linjan biologisena lääkehoitovaihtoehtona TNF-alfan salpaajiin reagoimattomien, niihin vasteen menettäneiden tai niillä toteutettavaan hoitoon soveltumattomien keskivaikeaa tai vaikeaa Crohnin tautia tai haavaista paksusuolitulehdusta sairastavien potilaiden hoitoon. Sitä voidaan pitää hyvänä hoitovaihtoehtona TNF-alfan salpaajahoitoon liittyvän psoriaasin kaltaisen ihottuman saaneille potilaille. Ustekinumabin etuina ovat haittavaikutusten vähäisyys (Liitetaulukko 1) ja vähäinen lääkevasta-aineiden muodostumistaipumus.
Uusista pienimolekyylisistä lääkkeistä toistaiseksi vain tablettimuotoiselle januskinaasin (JAK) estäjällä tofasitinibille on hyväksytty käyttöaiheeksi haavaisen paksusuolitulehduksen hoito (28). Lääkevaste on todettu tutkimusten perusteella nopeaksi (29). Induktiohoidon lääkeannokseen (10 mg x 2) on liittynyt lisääntynyt veritulpan riski, ja tämä tulee huomioida potilasvalinnassa ja hoidon seurannassa (30). Riskiä lisäävät erityisesti perinnöllinen veren hyytymishäiriö, aiemmin sairastettu veritulppa, yhdistelmäehkäisyvalmisteiden ja hormonikorvaushoidon käyttö sekä syöpäsairaudet. Lisääntyneen infektioriskin vuoksi yli 65-vuotiaille tofasitinibia tulee harkita vain, jos muita sopivia vaihtoehtoja ei ole. Hoidon seuranta kuuluu erikoissairaanhoitoon.
Useita lupaavia biologisia ja immunomoduloivia lääkehoitoja on odotettavissa markkinoille lähivuosina. Vaihtoehtojen lisääntyessä lääkehoitojen yksilöllisellä valinnalla on entistä suurempi merkitys. Sen vuoksi kliiniseen käyttöön kaivataan luotettavia merkkiaineita, joiden avulla jokaiselle potilaalle voitaisiin löytää paras mahdollinen lääkehoitovaihtoehto.
Mikrobilääkkeet osana ylläpitohoitoa ja septisten komplikaatioiden hoidossa
Metronidatsolia ja siprofloksasiinia käytetään oireisen fistuloivan perianaalisen Crohnin taudin hoidossa, kuten myös aktiivisen J-pussitulehduksen hoidossa (4,5). Lisäksi metronidatsolista näyttää olevan hyötyä postoperatiivisen Crohnin taudin uusiutumisen estossa (31). Kuuriluonteinen mikrobilääkehoito on aiheellinen septisten komplikaatioiden hoidossa (4,5,12).
Kummankin lääkkeen pitkäaikaiskäyttöä rajoittavat niiden haittavaikutukset. Erityisesti perifeerisen neuropatian riski suuria metronidatsoliannoksia (yli 10 mg/kg/vrk) käytettäessä on huomioitava. Siprofloksasiinille tyypillisiä ovat maha-suolikanavan haitat, kuten ripuli, pahoinvointi ja ruokahaluttomuus, mutta lisäksi siihen on liittynyt sidekudostoksisuutta, joka ilmenee tavanomaisimmin jännevaurioina. Useimmiten haitta kohdistuu akillesjänteeseen.
Onko probiooteista hyötyä?
Probiooteista on odotettu apua sekä haavaisen paksusuolitulehduksen että Crohnin taudin hoitoon. Tutkimusnäyttö on vakuuttavinta lähinnä J-pussitulehduksen hoidosta.
Probioottista Escherichia coli (E. coli) Nissle 1917 -valmistetta voidaan käytetään aikuisten haavaisen paksusuolitulehduksen pahenemisvaiheiden estohoitoon (9,10). Sen käyttö Suomessa on kuitenkin jäänyt verraten vähäiseksi. Crohnin taudissa probiootteja ei suositella.
Tukihoidosta tulee huolehtia
Tulehduksellista suolistosairautta sairastavilla potilailla todetaan usein kalsiumin ja D-vitamiinin puutetta, joten niiden riittävästä saannista tulee huolehtia. B12-vitamiinin puutteen ei ole todettu olevan tavallisempaa kuin muussa väestössä, mutta ohutsuolen loppuosan poistoleikkaus altistaa sille (32).
Toiminnalliset suolioireet ovat yleisiä tulehduksellista suolistosairautta sairastavilla potilailla. Remissiovaiheessa ripulioireita tulisi pyrkiä vähentämään lääkkeillä, kuten antikolinergeilla, lääkekuidulla tai kolestyramiinilla (33).
Myös anemia on tavanomaista. Yleisimmin se on raudanpuuteanemiaa, mutta myös kroonisen taudin anemiaa esiintyy, samoin kuin näiden kahden yhdistelmää (34). Aktiivinen suolitulehdus on tärkein raudanpuuteanemian syy, mutta raudanpuuteanemiaa esiintyy myös inaktiivisen taudin yhteydessä (35).
Raudanpuute tulee korjata ensisijaisesti suun kautta otettavalla rautavalmisteella, mutta parenteraalista rautahoitoa tulee harkita, jos potilas ei siedä peroraalista rautaa tai ei saa vastetta siihen. Parenteraalista rautavalmistetta suositaan myös silloin, kun potilaan kokonaistilanne edellyttää pikaista raudanpuutteen korjaamista erityisesti suolitulehduksen ollessa vaikeasti aktiivinen. Liian suuria rauta-annoksia tulee välttää; yleensä riittävä annos on 100 mg/vrk (36).
Tulehduksellista suolistosairautta sairastavilla anemia uusii herkästi asianmukaisen hoidon ja rautavarastojen täydennyksen jälkeen, joten seurantaa suositellaan myös anemian korjauksen jälkeen.
Lopuksi
Kroonisten tulehduksellisten suolistosairauksien hoito on pitkäaikaista, ja se on muuttunut viime vuosina aiempaa yksilöllisemmäksi uusien lääkevaihtoehtojen ansiosta. Valtaosa potilaista voidaan edelleen hoitaa tavanomaisella lääkityksellä ja seuranta toteuttaa osin perusterveydenhuollossa paikallisten hoitopolkujen mukaisesti.
KORJAUS
Golimumabin annostus taulukossa 2 on korjattu 17.9.2021.
Pauliina Molander: Konsultointipalkkiot (AbbVie, Celltrion, Pfizer, Roche), asiantuntijalausunto (Janssen-Cilag, Takeda), luentopalkkiot (AbbVie, MSD, Mylan, Orion, Tillots Pharma), matka-, majoitus- ja kokouskulut (Ferring, Pfizer, Tillots Pharma).
- 1
- Bouguen G, Levesque BG, Feagan BG ym. Treat to target: a proposed new paradigm for the management of Crohn’s disease. Clin Gastroenterol Hepatol 2015;13:1042–50.
- 2
- Sandborn WJ, Hanauer S, Van Assche G, ym. Treating beyond symptoms with a view to improving patient outcomes in inflammatory bowel diseases. J Crohns Colitis 2014;8:927–35.
- 3
- Sokol H, Seksik P, Cosnes J. Complications and surgery in the inflammatory bowel diseases biological era. Curr Opin Gastroenterol 2014;30:378–84.
- 4
- Lamb CA, Kennedy NA, Raine T ym. British Society of Gastroenterology consensus guidelines on the management of inflammatory bowel disease in adults. Gut 2019;68(3):1–106.
- 5
- Torres J, Bonovas S, Doherty G ym. ECCO Guidelines on Therapeutics in Crohn’s Disease: Medical Treatment. J Crohns Colitis 2020;14:4–22.
- 6
- Targownik LE, Nugent Z, Singh H ym. Prevalence of and outcomes associated with corticosteroid prescription in inflammatory bowel disease. Inflamm Bowel Dis 2014;20:622–30.
- 7
- Egam LJ, Derijks LJ, Hommes DW. Pharmacogenomics in inflammatory bowel disease. Clin Gastroenterol Hepatol 2006;4:21–8.
- 8
- Sandborn WJ, Travis S, Moro L ym. Once-daily budesonide MMX® extended-release tablets induce remission in patients with mild to moderate ulcerative colitis: results from the CORE I study. Gastroenterology 2012;143:1218–26.
- 9
- Rubin DT, Ananthakrishnan AN, Siegel CA ym. ACG Clinical Guideline: Ulcerative colitis in Adults. Am J Gastroenterol 2019;114:384–413.
- 10
- Hardbord M, Eliakim R, Bettenworth D ym. Third European Evidence-based Consensus on Diagnosis and Management of Ulcerative Colitis. Part 2: Current Management. J Crohns Colitis 2017;11:769–84.
- 11
- Ko CW, Singh S, Feuerstein JD ym. AGA Clinical Practice Guidelines on the Management of Mild-to-Moderate Ulcerative Colitis. Gastroenterology 2019;156:748–64.
- 12
- Lichenstein GR, Loftus EV, Isaacs KL ym. ACG Clinical Guideline: Management of Crohn’s Disease in Adults. Am J Gastroenterol 2018;113:481–517.
- 13
- Moon W, Loftus EV Jr. Review article: recent advances in pharmacogenetics and pharmacokinetics for safe and effective thiopurine therapy in inflammatory bowel disease. Aliment Pharmacol Ther 2016;43:863–83.
- 14
- Kennedy NA, Rhatigan E, Arnott DR ym. A trial of mercaptopurine is a safe strategy in patients with inflammatory bowel disease intolerant to azathioprine: an observational study, systematic review and meta-analysis. Aliment Pharmacol Ther 2013;38:1255–66.
- 15
- Sparrow MP, Hande SA, Friedman S ym. Effect of allopurinol on clinical outcomes in inflammatory bowel disease nonresponders to azathioprine or 6-mercaptopurine. Clin Gastroenterol Hepatol 2007;5:209–14.
- 16
- Teml A, Schaeffeler E, Herrlinger KR ym. Thiopurine treatment in inflammatory bowel disease: clinical pharmacology and implication of pharmacogenetically guided dosing. Clin Pharmacokinet 2007;46:187–208.
- 17
- Gisbert JP, Niño P, Rodrigo L ym. Thiopurine methyltransferase (TPMT) activity and adverse effects of azathioprine in inflammatory bowel disease: long-term follow-up study of 394 patients. Am J Gastroenterol 2006;101:2769–76.
- 18
- Vermeire S, Gils A, Accossato P ym. New biologics and small molecules in inflammatory bowel disease: an update. Therap Adv Gastroenterol 2018 Jan 21;11:1756283X17750355. eCollection 2018.
- 19
- Panaccione R, Steinhart AH, Bressler B ym. Canadian Association of Gastroenterology Clinical Practice Guideline for the Management of Luminal Crohn’s Disease. Clin Gastroenterol Hepatol 2019;17:1680–713.
- 20
- Loftus EV, Davis KL, Wang C-C ym. Treatment patterns, complications, and disease relapse in a real-world population of patients with moderate-to-severe ulcerative colitis initiating immunomodulator therapy. Inflamm Bowel Dis 2014;20:1361–7.
- 21
- Järnerot G, Hertervig E, Friis-Liby I ym. Infliximab as rescue therapy in severe to moderately severe ulcerative colitis: a randomized, placebo-controlled study. Gastroenterology 2005;128:1805–11.
- 22
- Thai A, Prindiville T. Hepatosplenic T-cell lymphoma and inflammatory bowel disease. J Crohns Colitis 2010;4:511–22.
- 23
- Doherty G, Katsanos KH, Burisch J ym. European Crohn’s and Colitis Organisation topical review on treatment withdrawal [’exit strategies’] in inflammatory bowel disease. J Crohns Colitis 2018;12:17–31.
- 24
- Loftus EV Jr, Colombel JF, Feagan BG ym. Long-term efficacy of vedolizumab for ulcerative colitis. J Crohns Colitis 2017;11:400–11.
- 25
- Vermeire S, Loftus EV Jr, Colombel JF ym. Long-term efficacy of vedolizumab for Crohn’s Disease. J Crohns Colitis 2017;11:412–24.
- 26
- Feagan BG, Sandborn WJ, Gasink D ym. Ustekinumab as induction and maintenance therapy for Crohn’s disease. N Engl J Med 2016;375:1946–60.
- 27
- Sands B, Sandborn WJ, Panaccione R ym. Ustekinumab as induction and maintenance therapy for ulcerative colitis. N Engl J Med 2019;381:1201–14.
- 28
- Sandborn WJ, Su C, Sands BE ym. Tofacitinib as induction and maintenance therapy for ulcerative colitis. N Engl J Med 2017;376:1723–36.
- 29
- Honap S, Chee D, Chapman TP ym. Real-world effectiveness of tofacitinib for moderate to severe ulcerative colitis: A multicentre UK experience. J Crohn Colitis 2020;14:1385–93.
- 30
- European Medicines Agency. Xeljanz (siteerattu 7.4.2021). https://www.ema.europa.eu/en/medicines/human/referrals/xeljanz
- 31
- Di Sario A, Sassaroli P, Daretti L ym. Postoperative recurrence of Crohn’s disease: pathophysiology, diagnosis and treatment. Curr Pharm Biotechnol 2017;18:979–88.
- 32
- Battat R, Kopylov U, Szilagyi A ym. Vitamin B12 deficiency in inflammatory bowel disease: prevalence, riski factors, evaluation, and management. Inflamm Bowel Dis 2014;4:1120–8.
- 33
- Shah SB, Hanauer SB. Treatment of diarrhea in patients with inflammatory bowel disease, concepts and cautions. Rev Gastroenterol Disord 2007;7:3–10.
- 34
- Dignass AU, Gasche C, Bettenworth D ym. European Consensus on the Diagnosis and Management of Iron Deficiency and Anaemia in Inflammatory Bowel Diseases. J Crohn’s Colitis 2015;9:211–22.
- 35
- Bager P, Befrits R, Wikman O ym. The prevalence of anemia and iron deficiency in IBD outpatients in Scandinavia. Scand J Gastroenterol 2011;46:304–9.
- 36
- Gomollón F, Gisbert JP. Current management of iron deficiency anemia in inflammatory bowel diseases: a practical guide. Drugs 2013;73:1761–70.
Medical therapy of chronic inflammatory bowel diseases
Inflammatory bowel disease (IBD) is a chronic inflammatory disease of the gastrointestinal tract which includes Crohn’s disease (CD) and ulcerative colitis (UC). Medical therapy for IBD has advanced dramatically in the last decade with the introduction of targeted biologic therapies and the optimization of older therapies, such as immunomodulators.
The first line drugs for treatment of IBD are corticosteroids and aminosalicylates, such as mesalamine. Steroids are the treatment of choice for moderate to severe flare-ups, but are inappropriate for long-term use because of their side effects and inability to maintain remission. Immunosuppressants, such as azathioprine, that require several weeks to achieve their therapeutic effect have a limited role in the acute setting, but are preferred for long-term management. Antibiotics may be used in addition to other medications, most often in cases of perianal Crohn’s disease, or when infection is a concern. Biologics are a newer category of therapy in which therapy is directed toward neutralizing proteins in the body that are causing inflammation. These drugs include infliximab, adalimumab, golimumab, vedolizumab and ustekinumab. In the last decade, oral agents inhibiting cell signalling have been explored successfully in IBD. Tofacitinib, a non-selective oral Janus kinase (JAK) inhibitor, is effective in patients with UC. Moreover, new treatment options have been actively explored in clinical trials.
Antidiarrhoeal agents, vitamin supplements and treatment of anaemia play supportive roles in reducing symptoms and improving quality of life. These drugs should be individualized based on a patient’s symptoms and given in addition to anti-inflammatory medications.
This review focuses on the current treatments for inflammatory bowel disease.