Muista immunosuppressioon liittyvä infektioiden riski
• Immuunijärjestelmän toimintaa hillitseviin lääkkeisiin liittyy infektioriskejä, joiden merkittävyys vaihtelee. Riski tulee arvioida ennen hoidon aloitusta.
• Osa infektioista on estettävissä rokotuksin tai ehkäisevällä mikrobilääkityksellä.
• Myös päivystävän lääkärin on osattava tunnistaa immunosuppressioon liitetyt riskit.
Immuunijärjestelmän toimintaa hillitseviä lääkkeitä käytetään autoimmuunitautien hoitona ja elinsiirroissa. Useissa sairauksissa yhteen biologiseen kohteeseen vaikuttavat lääkeaineet ovat osin syrjäyttäneet perinteisten, immunologisilta vaikutuksiltaan laajakirjoisten lääkkeiden käytön.
Infektiot ovat immunosuppressiivista hoitoa saavien potilaiden tavallisimpia kuolinsyitä. Niiden ehkäiseminen ja tunnistaminen ovat tärkeä osa potilaiden hoitoa. Myös päivystystilanteissa on osattava tunnistaa näihin lääkkeisiin liitettyjä infektiohaittoja.
Tässä artikkelissa käydään läpi tavallisimpiin immunosuppressiohoitoihin liittyviä infektioriskejä ja niiden ehkäisykeinoja, pois lukien muun muassa syövän hoitoon liittyvät riskit.
Immuunijärjestelmän eri toimintojen rooli
Immuunijärjestelmä voidaan jakaa luontaiseen ja hankittuun immuniteettiin (1). Luontainen immuunivaste toimii nopeana ensilinjan puolustajana haitallisia mikrobeja vastaan. Sen tärkeimpiä komponentteja ovat luonnolliset tappajasolut, syöjäsolut ja komplementtijärjestelmä. Hankitun immuniteetin toimijoista auttaja-T-solut vastaavat immuunivasteen laadusta ja voimakkuudesta, tappaja-T-solut solunsisäisten mikrobien tuhoamisesta ja B-solut vasta-aineiden tuotannosta.
Hankittu immuunivaste kehittyy erilaisten mikrobiantigeenien kohtaamisen seurauksena, mutta synnyttyään se on spesifinen ja immunologisen muistin kautta pitkäkestoinen.
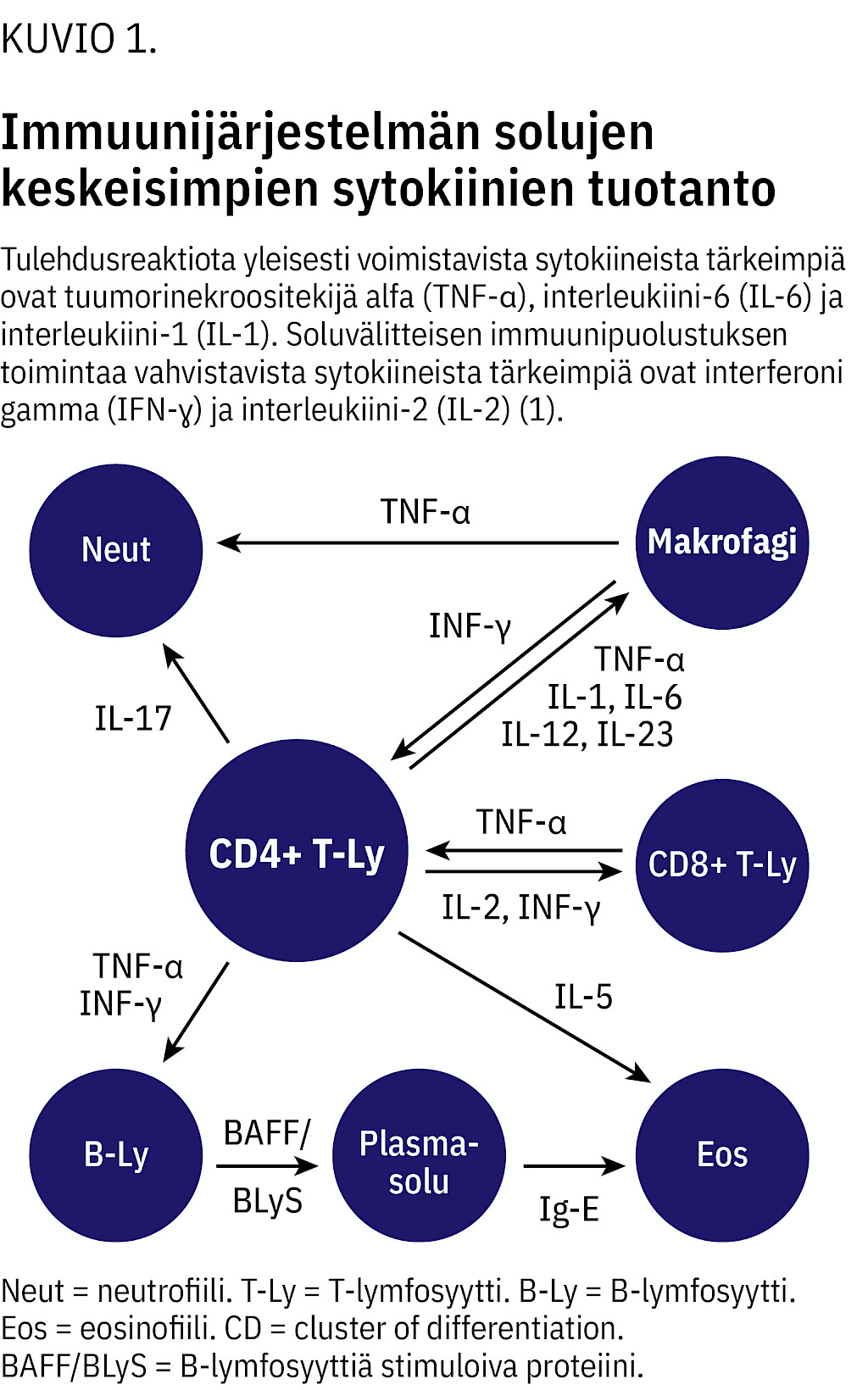
Mikrobin tunkeutuminen kudoksiin saa aikaan myös immuunivastetta säätelevien sytokiinien tuotannon (kuvio 1).
Immuunijärjestelmän komponentit toimivat yhteistyössä, mutta mikrobista riippuen torjunnassa tarvitaan immuunipuolustuksen eri osa-alueita.
Uusi infektio vai latentin infektion reaktivaatio?
Immuunivaje altistaa sekä uusille infektioille että elimistössä latentteina olevien mikrobien uudelleen aktivoitumiselle (reaktivaatiolle) (2).
Herpesryhmän viruksille on tyypillistä niiden jääminen primaari-infektion jälkeen elimistöön. Normaali immuunipuolustus pitää virukset yleensä latentteina, mutta immuunivajeessa ne voivat päästä jakautumaan uudelleen ja aiheuttaa oireisen infektion.
Muita immuunivajeessa mahdollisesti reaktivoituvia infektioita ovat B-hepatiittiviruksen (HBV) aiheuttama infektio, toksoplasmoosi, polyoomavirusinfektiot ja tuberkuloosi.
Immuunivajeinen henkilö voi saada kliinisen infektion myös sellaisen mikrobin aiheuttamana, joka on immunokompetentille yleensä harmiton. Tällaisia opportunisti-infektioita ovat mm. Pneumocystis jirovecii -pneumonia (PJP), kryptokokkoosi, ympäristömykobakteeri-infektiot, nokardioosi ja rihmasieni-infektiot.
Immunosuppressiohoitoon liittyvät infektioriskit lääkeryhmittäin
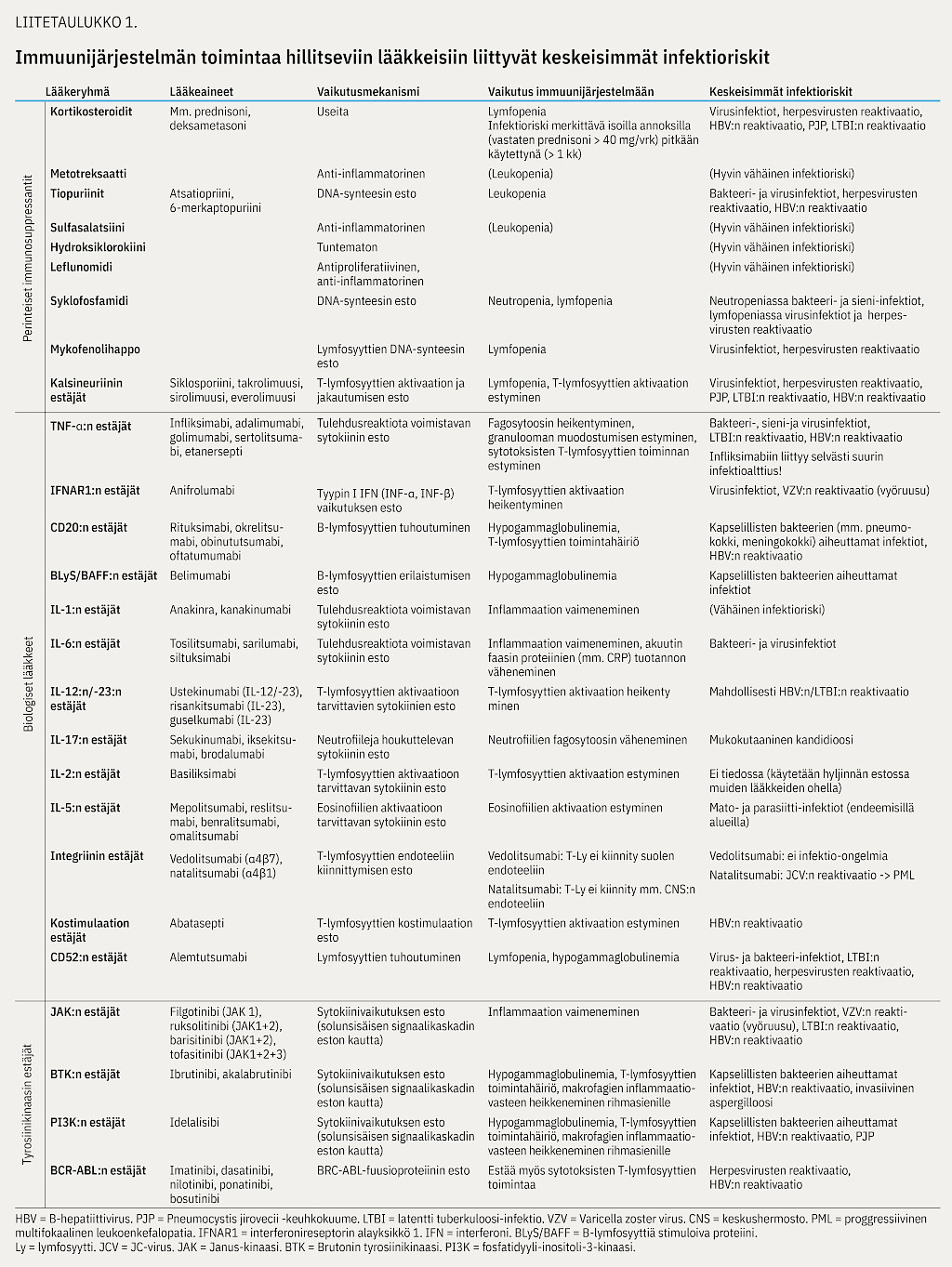
Eri lääkeryhmiin liittyy vaikutusmekanismin mukaisesti erilainen infektioriski, joka vaihtelee olemattomasta hyvin merkittävään (liitetaulukko 1).
Kortikosteroidit
Kortikosteroideja käytetään monenlaisten sairauksien ja tilojen hoidossa, usein yhdistettyinä muihin immunosuppressiivisiin lääkkeisiin. Suun kautta otettavia kortikosteroideja käyttävillä on todettu 2–6-kertainen infektioriski verrokkiväestöön nähden (3).
Kortikosteroidit vaikuttavat immuunijärjestelmään hyvin laajasti. Immunosuppressiivinen vaikutus ja infektioriski riippuvat annoksesta ja hoidon kestosta (4).
Pitkäaikaista steroidihoitoa ei tauoteta vaikeankaan infektion aikana. Lisämunuaiskuoren lamasta kärsivillä potilailla steroidiannosta suurennetaan stressitilanteissa.
Muut perinteiset immunosuppressantit
Kortikosteroideja lukuun ottamatta yleisimmin käytettyihin perinteisiin reumalääkkeisiin (metotreksaatti, sulfasalatsiini, leflunomidi, hydroksiklorokiini) ei ole liitetty kohonnutta infektioriskiä (5,6,7). Pienelle osalle sulfasalatsiinin käyttäjistä voi kehittyä hoidon seurauksena leukopenia, joka on usein lievä eikä altista infektioille, mutta myös henkeä uhkaavaa agranulosytoosia on kuvattu.
Edellä mainittuja lääkeitä ei tarvitse tauottaa lievissä infektioissa, mutta sairaalahoitoa vaativissa tai kuumeisissa infektioissa metotreksaatti ja sulfasalatsiini tauotetaan, kunnes potilaan infektiotilanne on helpottanut. Koska lääketauko voi johtaa reuman vaikeutumiseen, yli kahden viikon mittaiselle lääketauolle tulisi olla erityinen syy.
Leflunomidin tauotuksesta ei ole infektion paranemisen kannalta hyötyä, sillä sen metaboliitti on aktiivinen vielä kuukausien ajan lääkkeen lopetuksen jälkeen. Hydroksiklorokiinin tauotus voi tulla kyseeseen lähinnä lääkeaineiden yhteisvaiktusten takia.
Tiopuriinit ja syklofosfamidi altistavat infektioille etenkin yhteiskäytössä kortikosteroidien tai muiden immunosuppressiivisten lääkkeiden kanssa (8). Bakteeri-infektioiden riski liittyy neutropenian esiintymiseen. Vähäinen lymfosyyttien määrä puolestaan lisää riskiä solunsisäisille infektioille, kuten herpesvirusten reaktivaatiolle. Lääkkeiden tauotusta suositellaan kuumeisen infektion yhteydessä (9).
Kalsineuriinin estäjät ovat olleet elinsiirtopotilaiden hyljinnänestolääkityksen pääkomponentteja jo vuosikymmenten ajan. Niitä käytetään ajoittain myös autoimmuunisairauksien hoidossa. Erityisen infektio-ongelman mykofenolaattiin ja kalsineuriinin estäjiin liittyen muodostavat herpesvirusten reaktivaatiot (10).
Elinsiirtopotilaiden hyljinnänestolääkkeitä ei tule tauottaa infektion yhteydessä, mutta lääkkeen pitoisuusmääritys voi olla tarpeen. Lääkkeiden käytöstä infektion aikana tulee herkästi konsultoida kyseisen erikoisalan erikoislääkäriä.
Biologiset lääkkeet
Biologisten lääkkeiden toiminta perustuu yleensä sytokiinin tai solun pintareseptorin toiminnan estoon. Infektioriski vaihtelee lääkeaineittain erittäin pienestä hyvin merkittävään (11,12). Tässä esitettyjen yleisesti käytettyjen ja infektioriskin kannalta merkittävien lääkkeiden tauotus on yleensä infektion aikana tarpeen.
TNF-α:n estäjät. TNF-α saa aikaan proinflammatoristen sytokiinien (mm. interleukiini-6, IL-6) tuotannon ja tämän seurauksena neutrofiilien ja makrofagien aktivaation. TNF-α tarvitaan myös sytotoksisten T-lymfosyyttien aktivaatioon. TNF-α:n esto altistaa bakteeri- ja sieni-infektioille fagosytoosin heikentyessä. Latentti tuberkuloosi (LTBI) voi aktivoitua granuloomamuodostuksen estyessä, ja sytotoksisten T-lymfosyyttien toiminnanvajeessa voi muun muassa HBV aktivoitua vaikeaksi maksatulehdukseksi.
CD20:n estäjät. B-lymfosyytit erilaistuvat vasta-aineita tuottaviksi plasmasoluiksi. Tämän humoraalisen immuniteetin toiminta on erityisen tärkeää kapselillisten bakteerien aiheuttamien infektioiden torjunnassa, sillä fagosytoivat solut eivät tunnista niitä ilman vasta-ainein tapahtuvaa opsonisointia. CD20:n esto altistaakin etenkin kapselillisten bakteerien aiheuttamille infektioille.
Myös HBV:n latenttina pitämiseen tarvitaan soluvälitteisen immuniteetin ohella viruksen pintaproteiinia vastaan tuotettuja vasta-aineita. On huomioitava, ettei CD20-vasta-ainehoidon jälkeen synny humoraalista rokotusvastetta.
Antigeenejä esittelevillä B-lymfosyyteillä on myös tärkeä rooli T-lymfosyyttien aktivaatiossa.
IL-6:n estäjät. IL-6 saa aikaan proinflammatoristen sytokiinien ja akuutin faasin proteiinien (mm. C-reaktiivinen proteiini, CRP) tuotannon. IL-6:n esto altistaa bakteeri- ja virusinfektioille, muttei merkittävästi opportunisti-infektioille tai latenttien infektioiden reaktivaatiolle. On huomioitava, ettei IL-6:n estäjää saanut henkilö pysty tuottamaan CRP:tä vaikeassakaan infektiossa.
JAK:n estäjät. Janus-kinaasit (JAK) ovat entsyymejä, jotka kohdeproteiininsa fosforyloimalla saavat aikaan solunsisäisen signaalikaskadin. Esimerkiksi kun IL-6 sitoutuu T-lymfosyytin reseptoriin, käynnistyy signaalikaskadi, jonka lopputuloksena on proinflammatoristen sytokiinien ja akuutin faasin proteiinien tuotanto. Eri sytokiinireseptoreilla on erilaiset JAK-entsyymit, joita eri JAK:n estäjät vaihtelevasti estävät. Kaikki JAK:n estäjät altistavat bakteeri- ja virusinfektioille, LTBI:n ja HBV:n reaktivaatiolle ja vyöruusulle (11).
Immuunivajeisen potilaan infektioiden ehkäisy
Potilaan infektioriski tulee arvioida ennen immunosuppressiohoidon aloitusta (taulukko 2). Infektioita voidaan torjua rokotuksin ja tietyissä tilanteissa ehkäisevällä mikrobilääkityksellä.
Rokotteet
Immuunivajeiselle ja hänen lähipiirilleen suositellaan perusrokotteiden lisäksi vuosittaista kausi-influenssarokotetta (13). Koronarokotteet suositellaan ottamaan kansallisten suositusten mukaisesti (13).
Ennen immunosuppressiohoidon aloitusta varmistetaan, että potilaalla on joko sairastetun taudin tai rokotteiden antama suoja tuhkarokkoa vastaan. Vuonna 1965 – 1970-luvun alkupuolella syntyneiden rokottamattomien tuhkarokkoimmuniteetti voidaan tarvittaessa tarkistaa tutkimalla vasta-aineet.
Vesirokkorokotteet kannattaa antaa ennen immunosuppressiivisen lääkehoidon aloitusta, jos henkilö ei ole sairastanut vesirokkoa eikä ole saanut rokotesarjaa (kansallisessa rokotusohjelmassa vuoden 2005 jälkeen syntyneille). Jos henkilö ei ole varma taudin sairastamisesta, Varicella zoster virus (VZV) -immuniteetti voidaan selvittää tutkimalla vasta-aineet.
Pneumokokkikonjugaattirokotetta (PVC13 tai PVC20) suositellaan kaikille pysyvää immunosuppressiivista lääkehoitoa saaville. Pneumokokkirokote on joillekin ryhmille kansallisen rokotusohjelman mukaisesti maksuton (13).
Vyöruusun ehkäisyyn on hiljattain tullut markkinoille tehokas rekombinanttirokote, joka on turvallinen myös immuunipuutteiselle. Vyöruusurokote ei kuulu kansalliseen rokotusohjelmaan, vaan rokotteen maksaa hoitava taho tai rokotettava itse.
Meningokokkikonjugaattirokote tarjotaan kansallisen rokotusohjelman osana, jos potilaalle suunnitellaan komplementin aktivaatiota estävää lääkitystä (13).
Riittävän rokotusvasteen aikaansaamiseksi rokotteet tulisi antaa vähintään kaksi viikkoa ennen immunosuppressiivisen lääkehoidon aloitusta. Jos immunosuppressiivinen lääkitys on jo aloitettu, rokotus kannattaa ajoittaa mahdolliselle hoitotauolle siten, että lääkkeen edellisestä annoksesta on mahdollisimman pitkä aika, kuitenkin vähintään kaksi viikkoa ennen seuraavaa annosta.
Voimakkaasti immuunipuutteiselle ei saa antaa eläviä heikennettyjä taudinaiheuttajia sisältäviä rokotteita, koska heillä rokotevirus voi aiheuttaa taudin (esimerkiksi MPR- tai vesirokkorokote). Rokottamisen aiheet ja vasta-aiheet on arvioitava potilaskohtaisesti Terveyden ja hyvinvoinnin laitoksen (THL) rokotekohtaisten ohjeiden perusteella (13).
Ehkäisevä lääkehoito
Merkittävää T-lymfosyyttien vähyyttä aiheuttavien hoitojen yhteydessä tulee huolehtia PJP:n ehkäisystä (14,15). Estohoitona käytetään ensisijaisesti pieniannoksista sulfa-trimetopriimia, joka on tehokas ja suojaa myös toksoplasman reaktivaatiolta. PJP-profylaksin käyttöaiheet voi tarkistaa esimerkiksi Husin mikrobilääkehoito-oppaasta (16). Tavallisin aihe on suuriannoksinen ja pitkäkestoinen glukokortikoidihoito.
HSV:n (Herpes simplex virus) ja VZV:n reaktivaatiota ehkäisevä asikloviirilääkitys on tarpeen muun muassa alemtutsumabihoidon yhteydessä ja silloin kun potilaalla on toistuvia herpesinfektioita immunosuppressiohoidon aikana (17). Syvässä immunosuppressiossa (mm. elinsiirrot) voidaan tarvita myös sytomegalovirus (CMV) -estohoitoa.
Merkittävässä hypogammaglobulinemiassa harkitaan immunoglobuliinikorvaushoitoa, mikäli potilaalla esiintyy toistuvia bakteeri-infektioita. Eri tautiryhmissä on kansainvälisiä ohjeita immunoglobuliinien käytöstä infektioiden estossa (18).
HBV-kantajuus tulee sulkea pois ennen tiettyjen viruksen reaktivaatiolle altistavien immunosuppressiivisten hoitojen aloitusta (19,20) (liitetaulukko 1). Tuloksen ollessa positiivinen konsultoidaan infektiolääkäriä estolääkityksen tarpeesta.
Tuberkuloosi poissuljetaan ennen immunosuppressiohoitoa (21,22). Valtaosalla tartunnan saaneista tuberkuloosi jää elimistöön latentiksi (LTBI). Tällöin mikrobia on elimistössä elinkykyisenä, mutta lepotilassa, eikä tartunnan saaneella ole infektion oireita. Tulehdussolut kertyvät bakteerien ympärille muodostaen suojaavan granulooman, joka voi näkyä keuhkokuvassa arpena tai kalkkeutuneina imusolmukkeina. Tartunnan merkkinä todetaan yleensä positiivinen löydös IGRA-testissä (IFN-γ releasing assay). Aktivoitumisen todennäköisyys lisääntyy immuunipuolustuksen heikentyessä. Tämän vuoksi LTBI tulee hoitaa potilaan saadessa immunosuppressiivista hoitoa.
Muiden bakteeritautien mikrobilääkeprofylaksiaa ei käytetä immunosuppressiota aiheuttavien lääkehoitojen yhteydessä.
Lopuksi
Immunosuppressiivisten lääkehoitojen kehitys lisää vanhenevan väestön infektioriskejä. Uusien hoitojen aiheuttamat infektioriskit eroavat lääkeaineittain ja haastavat lääkärikunnan kykyä ylläpitää lääkkeisiin liittyvää osaamista. Näiden lääkkeiden käyttöön erikoistuneiden lääkärien tulee olla aktiivisia ajantasaisen tiedon jakamisessa koko lääkärikunnalle.
Suvi Niku: Luentopalkkiot (AbbVie, Pfizer).
Reetta Huttunen: Ei sidonnaisuuksia.
- 1
- Hedman K, Heikkinen, T, Huovinen P ym. Immunologia. Kustannus Oy Duodecim 2011.
- 2
- Fishman JA. Infections in immunocompromised hosts and organ transplant recipients: essentials. Liver Transpl 2011;17(suppl 3):S34–7.
- 3
- Fardet L, Petersen I, Nazareth I. Common infections in patients prescribed systemic glucocorticoids in primary care: A population-based cohort study. PLoS Med 2016;13:e1002024.
- 4
- Youssef J, Novosad SA, Winthrop KL. Infection risk and safety of corticosteroid use. Rheum Dis Clin North Am 2016;42:157–76.
- 5
- Sepriano A, Kerschebaumer A, Smolen J ym. Safety of synthetic and biological DMARDs: a systematic literature review informing the 2019 update of the EULAR recommendations for the management of rheumatoid arthritis. Ann Rheum Dis 2020;79:760–70.
- 6
- McLean-Tooke A, Aldridge C, Waugh S ym. Methotrexate, rheumatoid arthritis and infection risk: what is the evidence? Rheumatology 2009;48:867–71.
- 7
- Osiri M, Shea B, Welch V ym. Leflunomide for the treatment of rheumatoid arthritis. Cochrane Database Syst Rev 2002;9 Suppl 1.
- 8
- Dixon JS, Furst DE. Purine analogues. Kirjassa: Second line agents in the treatment of rheumatic diseases. Marcel Decker 1991.
- 9
- Suomen Reumatologinen Yhdistys. Ohjeet. www.reumatologinenyhdistys.fi/ohjeet/
- 10
- Ritter M, Pirofski L. Mycophenolate mofetil: effects on cellular immune subsets, infectious complications, and antimicrobial activity. Transpl Infect Dis 2009;11:290–7.
- 11
- Davis JS, Ferreira D, Paige E ym. Infectious complications of biological and small molecule targeted immunomodulatory therapies. Clin Microbiol Rev 2020;33:e00035-19.
- 12
- Singh J, Cameron C, Noorbaloochi S ym. The risk of serious infection with biologics in treating patients with rheumatoid arthritis: A systematic review and meta-analysis. Lancet 2015;386:258–65.
- 13
- Terveyden ja hyvinvoinnnin laitos. Infektiotaudit ja rokotukset. thl.fi/fi/web/infektiotaudit-ja-rokotukset
- 14
- Green H, Paul M, Vidal L, Leibovici L. Prophylaxis of Pneumocystis pneumonia in immunocompromised non-HIV-infected patients: systematic review and meta-analysis of randomized controlled trials. Mayo Clin Proc 2007;82:1052–9.
- 15
- Park JW, Curtis JR, Moon J ym. Prophylactic effect of trimethoprim-sulfamethoxazole for pneumocystis pneumonia in patients with rheumatic diseases exposed to prolonged high-dose glucocorticoids. Ann Rheum Dis 2018;77:644–9.
- 16
- Hus. Mikrobilääkehoito-opas. www.hus.fi/ammattilaiselle/ammattilaisten-palvelut-ja-ohjeet/infektiot/mikrobilaakehoito
- 17
- Sandherr M, Hentrich M, von Lilienfeld-Toal M ym. Antiviral prophylaxis in patients with solid tumours and haematological malignancies – update of the Guidelines of the Infectious Diseases Working Party (AGIHO) of the German Society for Hematology and Medical Oncology (DGHO). Ann Hematol 2015;94:1441–50.
- 18
- Suomen hematologiyhdistys. www.hematology.fi
- 19
- Shi Y, Zheng M. Hepatitis B virus persistence and reactivation. BMJ 2020;370:m2200.
- 20
- Shouval D, Shibolet O. Immunosuppression and HBV reactivation. Semin Liver Dis 2013;33:167–77.
- 21
- Hasan T, Au E, Chen S ym. Screening and prevention for latent tuberculosis in immunosuppressed patients at risk for tuberculosis: a systematic review of clinical practice guidelines. BMJ Open 2018;8:e022445.
- 22
- Bosch A, Valour F, Dumitrescu O ym. A practical approach to tuberculosis diagnosis and treatment in liver transplant recipients in a low-prevalence area. Med Mal Infect 2019;49:231–40.
Infection risks associated to immunosuppression need to be considered
Certain infections caused by immunosuppressive drugs can be prevented.
In recent years, many new immunosuppressive drugs have been developed for clinical use.
Some immunosuppressive agents predispose to infections more than others.
Physicians need to gain knowledge for infections associated with immunosuppression.
Suvi Niku, Reetta Huttunen